Clear Sky Science · es
VSIG10L es un determinante clave de la homeostasis esofágica y de la predisposición heredada al esófago de Barrett
Por qué esto importa para las personas con acidez
La acidez crónica es frecuente, pero solo una pequeña fracción de las personas desarrolla esófago de Barrett, una afección que puede conducir a cáncer de esófago. Este estudio formula una pregunta sencilla pero importante: ¿por qué algunas familias son mucho más propensas al esófago de Barrett que otras? Al seguir un único gen y observar cómo modela el revestimiento del esófago en humanos y ratones, los investigadores descubren un eslabón perdido entre el riesgo hereditario, el daño por reflujo y la capacidad del organismo para mantener el esófago sano.
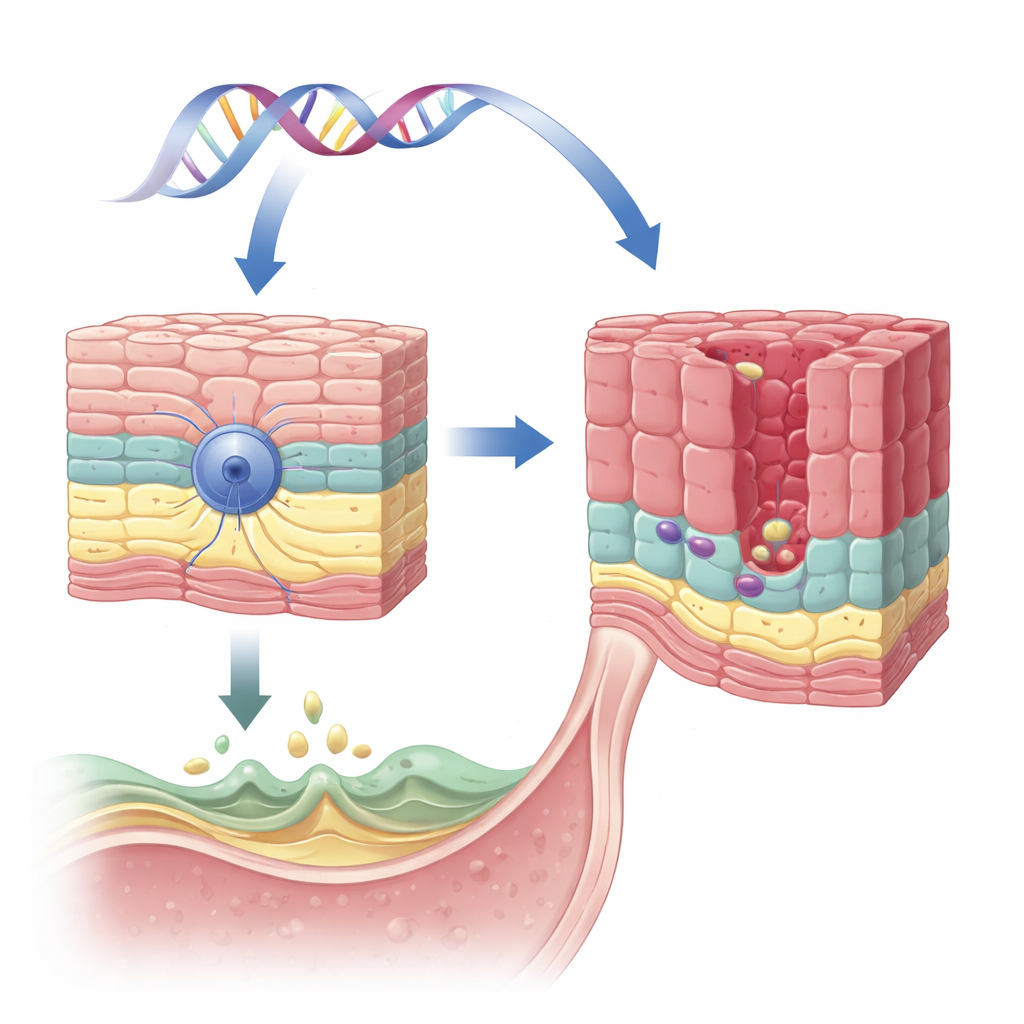
Un gen protector en el revestimiento esofágico
El equipo se centró en un gen llamado VSIG10L, previamente señalado en una gran familia con muchos miembros afectados por esófago de Barrett y cánceres relacionados. VSIG10L está activo en las capas superiores de las células escamosas que recubren el esófago, pero no en las células basales más profundas con carácter de células madre. Utilizando un método sensible de detección de ARN en tejidos humanos, de cerdo y de ratón, así como en cultivos tridimensionales de células esofágicas humanas, los investigadores demostraron que VSIG10L se enciende de forma consistente solo en las células “en maduración” justo por encima de la capa basal. Este patrón sugiere que VSIG10L ayuda a las células escamosas a completar los pasos finales de maduración y a formar una barrera estable.
Alteraciones hereditarias que debilitan la barrera
Al secuenciar el gen VSIG10L en 684 personas de 302 familias con esófago de Barrett y cáncer de esófago, los investigadores encontraron varias variantes raras y dañinas. Para probar qué hacen estas variantes, diseñaron organoides esofágicos derivados de células madre humanas a partir de un paciente portador de una de estas mutaciones. En comparación con los organoides de un donante sano, los organoides con la mutación no lograron construir la estructura escamosa normal por capas. En su lugar, a menudo formaron bolas celulares glandulares anormales que quedaron estancadas en un estado basal e inmaduro, marcado por una proteína llamada p63. Esta distorsión de la estratificación y la maduración normales refleja los pasos tempranos que se cree preceden al esófago de Barrett en los pacientes.
Modelos de ratón que recrean la enfermedad humana
Para ir más allá de los cultivos celulares, el equipo creó ratones que llevan una copia precisa de la mutación familiar humana de VSIG10L o la pérdida completa del gen. En ratones sanos, el gen correspondiente Vsig10l vuelve a estar activo únicamente en las células escamosas suprabasales. Bajo el microscopio electrónico, los ratones mutantes mostraron una pérdida notable de desmosomas—los diminutos “remaches” que fijan las células vecinas—en estas capas. Los mapas de actividad génica del estómago forestal escamoso, una región del ratón que se asemeja al esófago inferior, revelaron una amplia alteración de los programas estructurales y de diferenciación. Cuando los ratones recibieron una dieta que contenía el ácido biliar deoxicólico, imitando el reflujo crónico, el 70–100% de los animales con la mutación en Vsig10l desarrollaron extensas placas ricas en mucina similares a las del Barrett en la unión escamo-columnar, mientras que los ratones de tipo salvaje solo desarrollaron lesiones pequeñas y limitadas.
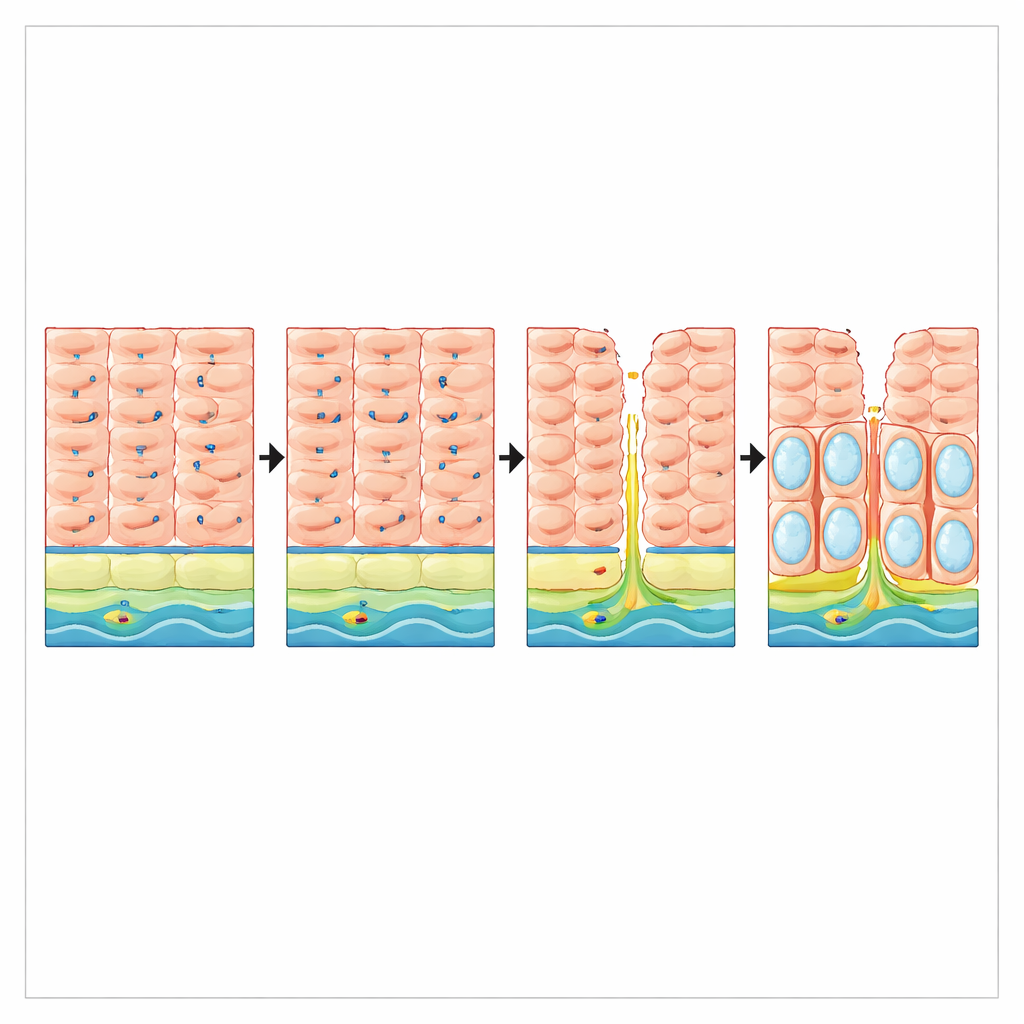
Lesión por reflujo y pérdida de protección en pacientes
Los investigadores preguntaron entonces si el propio reflujo podría alterar VSIG10L en humanos. En biopsias de pacientes con enfermedad por reflujo gastroesofágico de larga evolución pero sin esófago de Barrett, los niveles de ARN de VSIG10L fueron aproximadamente tres veces más bajos que en personas sin reflujo, aunque el marcador básico de células escamosas TP63 no varió. En cortes de tejido, el revestimiento esofágico sano mostró una franja clara de células positivas para VSIG10L por encima de la capa basal. En contraste, la mucosa dañada por reflujo presentó una expansión de células de aspecto basal ricas en p63 y una pérdida casi completa del gradiente de diferenciación positivo para VSIG10L. Estos hallazgos sugieren que el reflujo crónico erosiona no solo la integridad física del revestimiento, sino también el programa génico que mantiene su renovación ordenada.
Uniendo las piezas
En conjunto, el trabajo respalda un modelo sencillo: VSIG10L es un guardián clave de la barrera escamosa esofágica. Los defectos hereditarios en este gen, o su supresión adquirida por reflujo crónico, conducen a una pobre maduración del revestimiento, a menos anclajes entre células y a una superficie más permeable. En este estado vulnerable, la exposición repetida a ácido y bilis favorece una reparación anómala en forma de glándulas en lugar de la restauración del revestimiento escamoso original, preparando el terreno para el esófago de Barrett. Para pacientes y familias, esta investigación apunta hacia futuras pruebas genéticas que puedan identificar a los de mayor riesgo y hacia nuevas terapias destinadas a preservar o restaurar la función de VSIG10L, con el objetivo a largo plazo de prevenir el esófago de Barrett y su progresión a cáncer.
Cita: Ravillah, D., Singh, S., Katabathula, R.M. et al. VSIG10L is a major determinant of esophageal homeostasis and inherited predisposition to Barrett’s esophagus. Nat Commun 17, 2167 (2026). https://doi.org/10.1038/s41467-026-68975-3
Palabras clave: Esófago de Barrett, reflujo gastroesofágico, predisposición genética, homeostasis epitelial, riesgo de cáncer de esófago