Clear Sky Science · es
Explotar la alostería de la fucosiltransferasa humana 8 con un inhibidor covalente para suprimir la fucosilación central
Por qué bloquear un pequeño azúcar puede importar en el cáncer
Nuestras células decoran constantemente las proteínas con pequeñas cadenas de azúcar que afinan su funcionamiento. Una marca azucarada particular, llamada fucosilación central, ayuda a los tumores a crecer, diseminarse, evadir al sistema inmune e incluso resistir fármacos oncológicos modernos. Este artículo describe cómo los científicos hallaron un punto de control oculto en la enzima humana que añade este azúcar y diseñaron una nueva molécula de baja toxicidad que se engancha a ese punto de control para apagar la enzima. Su trabajo abre una vía para medicamentos que reconfiguren sutilmente los azúcares de la superficie celular en lugar de atacar directamente el ADN o las proteínas.
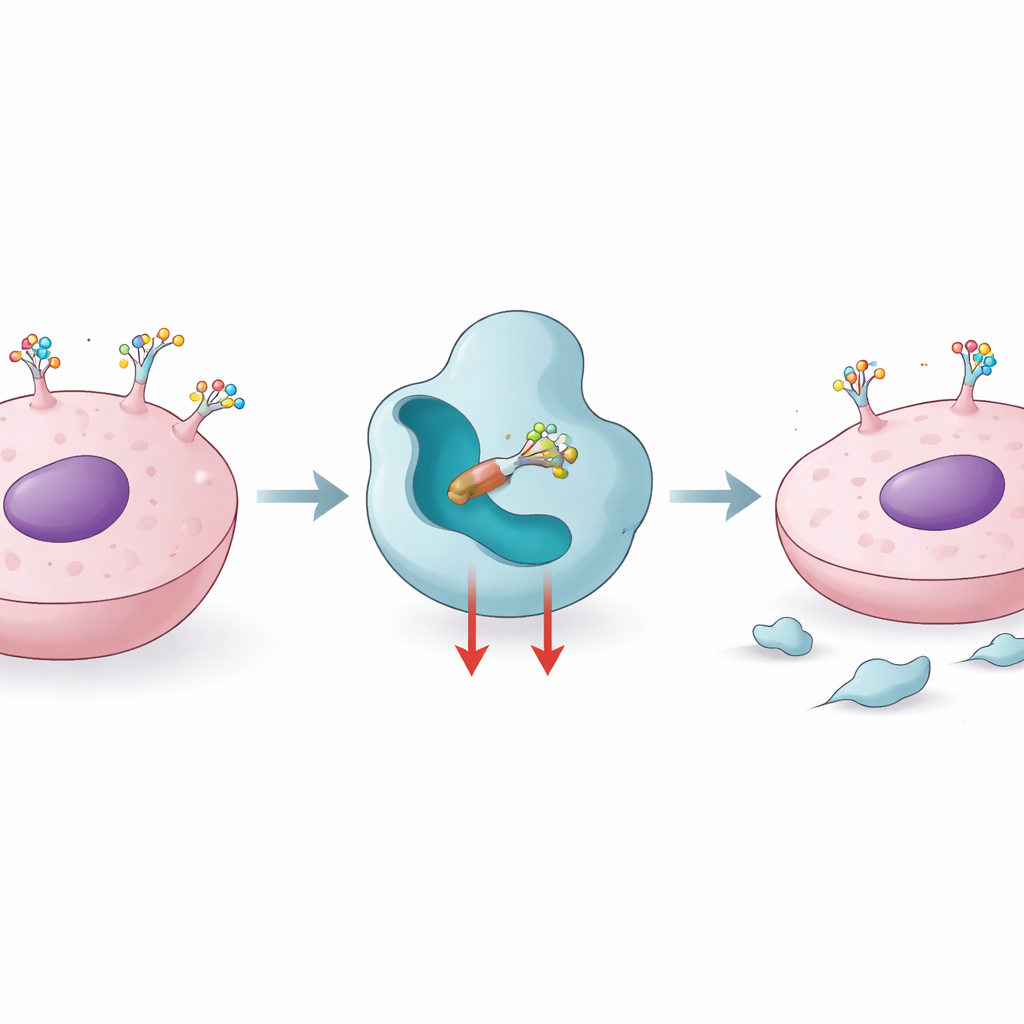
Cómo las células usan etiquetas de azúcar para moldear la enfermedad
Las proteínas que salen de la “fábrica” celular pasan por una especie de "línea de acabado" molecular donde se añaden y editan cadenas de azúcar. La fucosilación central es uno de esos pasos finales, catalizado por una enzima llamada FUT8, que añade una única fucosa a una posición clave en muchos glicanos unidos a proteínas. Cuando los niveles de FUT8 aumentan, esta marca azucarada se vuelve más frecuente en moléculas que controlan el crecimiento celular, el movimiento y el reconocimiento inmunológico. Estudios han vinculado la alta actividad de FUT8 con melanomas agresivos, cáncer de mama triple negativo, cáncer de pulmón y resistencia a fármacos dirigidos y a algunas terapias con anticuerpos. Bloquear FUT8 puede eliminar de la superficie celular ciertas proteínas que actúan como frenos inmunitarios, como PD‑1, y hacer que los tumores sean más visibles para el sistema inmune, lo que convierte a FUT8 en un objetivo atractivo para la inmunoterapia del cáncer y para mejorar medicamentos biológicos.
La necesidad de bloqueadores más inteligentes y selectivos
Diseñar fármacos contra FUT8 ha sido difícil porque muchas enzimas relacionadas usan el mismo combustible azucarado básico. Inhibidores anteriores a menudo imitaban ese combustible, provocando un apagado amplio y poco selectivo de muchas vías de fucosilación y efectos secundarios indeseados, incluidos problemas de coagulación que detuvieron un ensayo clínico. Los autores razonaron que una estrategia mejor sería evitar el concurrido sitio activo principal y, en su lugar, buscar un sitio “remoto” único en FUT8 que pudiera actuar como interruptor de control. Usando una prueba de cribado de alto rendimiento que monitorizaba la actividad de la enzima, revisaron más de seis mil compuestos y señalaron algunas moléculas alargadas que retardaban FUT8 y además reducían la invasión de células cancerosas en placas de cultivo.
Descubriendo un bolsillo de control oculto
Mediante cristalografía de rayos X, el equipo resolvió las estructuras tridimensionales de FUT8 unida a dos de estos inhibidores. Para su sorpresa, ninguno de los compuestos se situó en el lugar habitual donde se unen el donante y el aceptor del azúcar. En su lugar, ambos se alojaron en un largo bolsillo tipo canal entre dos grandes lóbulos de la enzima, cercano pero distinto del centro activo. La unión en este sitio desplazó ciertos bucles y aminoácidos clave fuera de posición, particularmente elementos que normalmente ayudan a sujetar al donante de azúcar. Simulaciones por ordenador mostraron que cuando el bolsillo estaba ocupado, el movimiento global y el paisaje energético de FUT8 cambiaban, favoreciendo conformaciones pobres para la catálisis. En otras palabras, los inhibidores actuaban alostéricamente: presionaban un botón distante que hacía que las partes funcionales de la enzima se desalinearan.
Convirtiendo una molécula hit en una herramienta covalente precisa
Con este mapa estructural, los investigadores buscaron moléculas que no solo ocuparan el bolsillo sino que además pudieran formar un enlace permanente con una lisina cercana (K216) que naturalmente oscila hacia el canal. Encontraron que un reactivo llamado SSO, que porta un éster N‑hidroxisuccinimida reactivo, se unía en la misma ranura y formaba un enlace covalente con K216, bloqueando la enzima en un estado inactivo. Partiendo de las características compartidas de SSO y su compuesto inicial NH125, combinaron fragmentos de ambos para crear una nueva molécula llamada CAIF. Las estructuras cristalinas confirmaron que CAIF se desliza a lo largo del canal, encaja entre residuos hidrofóbicos y forma un enlace covalente con K216. Este diseño potenció la inhibición de FUT8 varias veces respecto a sus compuestos progenitores, al tiempo que preservaba a enzimas estrechamente relacionadas, subrayando la forma única del bolsillo alostérico de FUT8.
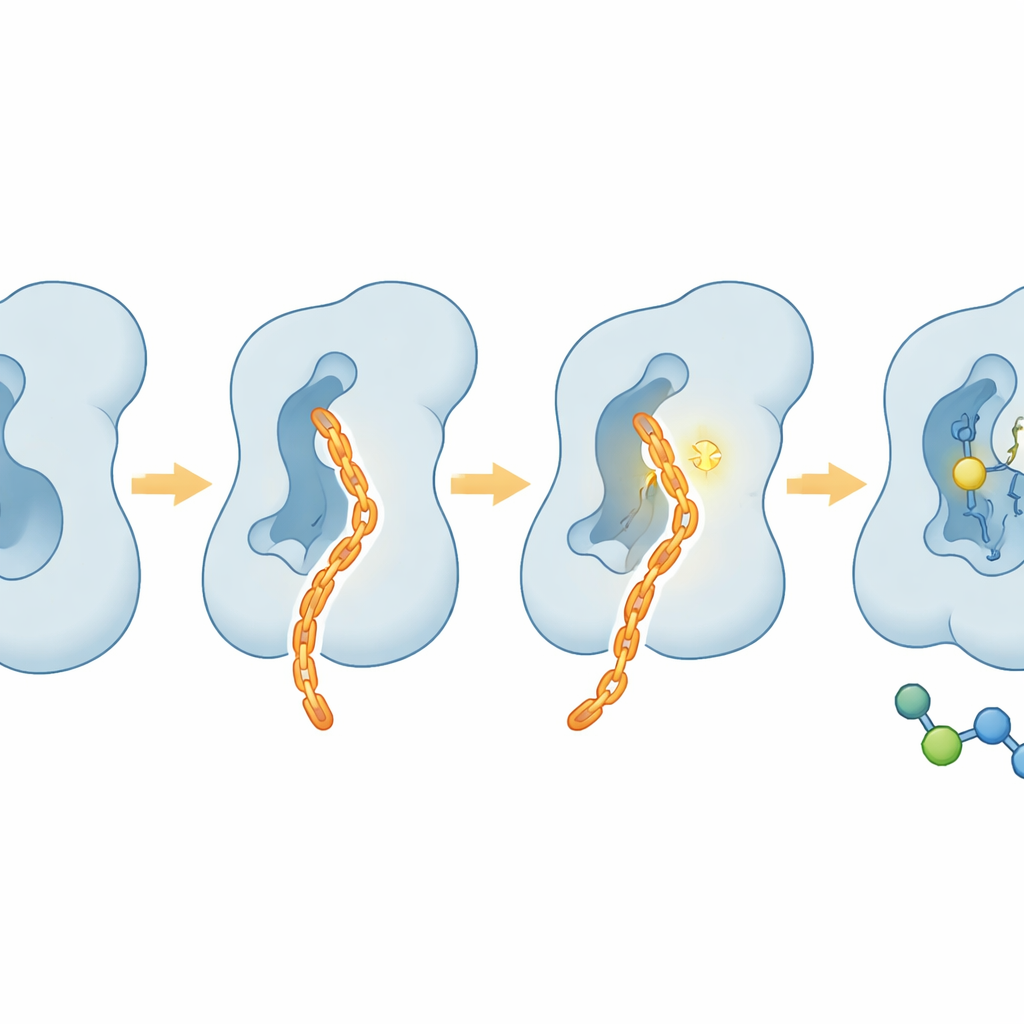
Suave con las células, duro con el comportamiento tumoral
Además de los ensayos de tubo, el equipo examinó cómo se comporta CAIF en células vivas. En varias líneas celulares humanas, CAIF mostró toxicidad mínima incluso a dosis altas, lo que indica que no envenena ampliamente la maquinaria celular. Sin embargo, redujo de forma marcada la fucosilación central en la superficie celular, como revelaron tintes que se unen a azúcares, y lo hizo con mucha mejor selectividad hacia FUT8 que los inhibidores pan‑fucosilantes anteriores. En ensayos de invasión celular, CAIF superó a un inhibidor común basado en azúcares al limitar la capacidad de las células tumorales de migrar a través de una matriz, un rasgo característico del potencial metastásico. Estos efectos concuerdan con el papel conocido de FUT8 en potenciar la invasión y la evasión inmune más que en impulsar directamente la división celular.
Qué significa esto para futuros tratamientos del cáncer
Este estudio no afirma que CAIF, por sí mismo, esté listo para convertirse en un fármaco. En cambio, demuestra que FUT8 contiene un bolsillo alostérico previamente desconocido y abordable farmacológicamente que puede ser apuntado con moléculas cuidadosamente diseñadas que forman un enlace duradero con una única lisina. Explotando este sitio, los investigadores pueden bajar selectivamente la actividad de una enzima modificadora de azúcares que se sitúa en la encrucijada de la progresión tumoral, la evasión inmune y la resistencia a fármacos, dejando en gran medida intactas a las enzimas relacionadas. El trabajo ofrece un plano para diseñar inhibidores de nueva generación que reconfiguren patrones de azúcar relevantes para la enfermedad en proteínas y que, en última instancia, puedan ampliar las herramientas para la inmunoterapia del cáncer y mejorar medicamentos basados en anticuerpos.
Cita: Jiang, J., He, D., Ke, M. et al. Exploiting human fucosyltransferase 8 allostery with a covalent inhibitor for core fucosylation suppression. Nat Commun 17, 2607 (2026). https://doi.org/10.1038/s41467-026-68971-7
Palabras clave: Inhibición de FUT8, fucosilación central, inhibidores alostéricos covalentes, glicosilación en el cáncer, diseño de fármacos contra glicosiltransferasas