Clear Sky Science · es
Transformaciones fotoinducidas por discordancia de polaridad de isoquinolinas a naftalenos
Iluminando nuevas vías para los medicamentos
Muchos fármacos modernos se basan en marcos carbonados planos y cíclicos. Cambiar un tipo de anillo por otro puede modificar radicalmente el comportamiento de un fármaco en el organismo, pero hacerlo suele requerir síntesis largas y costosas. Este estudio presenta un atajo impulsado por la luz: una forma de remodelar directamente un anillo nitrogenado común, la isoquinolina, en un anillo estrechamente relacionado compuesto solo por carbono, un naftaleno. El método funciona en condiciones suaves, tolera numerosos grupos funcionales y puede aplicarse en etapas tardías de la vida de una molécula farmacéutica, abriendo rutas más rápidas hacia tratamientos mejorados.
Por qué importa intercambiar los núcleos anulares
En el descubrimiento de fármacos, los químicos construyen y prueban amplias bibliotecas de moléculas relacionadas para ajustar propiedades como potencia, selectividad y estabilidad. Incluso cambiar un solo átomo en el anillo central puede alterar de forma marcada cómo encaja un compuesto en su diana biológica o cuánto tiempo perdura en el organismo. Las isoquinolinas y los naftalenos son ejemplos clásicos de núcleos «aparentemente iguales» intercambiables: tienen tamaño y forma similares, pero uno contiene un átomo de nitrógeno mientras que el otro está formado únicamente por carbono. Tradicionalmente, pasar de un núcleo a otro exige reconstruir la molécula desde cero, paso a laborioso paso. Una conversión directa en un solo paso entre ambos permitiría a los químicos reciclar moléculas existentes en nuevas variantes en lugar de comenzar de nuevo.
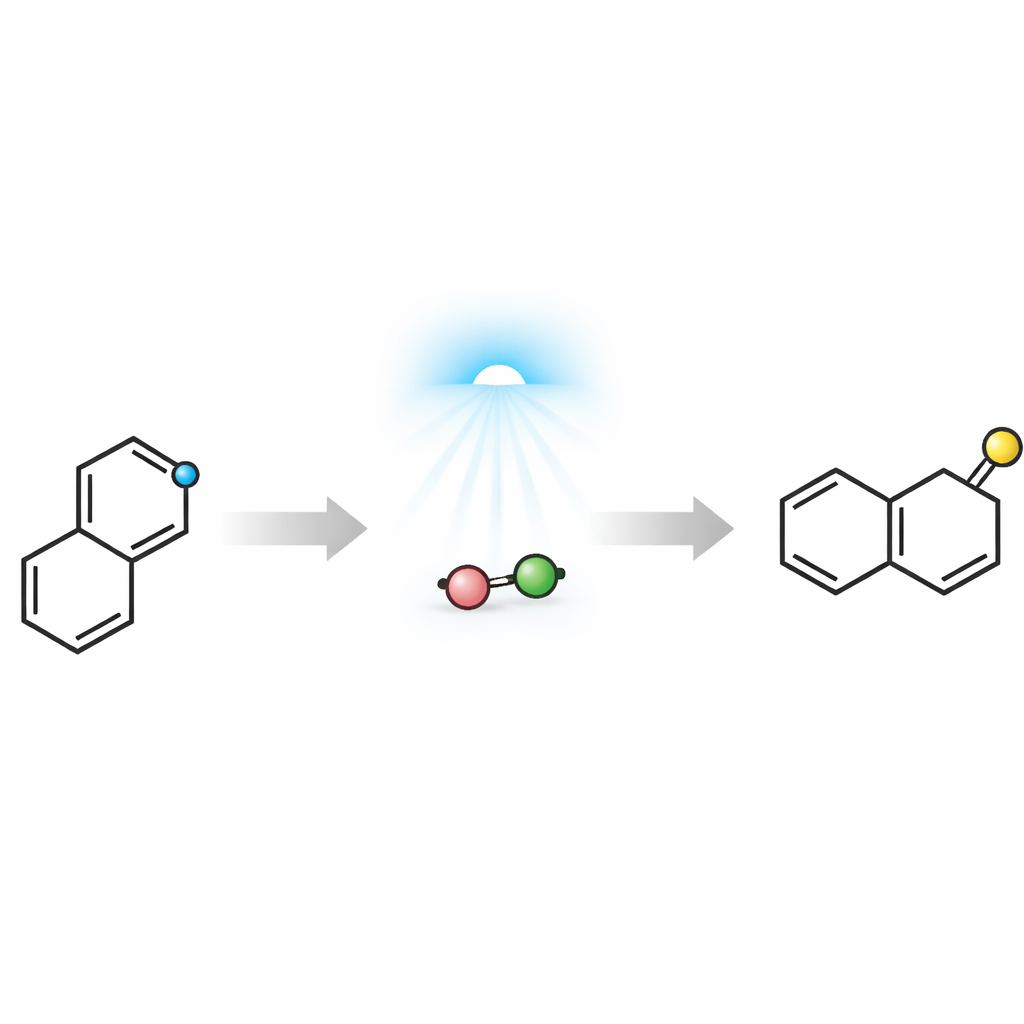
Convertir la desajuste electrónico en una ventaja
El reto es que las isoquinolinas y los alquinos utilizados para construir naftalenos son ambos relativamente pobres en electrones, por lo que normalmente se repelen entre sí en el paso clave de formación de enlace, un tipo de reacción de construcción de anillo de seis átomos. Los autores superaron este «desajuste de polaridad» reclutando luz visible y una base inorgánica simple. Cuando una isoquinolina se transforma en su sal y se empareja con carbonato, ambos forman una asociación débil que puede absorber luz azul. Estudios computacionales guiaron el diseño y mostraron que la excitación por luz transfiere un electrón del carbonato al anillo isoquinoliniun, convirtiéndolo temporalmente en un radical rico en electrones. En este estado activado, la isoquinolina puede ahora añadirse de forma escalonada a un alquino pobre en electrones, formando un nuevo sistema anular que finalmente se reorganiza en un naftaleno mientras expulsa un fragmento que contiene nitrógeno.
Sondeando la reacción en el laboratorio
Experimentalmente, la transformación es sencilla de ejecutar: sales de isoquinoliniun, alquinos y carbonato sódico se mezclan en etanol bajo LED azules sin fotocatalizador adicional. El equipo optimizó las condiciones, demostrando que el carbonato es crucial no solo como base sino también como donante de electrones, y que los iones bromuro ayudan a promover el proceso. Trampas de radicales detuvieron la reacción y capturaron aductos intermedios, apoyando la vía radicalaria propuesta por los cálculos. Experimentos espectroscópicos confirmaron que el par isoquinoliniun–carbonato es el verdadero complejo absorbente de luz, y cambiar los contraionos o las bases alteró los rendimientos de maneras consistentes con su capacidad para participar en transferencia electrónica.
De sistemas modelo a moléculas tipo fármaco
Una vez ajustadas las condiciones de reacción, los autores demostraron un amplio alcance. Muchos alquinos con distintas sustituciones participaron, incluidos aquellos con grupos sensibles como yodo, dobles enlaces adicionales y fragmentos de productos naturales o fármacos existentes. También funcionó una amplia gama de sales de isoquinoliniun, incluso las congestionadas o las que contienen heterociclos, dando acceso a naftalenos multisustituidos que son difíciles de preparar por vías tradicionales. El método incluso pudo remodelar moléculas bioactivas complejas como el inhibidor PRMT3 SGC707 y el fármaco contra vasoespasmo fasudil en sus análogos naftalénicos en una sola operación en etapa tardía. Los nuevos productos llevan grupos éster que actúan tanto como potenciales puntos de unión a proteínas como versátiles puntos de entrada sintéticos.
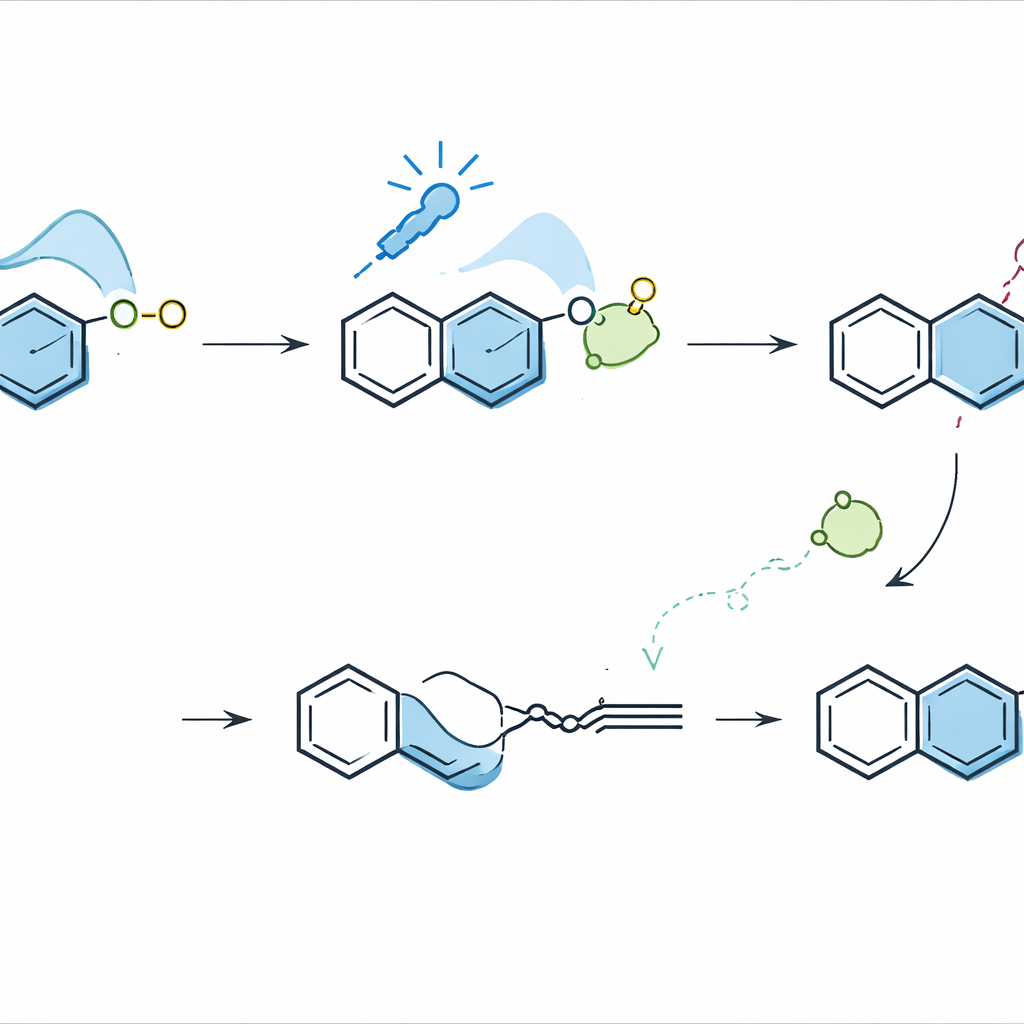
Construyendo arquitecturas mayores a partir de los nuevos anillos
Los ésteres de naftaleno recién formados no son solo productos finales; sirven como bloques de construcción para estructuras más elaboradas. El equipo mostró una serie de reacciones posteriores que convierten estos ésteres en hidrocarburos aromáticos policíclicos de alto valor y ligandos quirales, tales como benzofluorenonas, carbazoles, BINOLs y QUINOLs—andamiajes ampliamente usados en ciencia de materiales y catálisis asimétrica. En otra demostración, utilizaron el método como paso clave en la preparación de un análogo del adapaleno, un fármaco dermatológico, partiendo de un precursor de isoquinolina fácilmente ensamblado.
Qué significa esto de cara al futuro
Al usar luz visible para invertir el carácter electrónico de un anillo que contiene nitrógeno, este trabajo convierte una reacción previamente desfavorable en una potente herramienta de edición esqueletal. Los químicos pueden ahora convertir isoquinolinas abundantes directamente en naftalenos ricamente funcionalizados, evitando rutas sintéticas largas y preservando cadenas laterales delicadas. Para quienes no son especialistas, la conclusión es que «reciclar» moléculas existentes en nuevos núcleos se está volviendo más práctico, lo que podría acelerar la búsqueda de mejores fármacos y materiales avanzados a la vez que reduce costos y residuos.
Cita: Zhang, C., Zhang, J., Lan, Y. et al. Photoinduced polarity-mismatched transformations of isoquinolines into naphthalenes. Nat Commun 17, 2547 (2026). https://doi.org/10.1038/s41467-026-68969-1
Palabras clave: edición esqueletal, fotquímica, isoquinolina, naftaleno, descubrimiento de fármacos