Clear Sky Science · es
FANCD2 frena la progresión de las horquillas y evita la fragilidad en orígenes tempranos tras la re-replicación
Cuando las copias del ADN se desvían ligeramente del guion
Cada vez que una célula se divide, debe copiar su biblioteca de ADN completa exactamente una vez. Si partes de esa biblioteca se copian dos veces, o se copian de forma apresurada y descuidada, el resultado puede ser cromosomas rotos y mutaciones que fomentan el cáncer. Este estudio examina qué ocurre cuando las salvaguardas de la célula contra rondas extra de copiado comienzan a fallar y revela cómo una proteína de reparación llamada FANCD2 interviene para evitar que células con un comportamiento levemente errático deslicen hacia un caos genómico total.
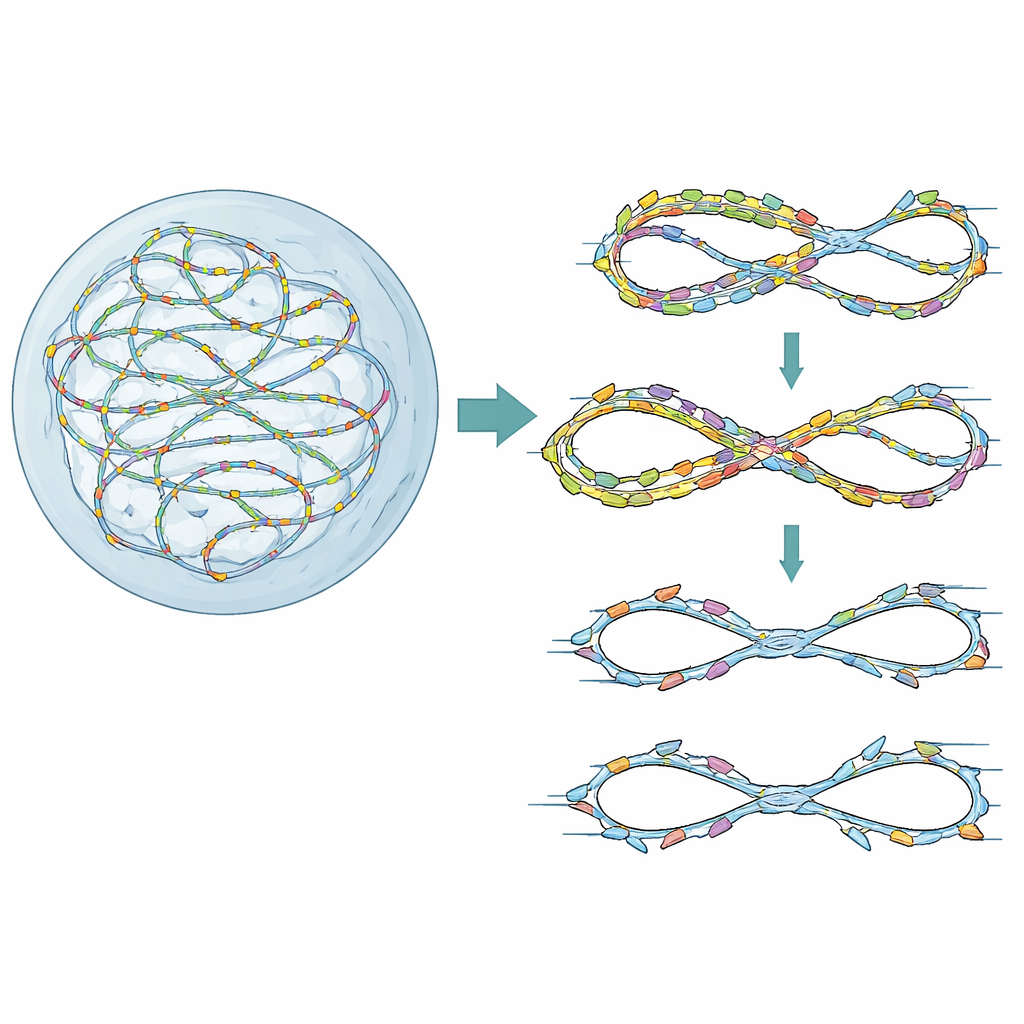
Barandillas para una copia limpia
Nuestros cromosomas se duplican desde miles de puntos de inicio, u “orígenes”, que se autorizan y luego se activan en una secuencia cuidadosamente temporizada. Una pequeña proteína llamada Geminin ayuda normalmente a garantizar que cada origen se active solo una vez por ciclo celular. Cuando Geminin se pierde o se debilita, algunos orígenes pueden reactivarse sobre ADN ya copiado, una situación conocida como re-replicación. Las células cancerosas, que con frecuencia sobreproducen factores de autorización, son especialmente propensas a este problema. Los autores usaron primero una pantalla genética de alto contenido en células humanas predispuestas a re-replicación de bajo nivel por depleción de Geminin. Preguntaron qué genes de reparación del ADN y de control de puntos de control se vuelven cruciales en este estado estresado y encontraron que FANCD2, mejor conocida por reparar entrecruzamientos de ADN en la anemia de Fanconi, surgió como una protectora clave de la supervivencia celular y la integridad del genoma.
Un primer interviniente en máquinas de copiado sobrecargadas
El equipo siguió entonces dónde y cuándo aparece FANCD2 en células que experimentan re-replicación. Poco después de eliminar Geminin, FANCD2 se acumula rápidamente en la cromatina y forma focos nucleares brillantes, mucho antes de que se detecte una rotura generalizada del ADN. Usando marcaje del ADN recién sintetizado junto con ensayos de proximidad, mostraron que FANCD2 se recluta directamente a las máquinas de replicación activas, especialmente en células cuyo ADN ya se está copiando por segunda vez. En células sincronizadas liberadas hacia el siguiente ciclo de división, emergió una población distintiva con un patrón difuso de sobre-replicación del ADN. Estas células mostraron señales intensas de FANCD2 y RPA, indicando estrés de replicación en curso, y quedaron retenidas en el umbral previo a la mitosis por un punto de control activo, lo que sugiere que FANCD2 forma parte de una respuesta temprana que estabiliza las horquillas estresadas en lugar de simplemente reaccionar ante ADN roto.
Conteniendo horquillas desbocadas y huecos ocultos
Para probar cómo FANCD2 moldea la copia del ADN, los investigadores combinaron la pérdida de Geminin con la depleción de FANCD2. Sorprendentemente, eliminar FANCD2 no aumentó la fracción de células con genomas claramente re-replicados. En su lugar, ensayos de fibras de ADN a nivel de molécula única revelaron que las horquillas de replicación avanzaron más y se volvieron más asimétricas, una señal de progresión irregular e inestable. Estas horquillas más rápidas dejaron más huecos de cadena sencilla en el ADN recién sintetizado, vistos como focos intensos de RPA y BrdU nativo y confirmados por la sensibilidad de los tractos marcados a una enzima que corta regiones de cadena sencilla. Las células que carecían tanto de Geminin como de FANCD2 mostraron un aumento de roturas cromosómicas, fragmentos, cuerpos nucleares y micronúcleos, todos indicadores de inestabilidad genómica severa. Bloquear PARP, un factor que normalmente ayuda a gestionar tales huecos, imitaron y empeoró estos defectos, subrayando que la formación descontrolada de huecos es central en el daño.
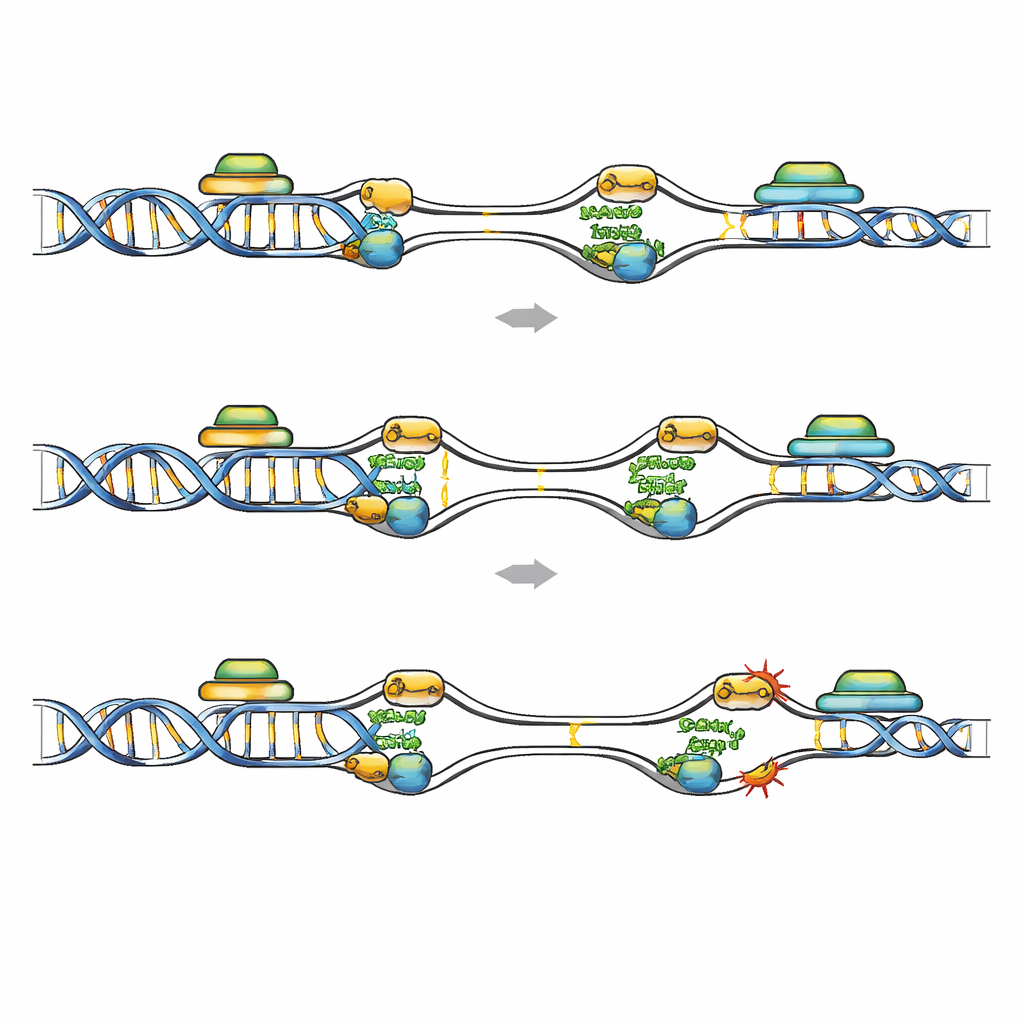
Puntos calientes frágiles donde copiar y transcribir colisionan
El mapeo a nivel genómico de la unión de FANCD2 ofreció una visión de dónde la re-replicación es más peligrosa. En células leucémicas con depleción de Geminin, FANCD2 se desplazó desde los clásicos sitios frágiles comunes hacia orígenes de replicación que se activan temprano y están insertados en genes cortos, ricos en GC y altamente transcritos. Estas regiones presentan marcas de transcripción activa y son propensas a R-loops, donde el ARN naciente se hibrida con su plantilla de ADN, lo que puede bloquear la replicación. Conjuntos de datos públicos mostraron más daño en el ADN y señales elevadas de híbridos ARN–ADN en genes enriquecidos en FANCD2 tras la pérdida de Geminin, y estas regiones se solaparon con los llamados sitios frágiles de replicación temprana. Cuando la transcripción se atenuó de forma general con un fármaco, o cuando los R-loops se eliminaron específicamente mediante sobreexpresión de RNasa H1, el número de focos de FANCD2, RPA y daño en el ADN en células deficientes en Geminin disminuyó de manera notable. Esto indica que las colisiones entre orígenes reactivados y unidades de transcripción activas, amplificadas por R-loops, crean puntos calientes frágiles que FANCD2 debe proteger.
Afinando la protección mediante etiquetas químicas
FANCD2 se activa en parte por la adición de una pequeña etiqueta similar a la ubiquitina. Al depletar FANCA, un componente central de la maquinaria de etiquetado, y al usar células que expresan un mutante de FANCD2 resistente a esta modificación, los autores mostraron que la mono-ubiquitinación mejora la supervivencia de células en re-replicación pero no es absolutamente indispensable. Incluso FANCD2 no etiquetada proporcionó protección parcial, consistente con roles distintos tanto en la detección como en la estabilización de horquillas estresadas. El panorama global es que FANCD2 ayuda a frenar y organizar la replicación en orígenes tempranos vulnerables y limita cuántos y cuán grandes llegan a ser los huecos de cadena sencilla.
Por qué esto importa para el tratamiento del cáncer
Para no especialistas, el mensaje central es que no todos los errores de replicación son catastróficos desde el principio. La re-replicación leve, como ocurre en algunos tumores, puede tolerarse si sistemas protectores como FANCD2 mantienen bajo control la replicación desbocada y evitan que los huecos frágiles se conviertan en cromosomas rotos. Cuando esta salvaguarda se elimina o se desborda, los mismos errores de autorización de bajo nivel escalan rápidamente hasta fragmentar el genoma. Dado que la pérdida de Geminin y los defectos en la autorización de replicación están enriquecidos en células cancerosas, y muchos tumores ya presentan debilidades en la red Fanconi/BRCA, las vulnerabilidades aquí descritas sugieren estrategias terapéuticas: combinar inhibidores que empujen a las células cancerosas hacia la re-replicación con fármacos que exacerben la acumulación de huecos, como los inhibidores de PARP, podría llevar selectivamente a las células malignas más allá de su límite de tolerancia mientras se preservan las células normales con protección intacta.
Cita: Badra-Fajardo, N., Karydi, E., Bayona-Feliu, A. et al. FANCD2 restrains fork progression and prevents fragility at early origins upon re-replication. Nat Commun 17, 2478 (2026). https://doi.org/10.1038/s41467-026-68966-4
Palabras clave: estrés de replicación del ADN, FANCD2, Geminin, re-replicación, inestabilidad genómica