Clear Sky Science · es
El plegamiento inducido por asociación rige el ensamblaje del receptor ligero sustituto y el receptor pre-B
Cómo nuestro cuerpo prueba los nuevos anticuerpos
Antes de que una célula B joven en la médula ósea pueda incorporarse al sistema inmunitario, debe aprobar una prueba exigente: ¿puede construir un núcleo de anticuerpo funcional? Este artículo explora cómo una versión "de ensayo" de una parte del anticuerpo, denominada cadena ligera sustituta, contribuye a llevar a cabo esa prueba. Al observar cómo estas proteínas se pliegan y encajan, los autores revelan un sistema de control de calidad oculto que decide qué anticuerpos futuros son lo bastante buenos para conservarse y cuáles se descartan.
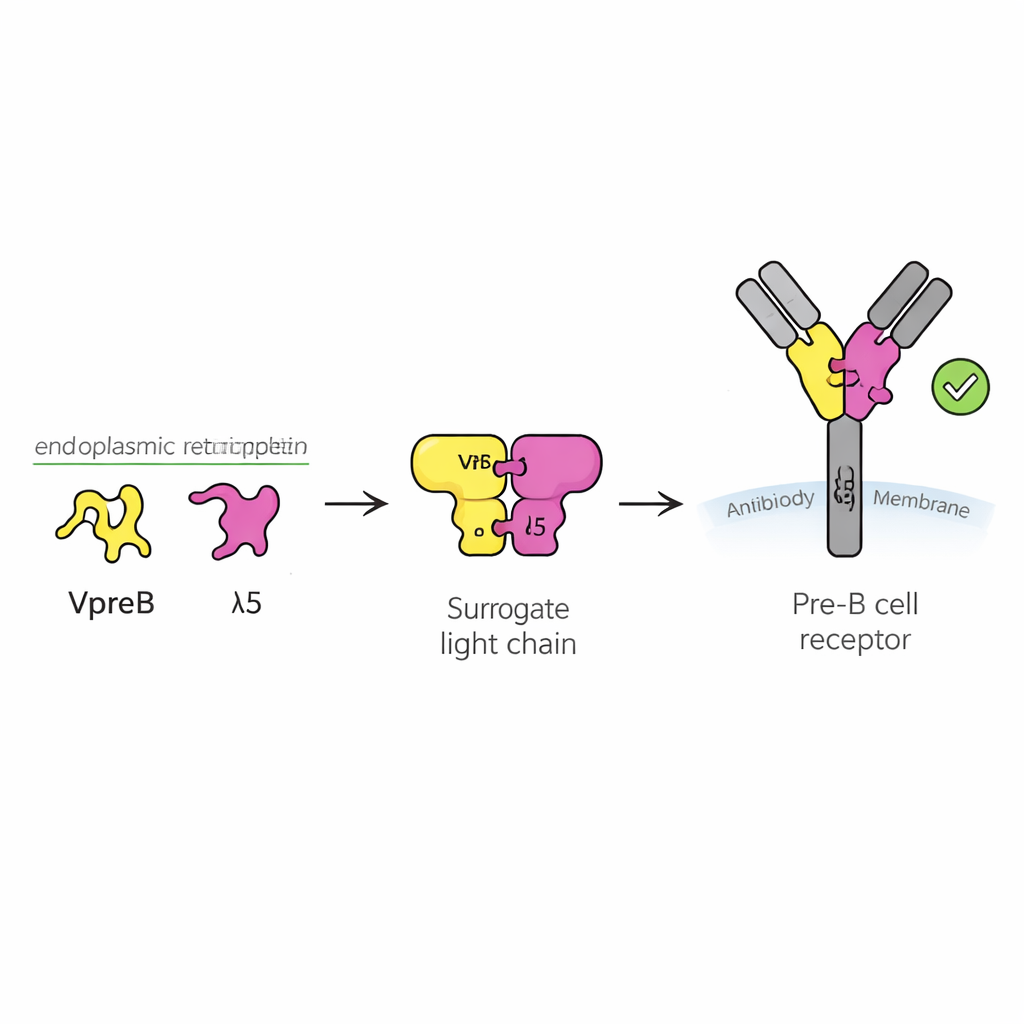
Un punto de control de seguridad para células inmunitarias jóvenes
Los anticuerpos son proteínas con forma de Y que reconocen agentes patógenos. Se componen de dos partes principales: cadenas pesadas y cadenas ligeras. Durante el desarrollo de las células B, la cadena pesada se produce primero, y la célula debe determinar si esa nueva cadena pesada es útil antes de invertir energía en fabricar una cadena ligera a juego. Para ello, la célula utiliza un sustituto temporal llamado cadena ligera sustituta, formado por dos proteínas denominadas VpreB y λ5. Junto con la cadena pesada, forman el receptor pre-B, un sensor en la superficie celular que envía una señal de “adelante” o “alto”. Alrededor de la mitad de las cadenas pesadas recién reordenadas fracasan en esta prueba, por lo que entender cómo funciona la cadena ligera sustituta es clave para comprender cómo se construye un repertorio de anticuerpos sano.
Plegamiento por asociación: ayudar a un socio inestable
Los autores hallaron que uno de los componentes, VpreB, está en gran medida desestructurado e inestable cuando está solo. Usando técnicas biofísicas, mostraron que solo adopta su forma tridimensional correcta cuando se une a λ5. Un tramo corto de λ5, con forma de hebra beta, se inserta en VpreB y completa su estructura, como encajar un diente faltante en un engranaje. Este "plegamiento inducido por asociación" no solo estabiliza a VpreB, sino que también crea una asociación muy estrecha entre ambas proteínas, con una afinidad en el rango de los nanomolares bajos. En las células, solo cuando VpreB y λ5 se ensamblan en esta cadena ligera sustituta evitan la retención en el retículo endoplásmico y son secretadas o transportadas más adelante, subrayando cómo el plegamiento y el control de calidad están estrechamente acoplados.
Terminar la cadena pesada y pasar la inspección
La historia no termina con VpreB y λ5. Una región crucial de la cadena pesada, llamada CH1, está inicialmente desestructurada y se mantiene dentro de la célula. Los investigadores demostraron que λ5, actuando en cierto modo como una chaperona, puede desencadenar el plegamiento de CH1 cuando se unen. Este segundo paso de plegamiento inducido por asociación es esencial para construir el receptor pre-B completo y permitir que abandone el retículo endoplásmico y alcance la superficie celular. Curiosamente, ambas partes de la cadena ligera sustituta —VpreB y λ5— pueden contactar la cadena pesada, pero solo λ5 es capaz de impulsar a CH1 hacia su estado final, competente para plegarse. Cuando esto no ocurre, el receptor parcial se retiene y la célula efectivamente rechaza esa cadena pesada.
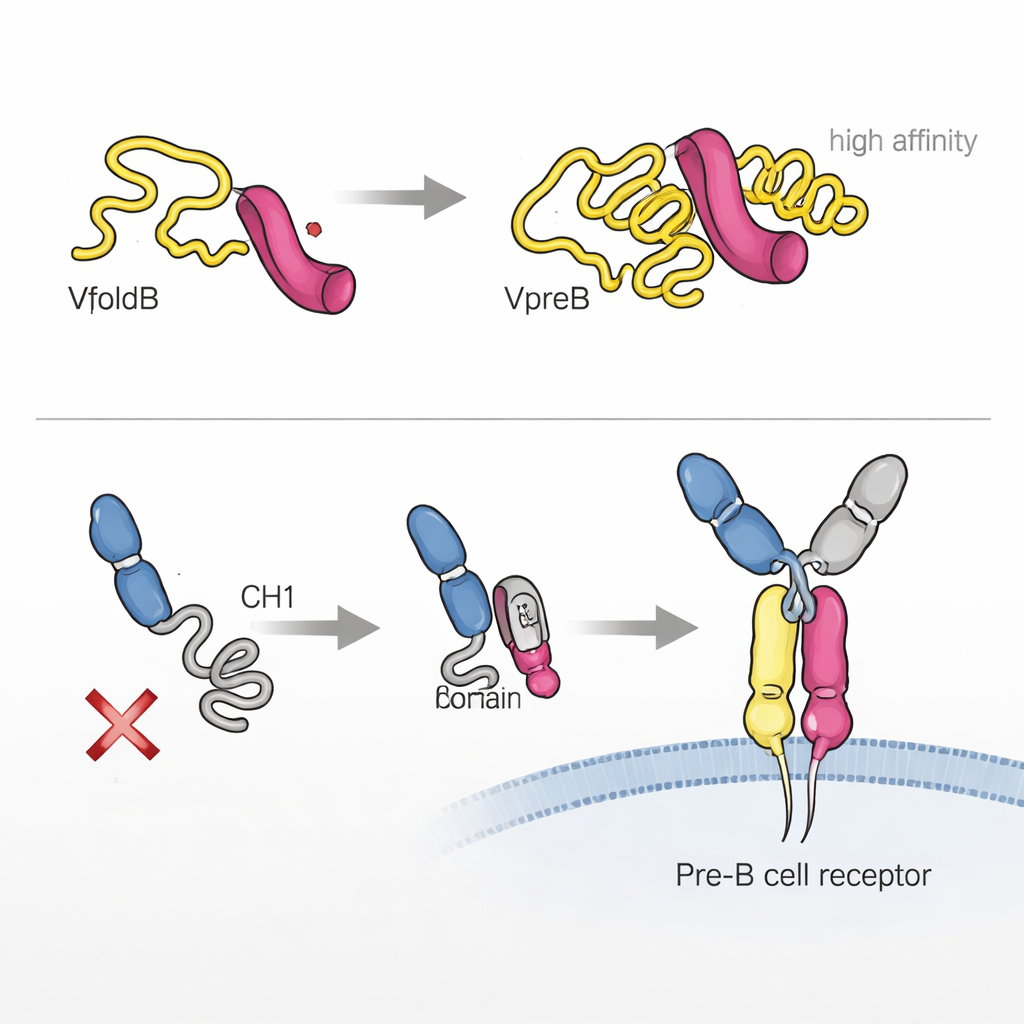
Colas flexibles que afinan la unión y la señalización
Tanto VpreB como λ5 llevan segmentos flexibles y desestructurados conocidos como regiones únicas, que no se parecen a secuencias proteicas conocidas. Aunque estas colas no son estrictamente necesarias para que las dos proteínas se ensamblen en un tubo de ensayo, el equipo descubrió que influyen fuertemente en la rapidez con la que se forma la cadena ligera sustituta, en su estabilidad y en cuánto se une a segmentos de la cadena pesada. En las células, la eliminación de estas regiones redujo la eficiencia con la que los complejos ensamblados eran secretados. La cola de λ5, en particular, emergió como multifuncional: acelera el ensamblaje, es esencial para ciertos contactos con la región variable de la cadena pesada y contribuye de forma importante a cómo el receptor pre-B se compromete con antígenos y otros ligandos. En algunos casos, la fuerza de unión de una combinación cadena ligera sustituta–cadena pesada se acercó a la de un fragmento de anticuerpo normal.
Por qué esto importa para la diversidad de anticuerpos
Al cartografiar estos eventos escalonados de plegamiento y ensamblaje, los autores proponen que la cadena ligera sustituta hace más que simplemente mantener la cadena pesada en su sitio. Actúa como una inspectora dinámica, usando su núcleo estructurado y sus colas flexibles para detectar si una cadena pesada puede plegarse correctamente e interactuar de forma productiva con posibles blancos. Las combinaciones exitosas se pliegan, se estabilizan y se les permite llegar a la superficie celular, donde envían señales que permiten que la célula B continúe madurando. Las combinaciones defectuosas quedan atrapadas y, eventualmente, se eliminan. Para el público general, la conclusión es que tu sistema inmunitario opera una sofisticada “banco de pruebas” para los anticuerpos futuros, construida a partir de proteínas que literalmente se pliegan entre sí, asegurando que solo los núcleos de anticuerpo bien comportados avancen para defenderte.
Cita: König, J., Sarmiento Alam, N.C., He, R. et al. Association-induced folding governs surrogate light chain and pre-B cell receptor core assembly. Nat Commun 17, 1202 (2026). https://doi.org/10.1038/s41467-026-68965-5
Palabras clave: Desarrollo de células B, Plegamiento de anticuerpos, Cadena ligera sustituta, Control de calidad de proteínas, Receptor pre-B