Clear Sky Science · es
Desbloqueando la deracemización enzimática de allenos estructuralmente diversos mediante fotoenzimas diseñadas
Por qué importa combinar y emparejar moléculas
Muchos fármacos funcionan solo cuando sus átomos están dispuestos de una manera tridimensional muy específica, como una mano izquierda que encaja en un guante izquierdo pero no en uno derecho. Los químicos a menudo pueden fabricar estas moléculas “de una sola mano”, pero resulta difícil hacerlo de forma limpia cuando los bloques de construcción son complejos. Este artículo aborda ese reto para una clase complicada de estructuras torcidas llamadas allenos, empleando enzimas impulsadas por luz diseñadas a medida. El trabajo muestra cómo se pueden combinar biología y fotoquímica para separar la “mano” molecular deseada de una mezcla aleatoria, prometiendo vías más rápidas y limpias hacia futuros fármacos y materiales.
Bloques torcidos con un gran beneficio
Los allenos son cadenas lineales de tres átomos de carbono con dos enlaces dobles adyacentes, pero esta disposición simple tuerce el espacio de forma que confiere quiralidad al conjunto molecular. Estos giros axiales aparecen en productos naturales, agentes de protección de cultivos y catalizadores avanzados. Desafortunadamente, los métodos tradicionales para sintetizar allenos quirales tienden a ser muy especializados: un catalizador que funciona de forma excelente para un alleno a menudo fracasa con otro que presenta cambios estructurales pequeños. Incluso los catalizadores químicos impulsados por luz desarrollados recientemente luchan con este problema. Como resultado, los químicos deben rediseñar repetidamente los catalizadores desde cero al explorar nuevos allenos, lo que ralentiza el descubrimiento y aumenta los residuos.
Tomando la selectividad de la naturaleza y añadiendo luz
Las enzimas en los sistemas vivos sobresalen en reconocer y transformar formas específicas con notable precisión, pero evolucionaron para objetivos naturales, no para allenos sintéticos. Los autores se propusieron crear una “fotoenzima” que combine la selectividad tipo enzima con la capacidad de aprovechar la luz como fuente de energía. Partieron de un andamiaje proteico llamado CTB10 y lo reprogramaron genéticamente para incorporar un aminoácido no natural que actúa como una pequeña antena luminosa integrada. Cuando este bloque especial absorbe luz ultravioleta, puede transferir energía a un alleno cercano, excitándolo temporalmente y permitiendo que su giro se reordene. Al repetir este proceso muchas veces, la enzima puede eliminar selectivamente una mano de una mezcla 50:50 y dejar principalmente la otra. 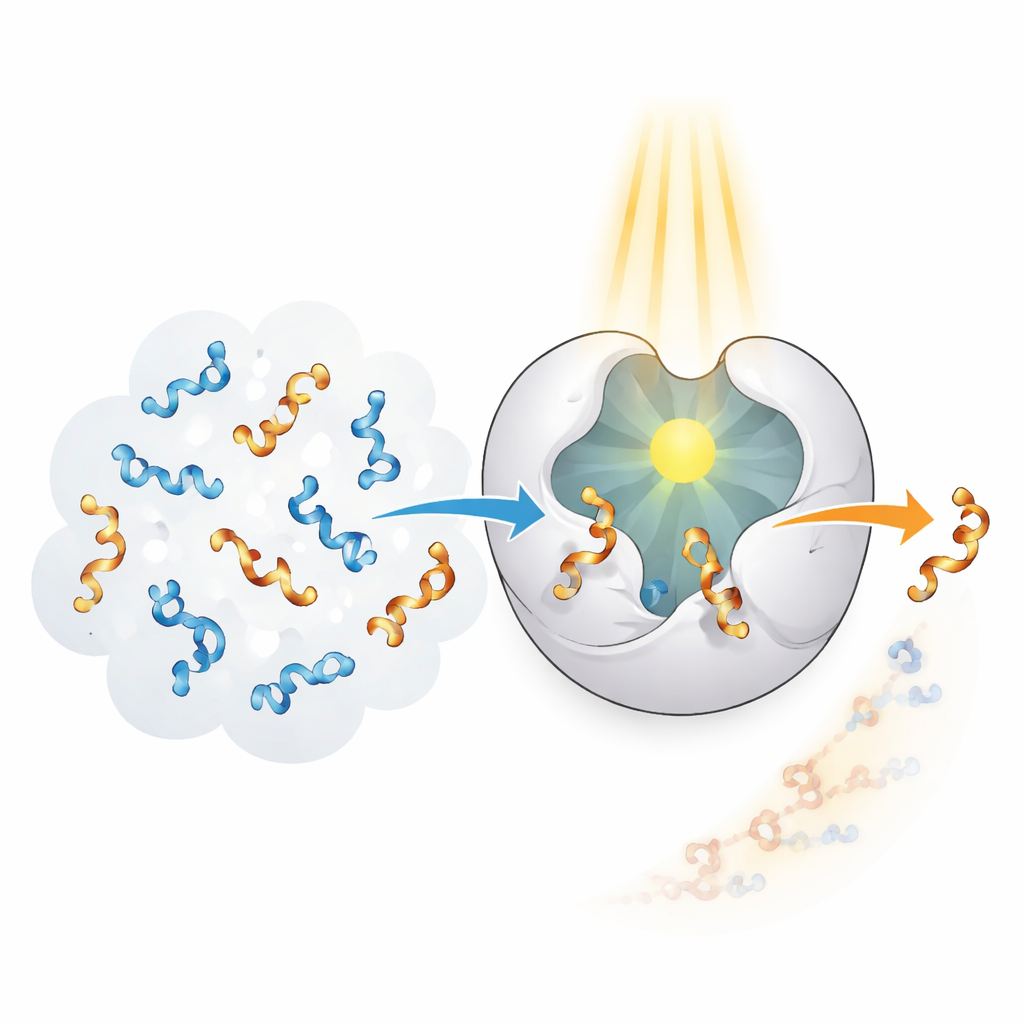
Esculpir cavidades a la medida para muchos huéspedes distintos
Diseñar un sistema así no es tan simple como iluminar una proteína. El equipo usó modelado por ordenador, mutaciones estratégicas y capturas por rayos X para esculpir varias versiones de la fotoenzima, cada una con una cavidad interna ligeramente distinta. Estas cavidades mantienen al alleno en una posición definida junto a la antena luminosa y estabilizan partes clave de la molécula mediante enlaces de hidrógeno e interacciones de empaquetamiento sutiles. Paso a paso, los investigadores mejoraron tanto la fuerza de unión como la alineación entre la enzima y el alleno, que son cruciales para una transferencia de energía eficiente. Las variantes finales mostraron un rendimiento impresionante, convirtiendo ácidos carboxílicos de alleno, ésteres y amidas en productos de una sola mano con purezas muy altas, a menudo por encima del 99% de una mano, y lo hicieron en presencia de aire sin necesidad de condiciones delicadas.
Observando el mecanismo a resolución atómica
Para entender por qué las nuevas fotoenzimas prefieren una mano sobre la otra, los autores cristalizaron pares enzima‑sustrato y los examinaron a resolución atómica. Encontraron que la mano de alleno favorecida se sitúa más cerca del grupo captador de luz y puede adoptar varias formas ligeramente diferentes, todas compatibles con una transferencia de energía eficiente. La mano desfavorecida se une débilmente o queda más alejada, lo que la hace mucho menos propensa a excitarse. Experimentos adicionales con materiales de partida puros, derecho y izquierdo, confirmaron este sesgo: la enzima convierte rápidamente la mano preferida en un intermedio reactivo, que luego se relaja en solución volviendo a una mezcla donde la mano opuesta se acumula. En esencia, la proteína actúa como un torniquete molecular, excitando y consumiendo repetidamente una mano mientras permite que la otra se acumule. 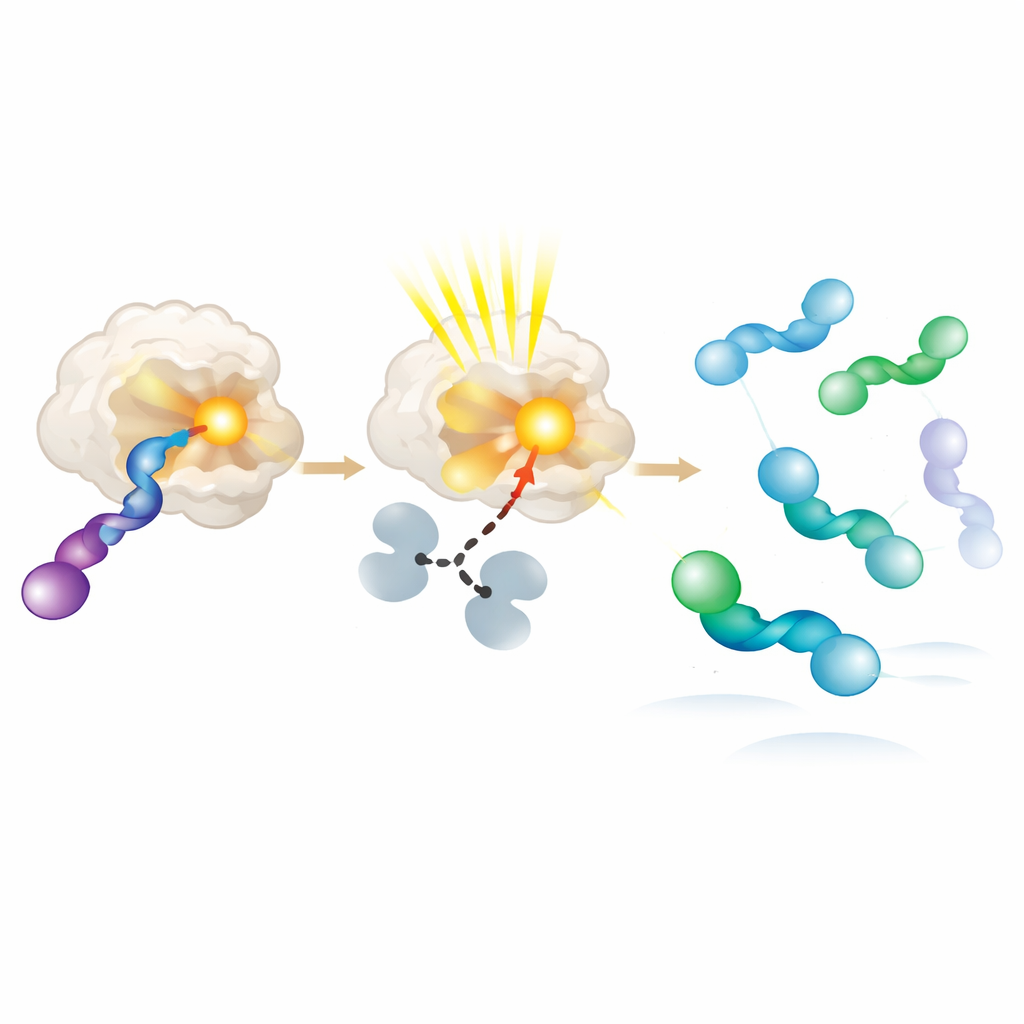
Qué significa esto para la química futura
Para los no especialistas, el mensaje principal es que el equipo ha creado una máquina proteica programable que usa la luz para clasificar y mejorar moléculas torcidas con una versatilidad sin precedentes. En lugar de diseñar un catalizador químico completamente nuevo para cada objetivo, los investigadores pueden ahora partir de esta plataforma de fotoenzimas y ajustar su cavidad interna para aceptar muchos allenos diferentes. Este enfoque reduce la brecha entre el control exquisito de la naturaleza y la necesidad de la industria química de métodos amplios y robustos. A largo plazo, tales enzimas alimentadas por luz podrían ayudar a los químicos a preparar bloques de construcción complejos y de una sola mano para fármacos y materiales de forma más eficiente, con menos pasos y menos residuos.
Cita: Fu, K., Li, M., Deng, Z. et al. Unlocking enzymatic deracemization of structurally diverse allenes by designed photoenzymes. Nat Commun 17, 2082 (2026). https://doi.org/10.1038/s41467-026-68964-6
Palabras clave: fotoenzima, deracemización, alleno quiral, biocatálisis, transferencia de energía triplete