Clear Sky Science · es
La infección por HCMV altera las funciones de barrera y promueve la transición epitelio–mesénquima en un modelo de organoide de colangiocito
Por qué importa esta historia del virus en el hígado
El citomegalovirus humano es un virus muy común que la mayoría de nosotros llevamos sin saberlo. Sin embargo, en recién nacidos y en personas con sistemas inmunitarios frágiles puede asociarse a problemas graves del hígado y de los conductos biliares, incluida una enfermedad infantil rara pero devastadora llamada atresia biliar. Este estudio utiliza conductos biliares humanos en miniatura cultivados en el laboratorio para mostrar cómo el virus puede dañar directamente estos tubos delicados y desencadenar cambios fibróticos que podrían ayudar a explicar las relaciones debatidas durante mucho tiempo entre la infección y la enfermedad hepática crónica.
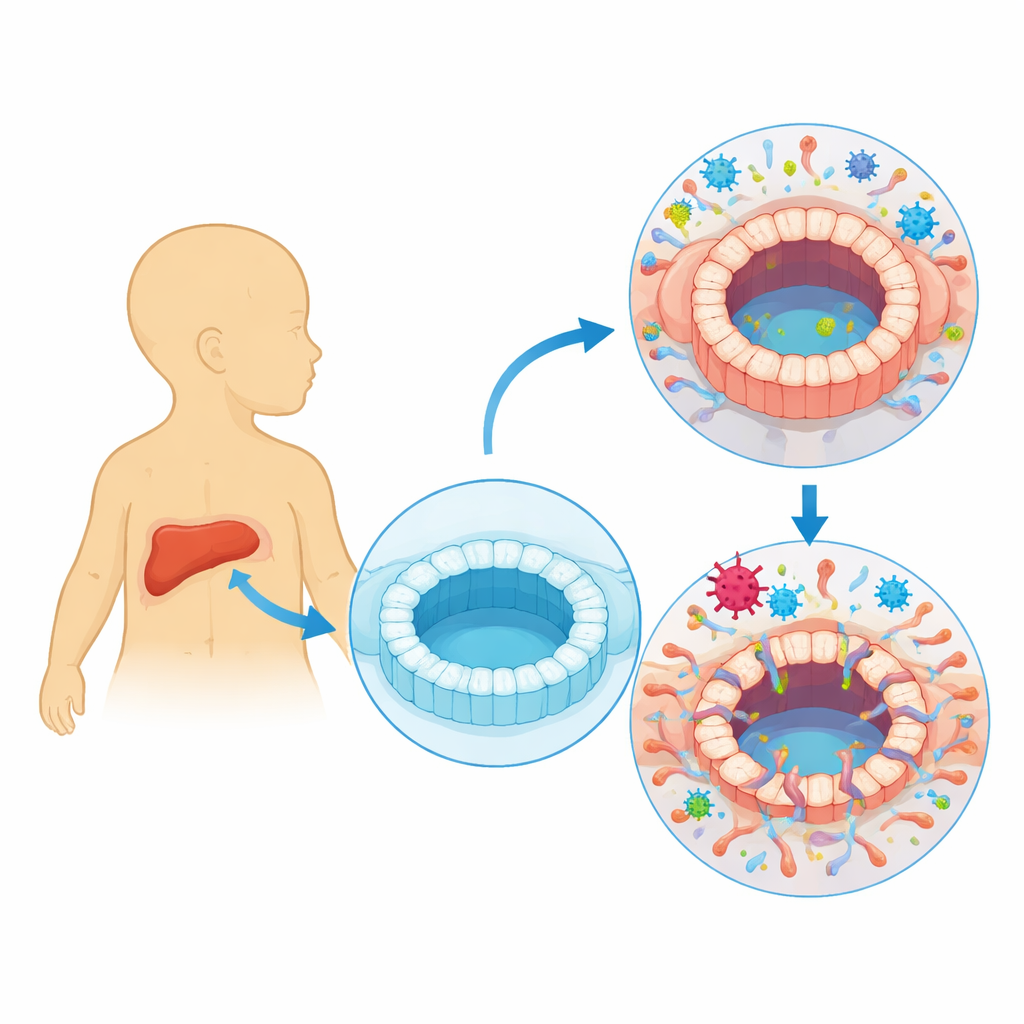
Una mirada más atenta a un virus común pero silencioso
El citomegalovirus humano (HCMV) suele permanecer en silencio en nuestros cuerpos, alternando entre una fase activa, en la que produce nuevas partículas virales, y una fase latente, en la que se oculta dentro de ciertos glóbulos sanguíneos. Los médicos llevan tiempo observando que personas con infección evidente por HCMV pueden desarrollar lesión de los conductos biliares y colestasis, una condición en la que la bilis no fluye correctamente. Muchos lactantes con atresia biliar, una afección en la que los conductos biliares se obstruyen y cicatrizan poco después del nacimiento, también muestran signos de infección reciente por HCMV. Sin embargo, no estaba claro si el virus infecta realmente las células que recubren los conductos biliares o si simplemente aparece como un acompañante durante la enfermedad.
Construir pequeños conductos biliares en una placa
Para responder a esto, los investigadores crearon “organoides” tridimensionales que imitan los conductos biliares humanos. Partieron de células madre pluripotentes inducidas, reprogramadas a partir de sangre humana, y las guiaron para que formaran células similares a colangiocitos, el tipo que recubre los conductos biliares. Estas células se autoorganizaron en esferas huecas con una cavidad central y conexiones célula–célula estrechas, semejantes a un conducto biliar en miniatura. El equipo expuso luego estos organoides a una cepa de HCMV marcada con un marcador fluorescente que se enciende cuando el virus está replicándose activamente. Esto les permitió rastrear las células infectadas y medir cómo cambiaban los organoides con el tiempo.
Cómo la infección deforma la estructura y debilita la barrera
Una vez infectados, los organoides dejaron de crecer con normalidad y se deformaron, con paredes engrosadas e irregulares. Algunas células brillaban intensamente, mostrando actividad viral completa y producción de nuevas partículas; otras contenían material genético viral en niveles más bajos, lo que sugiere un estado más latente. Pruebas funcionales revelaron que los organoides infectados perdieron funciones clave de los conductos biliares. Ya no se hinchaban correctamente en respuesta a un estímulo dependiente de canales de transporte de iones, y presentaban mayor permeabilidad en un ensayo de resistencia eléctrica que mide la hermeticidad de la barrera. Proteínas que normalmente sellan los espacios entre las células, como componentes de las uniones estrechas, se encontraban reducidas, y el transporte de un tinte de prueba hacia dentro y fuera de la cavidad interna se volvió anómalo. En conjunto, estos cambios muestran que el HCMV puede comprometer directamente la pared del conducto biliar, haciéndola permeable y disfuncional.
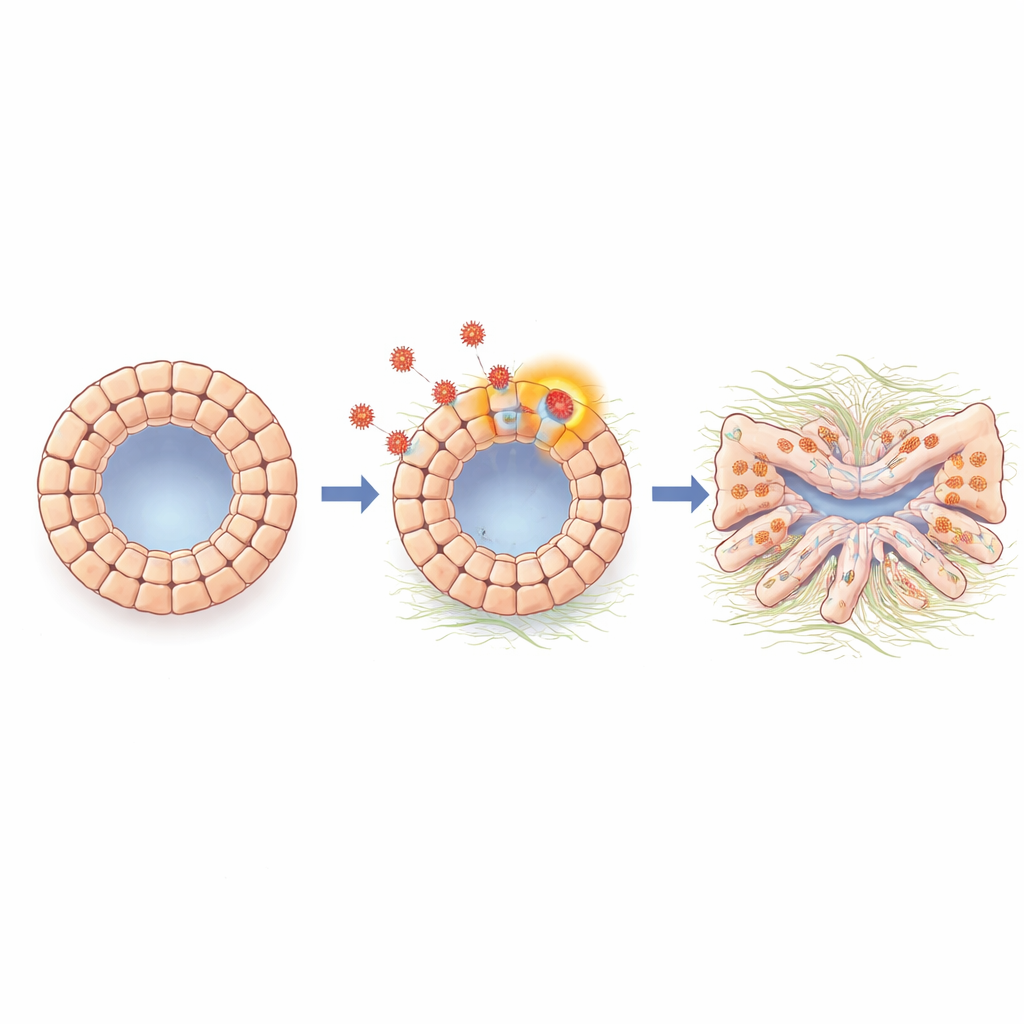
Las células cambian su identidad hacia un estado fibrótico
Profundizando más, los científicos analizaron la actividad génica en los organoides tanto a nivel global como a nivel de célula individual. Encontraron una fuerte activación de un programa parecido a la transición epitelio–mesénquima, un proceso en el que las células superficiales estrechamente conectadas aflojan sus uniones, adoptan un carácter más móvil y fibrótico, y comienzan a producir moléculas asociadas a la cicatrización del tejido. Los organoides infectados mostraron niveles aumentados de N-cadherina y otros marcadores vinculados a este cambio, así como genes implicados en fibrosis y producción de matriz. Una molécula de señalización llamada TGF-beta, bien conocida por impulsar la cicatrización en muchos órganos, se incrementó durante la infección. Cuando el equipo bloqueó la señalización de TGF-beta con un inhibidor de pequeña molécula o con un anticuerpo, los organoides recuperaron una forma más normal y muchos de los genes relacionados con la fibrosis y la transición volvieron cerca de los niveles basales, lo que indica que TGF-beta es un intermediario clave que conecta la presencia viral con los cambios celulares dañinos.
De los tubos cultivados en el laboratorio a niños enfermos
Para comprobar si estas observaciones de laboratorio se relacionan con la enfermedad real, los investigadores examinaron tejido hepático de niños con atresia biliar y de otras patologías hepáticas pediátricas. Usando sondas sensibles, detectaron ADN de HCMV en colangiocitos—las células de los conductos biliares—en aproximadamente dos tercios de las muestras de atresia biliar, pero con mucha menos frecuencia en hígados sin atresia biliar. En las mismas regiones donde se encontró ADN viral, las células de los conductos biliares mostraron niveles más altos de TGF-beta y N-cadherina, coincidiendo con el patrón de transición y cicatrización observado en los organoides. Esto sugiere que, al menos en un subconjunto de niños, el HCMV infecta directamente a las células del conducto biliar y las inclina hacia un estado fibrótico al activar vías impulsadas por TGF-beta.
Qué significa esto para entender y tratar las enfermedades de los conductos biliares
En términos sencillos, este trabajo muestra que un virus común puede invadir las células que recubren los conductos biliares, aflojar sus conexiones estrechas y empujarlas hacia una identidad más fibrosa y menos especializada mediante una señal basada en TGF-beta. Estos cambios debilitan las funciones de barrera y transporte de los conductos y pueden contribuir a la obstrucción y fibrosis observadas en enfermedades como la atresia biliar. Aunque no todos los casos de enfermedad de los conductos biliares estarán causados por HCMV, el estudio refuerza la idea de que, en lactantes vulnerables, la infección viral podría ser una pieza importante del rompecabezas, y que orientar vías relacionadas con TGF-beta podría algún día ayudar a proteger o restaurar conductos biliares frágiles.
Cita: Ye, Z., Hu, X., Rahaman, S.M. et al. HCMV infection disrupts barrier functions and promotes epithelial–mesenchymal transition in a cholangiocyte organoid model. Nat Commun 17, 2273 (2026). https://doi.org/10.1038/s41467-026-68962-8
Palabras clave: citomegalovirus, atresia biliar, organoides de conducto biliar, transición epitelial mesenquimal, señalización TGF-beta