Clear Sky Science · es
Comprender la promoción con metales alcalinos en la catálisis de hidrogenación mediante la interacción fuerte metal‑base
Por qué ajustar los catalizadores importa en la vida cotidiana
Transformar moléculas simples como el dióxido de carbono e hidrógeno en combustibles y productos químicos útiles es clave para una energía más limpia y una industria más verde. Muchos de los catalizadores metálicos que impulsan estas reacciones ya contienen pequeñas cantidades de metales alcalinos como sodio o potasio como “promotores”, pero su papel real ha sido sorprendentemente confuso. Este estudio revela un principio unificador sobre cómo actúan realmente estos aditivos, ofreciendo una vía para diseñar catalizadores más inteligentes que orienten las reacciones hacia los productos deseados y lejos del desperdicio.
Una mirada más cercana a los catalizadores potenciados
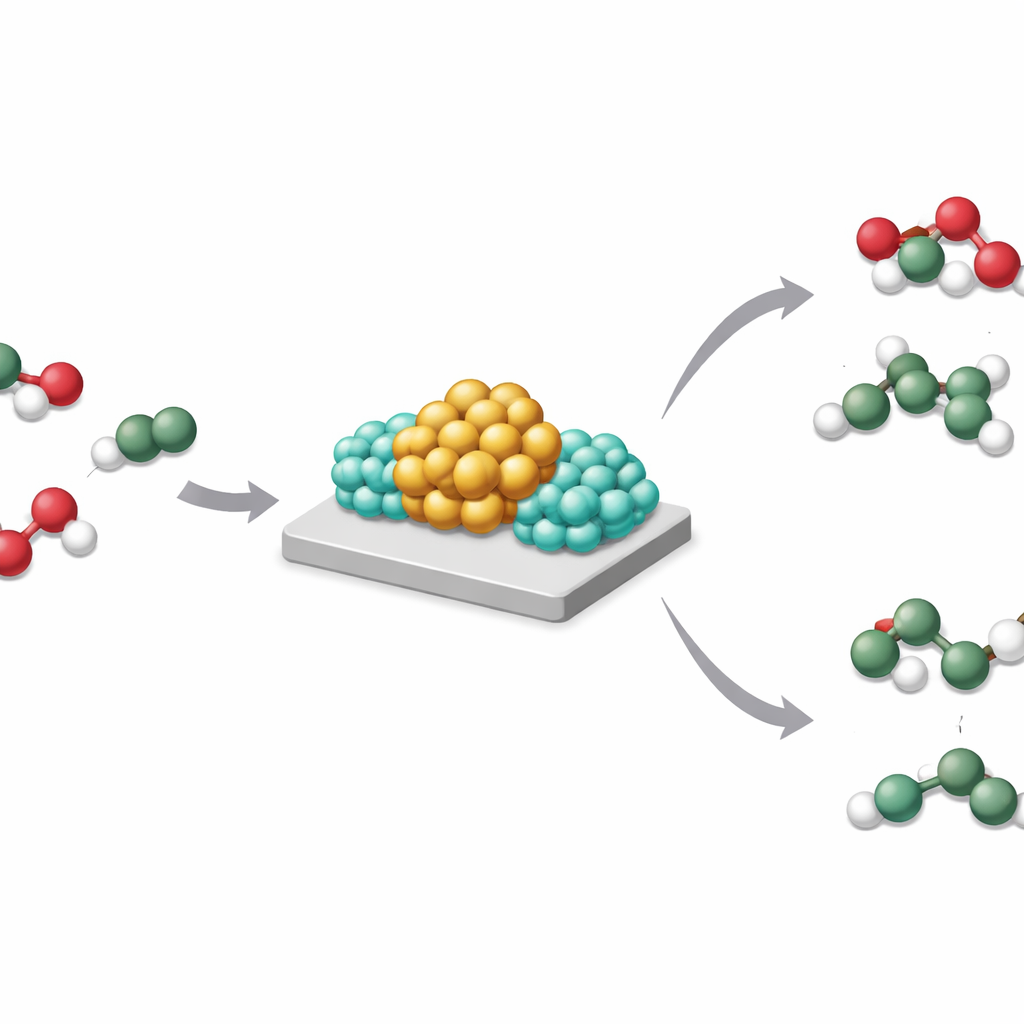
Los catalizadores formados por metales de transición como rodio y níquel se apoyan sobre soportes sólidos y ayudan a romper y reformar enlaces químicos. Durante décadas, la industria ha añadido metales alcalinos para hacer estos catalizadores más activos, más selectivos o más duraderos. Las explicaciones habituales se han centrado en efectos geométricos simples (cambio en la forma y tamaño de las partículas) o en la donación directa de electrones desde el metal alcalino al metal activo. Sin embargo, en condiciones reales de operación estos promotores existen principalmente como óxidos, no como átomos metálicos desnudos, lo que hace que la transferencia de electrones sea una imagen incompleta.
Descubriendo una asociación fuerte en la superficie
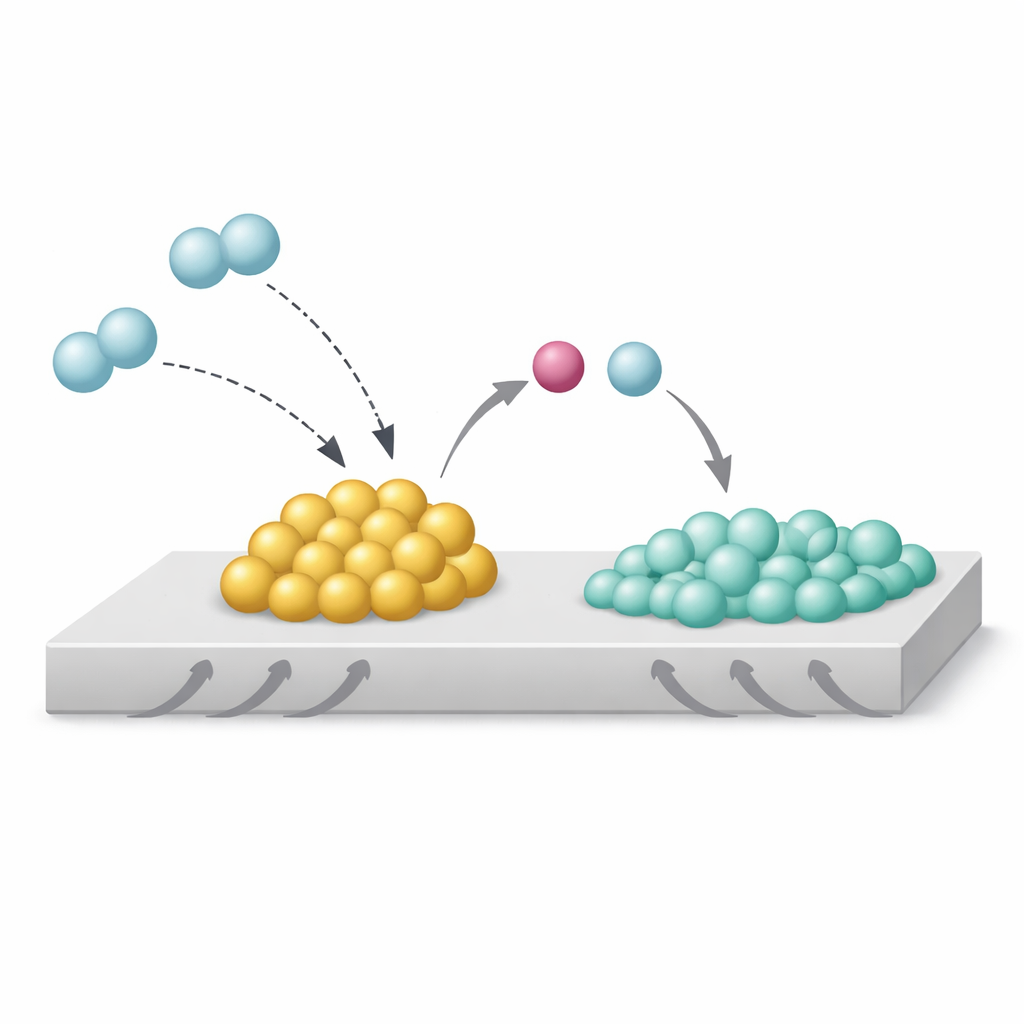
Los autores estudiaron un sistema modelo: nanopartículas de rodio sobre dióxido de titanio, con y sin sodio añadido. Usando microscopía electrónica avanzada, espectroscopía de rayos X y simulaciones por ordenador, encontraron que el sodio se localiza como óxido, Na2O, justo en el borde donde las partículas de rodio contactan el soporte. Bajo hidrógeno, esta disposición crea lo que llaman una Interacción Fuerte Metal‑Base, o SMBI. En estos puntos de contacto especiales, las moléculas de hidrógeno entrantes se rompen de forma heterolítica: la Na2O, más básica, captura la parte tipo protón, mientras que el rodio retiene la pareja rica en electrones. Esta escisión deja la superficie de rodio inusualmente rica en electrones y evita que el hidrógeno se extienda, o “desborde”, sobre el soporte de dióxido de titanio.
Cómo este efecto oculto dirige las reacciones
Esta sutil redistribución de dónde residen el hidrógeno y los electrones tiene grandes consecuencias. En la hidrogenación del dióxido de carbono, el rodio simple sobre dióxido de titanio favorece la hidrogenación intensa hasta metano. Cuando se añade sodio, ese mismo catalizador produce principalmente monóxido de carbono, un bloque de construcción valioso, mientras genera mucho menos metano. Se observa un comportamiento similar con litio o potasio, o cuando se cambia rodio por níquel. Los autores muestran que cuando el hidrógeno puede desbordarse libremente al soporte, domina la hidrogenación profunda; cuando la SMBI mantiene el hidrógeno concentrado en la frontera metal‑base y lejos del soporte, se favorecen productos más leves.
Dobles enlaces diferentes, resultados distintos
El equipo investigó luego cómo la SMBI afecta reacciones comunes de hidrogenación orgánica que implican dobles enlaces carbono‑carbono, carbono‑oxígeno y nitrógeno‑oxígeno. Para un doble enlace carbono‑carbono en acetato de vinilo, la promoción con sodio acelera el catalizador, probablemente porque el rodio rico en electrones ayuda a debilitar ese enlace mientras que el hidrógeno, más débilmente ligado, se adiciona de forma eficiente. En contraste, para moléculas como acetofenona y nitrobenceno, cuyos grupos reactivos prefieren adsorberse en el soporte de óxido, la misma adición de sodio ralentiza la reacción. Aquí, el suprimido desbordamiento de hidrógeno significa que el soporte ya no recibe suficiente hidrógeno para impulsar esas transformaciones, revelando que no todos los dobles enlaces se benefician por igual del mismo efecto promotor.
Diseñar catalizadores con control intencionado
Combinando experimentos y teoría, los autores sostienen que la SMBI proporciona una forma unificada de entender cómo los promotores de metales alcalinos remodelan las superficies catalíticas. En lugar de actuar como simples donantes de electrones, los óxidos alcalinos funcionan como fuertes atrapadores de protones, forzando que el hidrógeno se divida de manera polarizada y confinando el hidrógeno reactivo cerca de la interfaz metal‑base. Esta idea explica tendencias desconcertantes en muchas reacciones de hidrogenación y en distintos metales, y apunta a una regla de diseño práctica: ajustando cuánto y dónde se sitúan los óxidos alcalinos alrededor de las partículas metálicas, los químicos pueden orientar deliberadamente las reacciones hacia productos específicos optimizando a la vez la actividad y la estabilidad para procesos químicos más limpios.
Cita: Jung, M., Dickieson, M.P., Chen, P. et al. Understanding alkali metal promotion in hydrogenation catalysis through Strong Metal–Base Interaction. Nat Commun 17, 2465 (2026). https://doi.org/10.1038/s41467-026-68952-w
Palabras clave: catálisis de hidrogenación, promotores de metales alcalinos, conversión de CO2, catalizadores heterogéneos, interfaces metal‑óxido