Clear Sky Science · es
Un inhibidor alostérico de la proteasa NS2B-NS3 del virus del Zika con eficacia oral en modelos murinos
Una nueva forma de burlar a un virus peligroso
El virus del Zika acaparó titulares internacionales hace una década cuando las infecciones en mujeres embarazadas se asociaron con bebés nacidos con cráneos anormalmente pequeños y daño cerebral. Sin embargo, hoy todavía no existe un fármaco aprobado para tratar o prevenir el Zika. Este estudio describe un prometedor compuesto en forma de pastilla que desactiva una enzima viral clave de una manera inesperada y protege a ratones de una infección grave por Zika, apuntando hacia un futuro medicamento que podría, algún día, proteger a las personas vulnerables, especialmente durante los brotes.
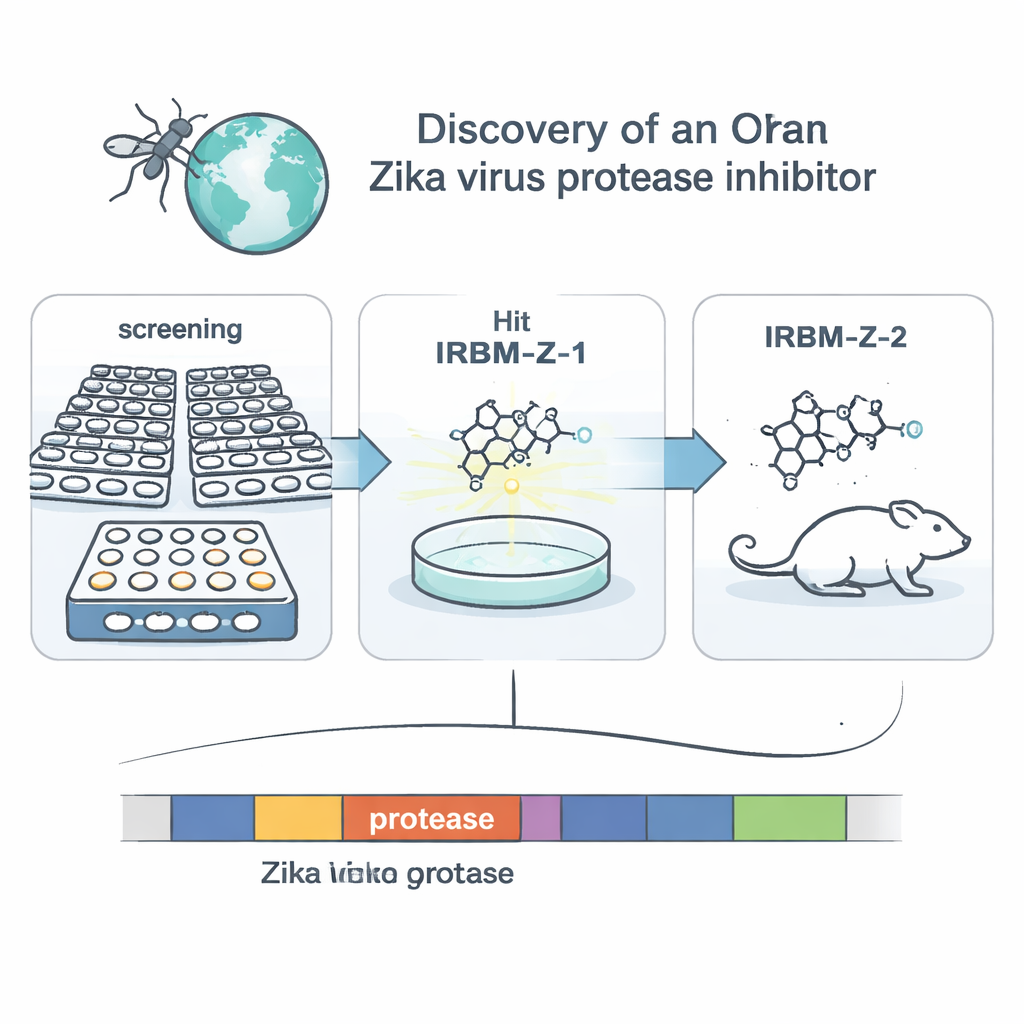
Por qué el Zika sigue importando
El virus del Zika se transmite principalmente por mosquitos Aedes y pertenece a la misma familia que los virus del dengue y del Nilo Occidental. La mayoría de las personas infectadas presentan poco o ningún malestar, pero alrededor de una de cada cinco desarrolla problemas que van desde fiebre y erupción cutánea hasta complicaciones graves como daño ocular, fallo orgánico y trastornos del sistema nervioso. El mayor peligro es para los fetos: la infección durante el embarazo puede causar microcefalia y discapacidad de por vida. Dado que no hay vacuna ni tratamiento antiviral aprobado, los médicos solo pueden ofrecer cuidados de soporte. Por ello, los científicos consideran al Zika una prioridad en la preparación ante pandemias, buscando fármacos que puedan emplearse tanto para proteger a poblaciones en riesgo como para contener nuevos brotes.
Buscando puntos débiles ocultos
Los investigadores se centraron en una enzima viral llamada proteasa NS2B–NS3. Estas “tijeras” moleculares cortan la gran proteína inicial del virus en las piezas necesarias para construir nuevos virus, lo que la convierte en un objetivo atractivo para fármacos. En lugar de diseñar un fármaco para el sitio evidente de corte, el equipo utilizó un sistema de cribado basado en células que imita la replicación del Zika dentro de células de riñón de mono. Construyeron un genoma de Zika modificado, o replicón, que carece de genes estructurales pero porta un reportero de luciferasa para que la emisión de luz refleje la copia viral. Cribando más de 120 000 pequeñas moléculas de una biblioteca química nacional, seleccionaron las que reducían con fuerza la señal luminosa sin dañar las células y luego generaron replicones virales que se volvieron resistentes a cada compuesto hit. Esta investigación genética señaló a la proteasa como el objetivo clave para una familia de compuestos, encabezada por una molécula inicial llamada IRBM-Z-1.
Bloqueando la enzima en la forma equivocada
Pruebas bioquímicas mostraron que IRBM-Z-1 no competía con el sustrato habitual en el sitio de corte. En cambio, se comportó como un inhibidor no competitivo, u alostérico: se une en un bolsillo separado e impide que la enzima adopte su conformación activa. La cristalografía de rayos X de alta resolución reveló que el compuesto se aloja en un bolsillo previamente desconocido, alejado del centro catalítico. Allí, su inusual núcleo “N-acilsidnona imina” forma una red de enlaces de hidrógeno e interacciones de apilamiento que empujan una región clave de la proteasa hacia una conformación abierta e inactiva. Un único cambio de aminoácido en esta región, en la posición 156, confiere resistencia al virus, subrayando cuánto explota el compuesto este sitio oculto. Este bolsillo también difiere de los sitios alostéricos descritos en flavivirus relacionados, ofreciendo un punto de apoyo genuinamente nuevo para el diseño de fármacos.
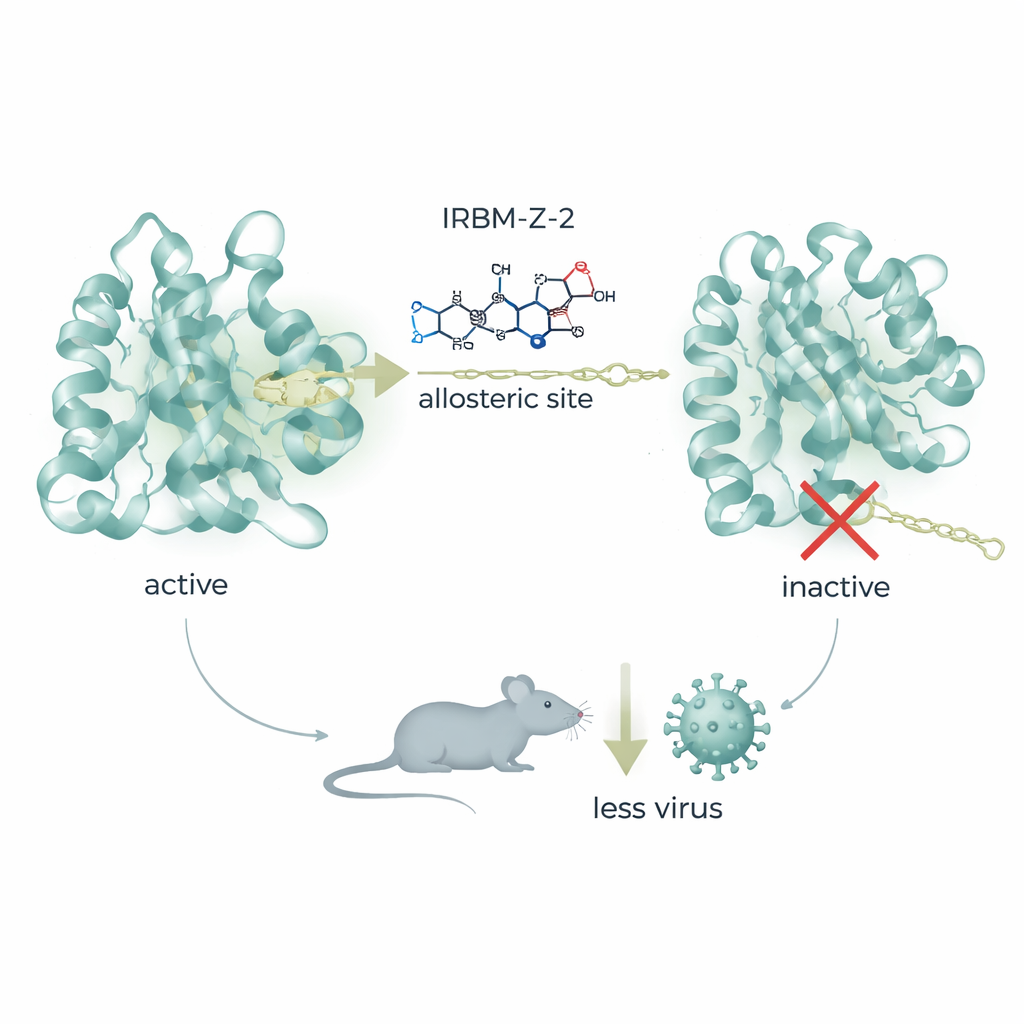
Del compuesto hit al fármaco protector en ratones
Guiado por conocimientos estructurales, el equipo refinó IRBM-Z-1 hasta obtener una molécula más potente denominada IRBM-Z-2. Este compuesto mejorado bloquea la proteasa del Zika a concentraciones nanomolares, inhibe con fuerza la replicación viral en varios tipos celulares y muestra actividad contra proteasas relacionadas del dengue y del Nilo Occidental, al tiempo que respeta las enzimas humanas. En estudios animales, IRBM-Z-2 mostró un comportamiento “con características de fármaco” favorable: fue estable en el organismo, presentó buena absorción oral y mantuvo niveles sanguíneos muy por encima de los necesarios para paralizar el virus, sin signos claros de toxicidad. En ratones AG129 altamente susceptibles infectados con Zika, el tratamiento diario—ya fuera por inyección o por vía oral—redujo drásticamente la cantidad de ARN viral en la sangre, previno la pérdida de peso y los síntomas de la enfermedad, y permitió que todos los animales tratados sobrevivieran, mientras que los controles no tratados sucumbieron a la infección.
Qué podría significar para futuros brotes
En conjunto, estos hallazgos introducen una nueva clase de antivirales contra el Zika que actúan congelando una enzima viral crítica en una pose inactiva en lugar de bloquear directamente su sitio activo. Debido a que IRBM-Z-2 puede administrarse por vía oral, muestra una protección sólida en modelos murinos rigurosos y, hasta ahora, presenta un perfil de seguridad limpio, destaca como un candidato prometedor para un desarrollo posterior como fármaco preventivo—potencialmente para proteger a mujeres embarazadas, trabajadores sanitarios y viajeros si el Zika resurge. Más ampliamente, el bolsillo alostérico recién descubierto podría inspirar fármacos similares contra virus emparentados, abriendo un nuevo frente en la lucha contra las enfermedades transmitidas por mosquitos.
Cita: Ontoria, J.M., Torrente, E., Missineo, A. et al. An allosteric inhibitor of the Zika virus NS2B-NS3 protease with oral efficacy in mouse models. Nat Commun 17, 1439 (2026). https://doi.org/10.1038/s41467-026-68943-x
Palabras clave: virus del Zika, fármaco antiviral, inhibidor de proteasa, modulación alostérica, enfermedad transmitida por mosquitos