Clear Sky Science · es
FCHo2, no talin, permite la activación inside-out de la integrina ɑvβ5 en adhesiones curvas
Cómo las células perciben la forma de su entorno
Nuestros cuerpos están formados por células que constantemente se agarran a su entorno, tirando y empujando para moverse, dividirse o mantenerse en su lugar. Este artículo revela que las células no solo detectan la rigidez del entorno: también leen su forma. Al descubrir un sistema adhesivo especial que se activa únicamente donde la membrana celular está fuertemente curvada, los autores muestran que las células usan diferentes “agarres” internos para superficies planas frente a entornos fibrosos, con importantes implicaciones para la formación de tejidos y la diseminación del cáncer.
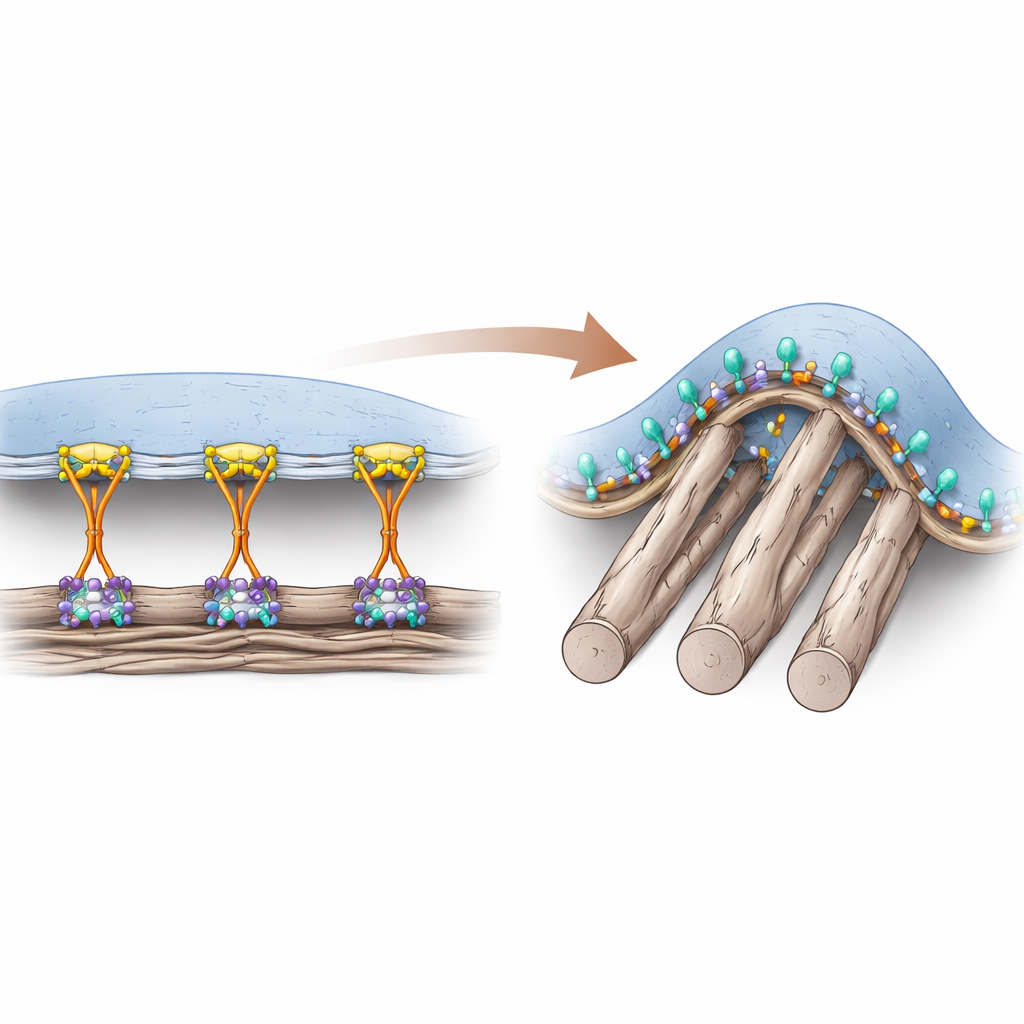
Dos maneras en que las células se sujetan
Las células se adhieren al material rico en proteínas que las rodea mediante receptores de superficie llamados integrinas. Durante años, los investigadores pensaron que una proteína auxiliar llamada talin era absolutamente esencial para activar las integrinas “desde dentro” de la célula, permitiendo una adhesión fuerte en sitios clásicos conocidos como adhesiones focales. Estas adhesiones se forman principalmente en superficies planas y rígidas y transmiten grandes fuerzas de tracción a través del citoesqueleto celular. Sin embargo, en tejidos vivos, muchas de las fibras circundantes son blandas y cilíndricas, creando puntos de contacto curvados que no soportan fácilmente estas estructuras sometidas a altas fuerzas. Los autores habían encontrado previamente un tipo distinto de estructura adhesiva, llamada adhesión curva, que aparece justo donde la membrana se pliega alrededor de fibras finas y que depende de una integrina específica, αvβ5.
Los agarres curvados utilizan un ayudante distinto
En el nuevo estudio, el equipo muestra que talin, aunque todavía está presente, no es el activador clave de la integrina αvβ5 en las adhesiones curvas. En su lugar, una proteína sensora de curvatura llamada FCHo2 se encarga de esta función. Usando barras y pilares nanoingenierizados para doblar la membrana celular de forma controlada, observaron que αvβ5 se agrupa fuertemente en regiones curvas, pero solo cuando FCHo2 puede unirse a una secuencia muy corta —un motivo HDRRE— justo en el interior de la célula, en la cola de la subunidad β5. Cuando este motivo se altera, la integrina sigue funcionando en adhesiones focales pero ya no puede formar adhesiones curvas. La supresión de FCHo2 deja las adhesiones focales clásicas en gran parte intactas pero elimina las adhesiones curvas, mientras que eliminar talin debilita severamente las adhesiones focales pero deja las adhesiones curvas mayormente sin afectar.
Un interruptor de un solo aminoácido como selector de forma
Un enigma fue por qué una integrina estrechamente relacionada, αvβ3, no puede formar adhesiones curvas aunque su cola interna se parezca mucho a la de β5. Intercambiando dominios entre las dos integrinas e introduciendo mutaciones puntuales, los autores identificaron una posición única cerca del sitio de unión a talin: la mayoría de las integrinas β tienen un triptófano (W), pero β5 tiene de forma única una tirosina (Y766). Cuando la tirosina de β5 se reemplazó por triptófano, la integrina perdió su capacidad para participar en adhesiones curvas y se comportó más como β3, favoreciendo solo las adhesiones focales. El cambio inverso —poner tirosina en el quimera tipo β3— restauró la sensibilidad a la curvatura. Experimentos adicionales con variantes que imitan estados fosforilados o no fosforilados de esta tirosina sugieren que la modificación química de ese residuo puede sesgar a la integrina hacia adhesiones focales planas y de alta fuerza o hacia adhesiones curvas de baja fuerza.
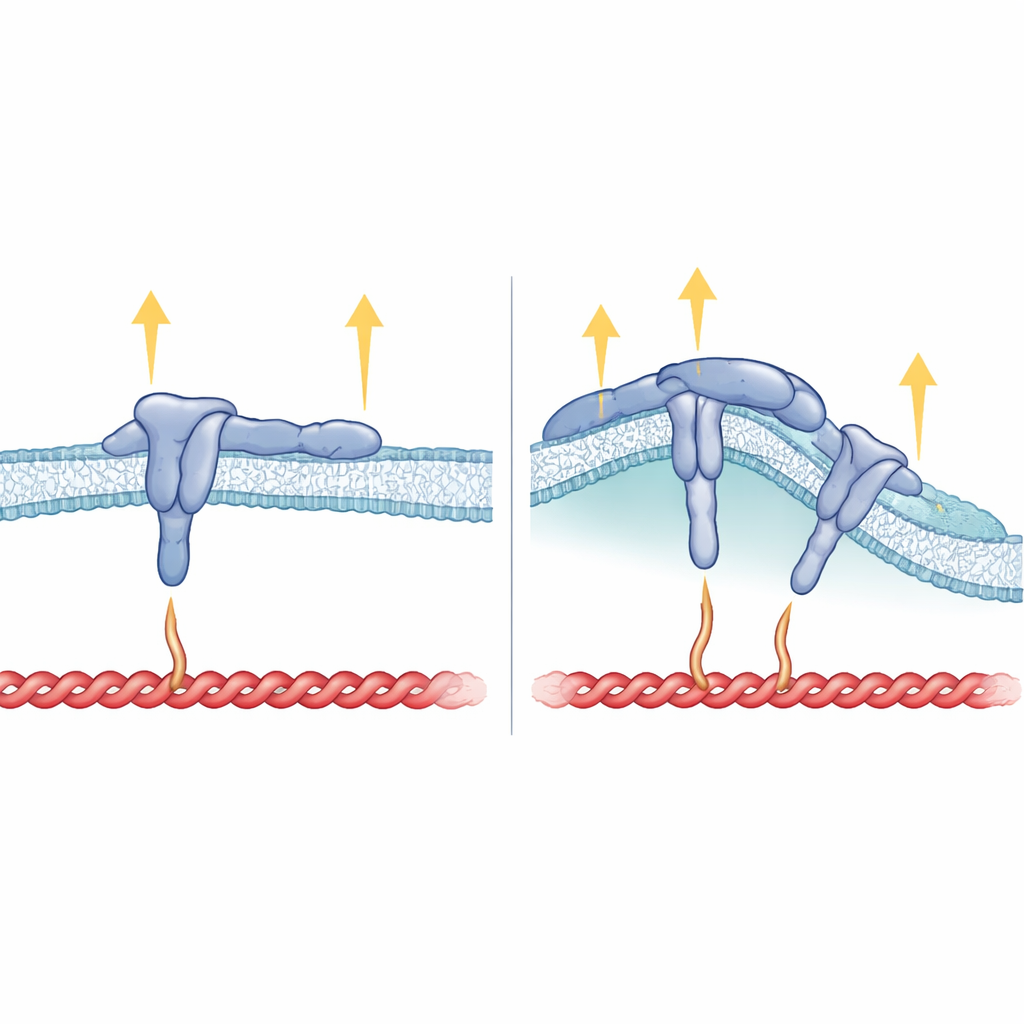
Cómo encajan la forma de la membrana, la estructura de la integrina y la fuerza
Más allá de la cola interna, la porción de β5 que atraviesa la membrana también resultó crítica. Cuando los investigadores reemplazaron el segmento transmembrana de β5 por el de β3, la integrina resultante aún podía formar adhesiones focales pero dejó de preferir sitios curvos y dejó de asociarse con FCHo2. Esto sugiere que la forma en que la integrina se sitúa en la membrana ayuda a orientar el motivo HDRRE para que FCHo2 pueda engancharse en regiones curvas y estabilizar la αvβ5 unida al ligando en su forma activa. En las adhesiones curvas, talin parece contactar solo una parte más alejada de la cola de la integrina y no soporta alta tensión, lo que explica por qué otros componentes dependientes de fuerza como vinculina, tensina y kindlin están en gran medida ausentes allí. En contraste, en las adhesiones focales, talin se acopla tanto a sitios cercanos como distantes de la cola y la membrana, soportando fuertes fuerzas de tracción pero impidiendo que FCHo2 acceda a la misma región.
Qué significa esto para el comportamiento celular
Para un observador no especialista, la conclusión de este trabajo es que las células disponen de dos “modos de agarre” separados para adherirse a su entorno. En áreas planas y rígidas usan adhesiones focales impulsadas por talin diseñadas para tirar con fuerza. En estructuras blandas, fibrosas y curvas cambian a adhesiones curvas impulsadas por FCHo2 que estabilizan la integrina αvβ5 con mucha menos fuerza. Un cambio diminuto en la secuencia de la integrina —y si ese sitio está químicamente modificado— ayuda a decidir qué modo se usa. Este sistema dual permite a las células interpretar tanto la rigidez como la forma en entornos tridimensionales, influyendo en cómo migran, organizan los tejidos y, potencialmente, cómo invaden durante la enfermedad.
Cita: Lu, CH., Lee, C.E., Zhang, W. et al. FCHo2, not talin, enables inside-out activation of integrin ɑvβ5 in curved adhesions. Nat Commun 17, 2419 (2026). https://doi.org/10.1038/s41467-026-68942-y
Palabras clave: integrinas, adhesión celular, curvatura de la membrana, FCHo2, citoesqueleto