Clear Sky Science · es
Un modelo polimérico informado experimentalmente revela la organización de alta resolución de loci genómicos
Cómo el plegamiento del ADN conforma la identidad celular
Cada célula de tu cuerpo porta esencialmente el mismo ADN, pero las neuronas, las células de la piel y las células madre se comportan de formas muy distintas. Una razón clave es cómo ese ADN se pliega y empaqueta dentro del núcleo. Este estudio presenta una nueva manera de «ver» ese plegamiento con un detalle notable, conectando la disposición física del ADN con si genes importantes están activados o silenciados. Al combinar experimentos con simulaciones por computadora basadas en la física, los autores revelan agrupamientos ocultos de material genético que parecen actuar como bloques básicos de la organización del genoma.
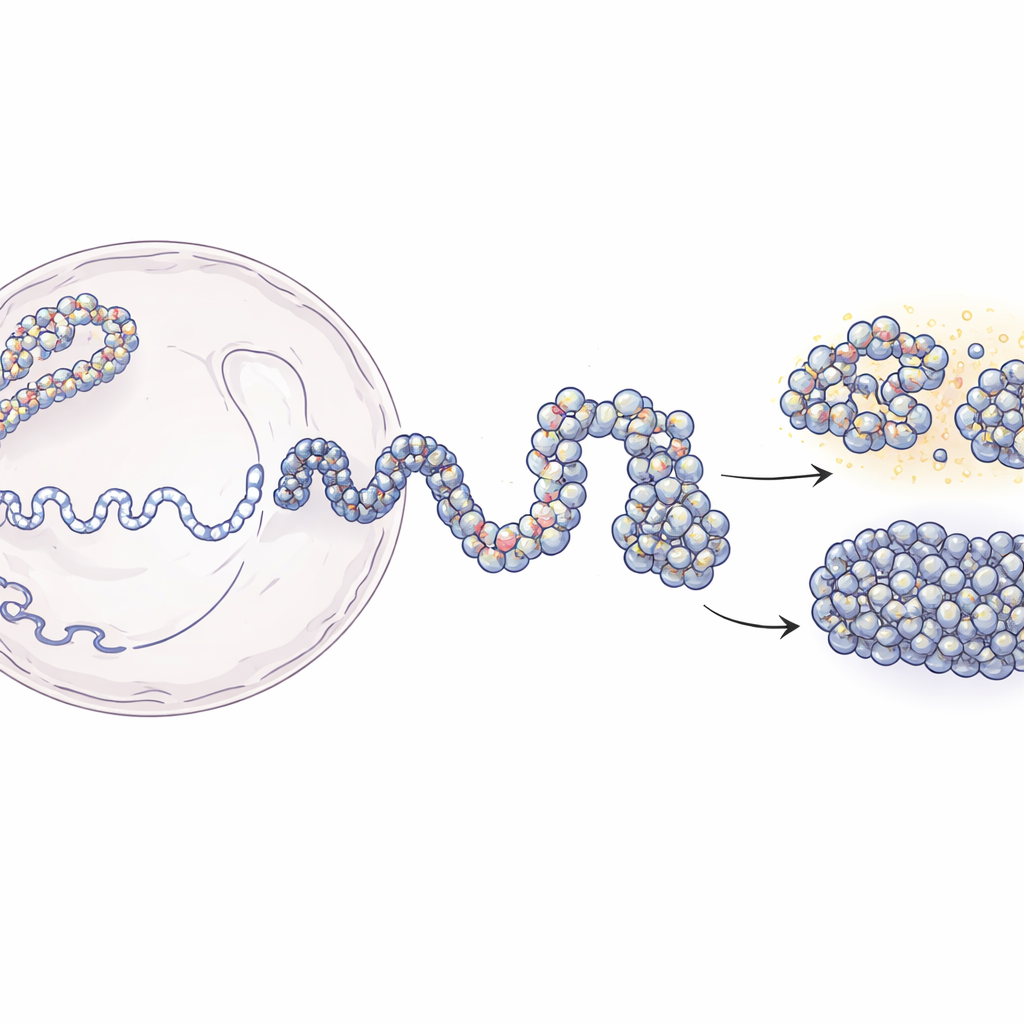
De largas hebras de ADN a mapas 3D del genoma
En el núcleo, el ADN se enrolla alrededor de carretes proteicos llamados nucleosomas, formando una estructura de cuentas en un hilo conocida como cromatina. Técnicas modernas como Hi-C y Micro-C pueden indicarnos qué fragmentos de ADN están próximos en 3D, pero por lo general ofrecen imágenes borrosas promediadas sobre poblaciones. Por otro lado, experimentos que localizan nucleosomas individuales aportan detalle local nítido pero poca idea de la estructura a mayor escala. Este trabajo salva esa brecha. Los autores parten de mapas de contactos de baja resolución que informan con qué frecuencia segmentos distantes de ADN se tocan, y los combinan con mapas experimentales de posiciones de nucleosomas. Aplicando principios de la física de polímeros, construyen conjuntos simulados 3D de cromatina que coinciden con los datos experimentales y, al mismo tiempo, resuelven estructuras hasta apenas unas decenas de letras de ADN.
Una estrategia en dos pasos para reconstruir la cromatina
El enfoque de modelado se desarrolla en dos etapas principales. Primero, el equipo usa datos de Hi-C para generar muchas formas posibles a gran escala de un tramo de ADN de 200 000 letras, tratando la cromatina como una cadena flexible en la que segmentos de 5 000 letras se guían suavemente para formar o evitar contactos como se observa en los experimentos. Estas estructuras gruesas capturan el patrón de plegamiento global que las proteínas en la célula contribuyen a crear. En la segunda etapa, cada gran partícula se reemplaza por una cadena mucho más fina compuesta por nucleosomas individuales y los cortos enlaces de ADN entre ellos. Las posiciones de esos nucleosomas proceden de un método de mapeo basado en enzimas (MNase-seq) que revela dónde suelen ubicarse a lo largo del genoma. A continuación, se permite que las cadenas de alta resolución se plieguen respetando la arquitectura más amplia. Cuando los investigadores "desenfocan" sus modelos de alta resolución hasta las resoluciones experimentales, reproducen con alta precisión tanto los mapas de contactos Hi-C como los de Micro-C.
Descubrimiento de «grumos» de nucleosomas como unidades estructurales
Al acercarse en sus estructuras simuladas, emergió un patrón llamativo: los nucleosomas no se disponían de forma uniforme, sino que se agrupaban en racimos irregulares, que los autores denominan grumos de nucleosomas. Estos grumos se parecen a las estructuras agrupadas observadas anteriormente en imágenes de microscopía de superresolución de células reales. Al analizar miles de instantáneas simuladas, el equipo mostró que estos grumos son elongados, no esféricos, y suelen contener varios nucleosomas compactados. De manera crucial, los contactos dentro de estos grumos se corresponden estrechamente con los bloques de interacción tipo dominio vistos en los datos experimentales, lo que indica que los grumos no son accidentes aleatorios sino unidades 3D fundamentales de la organización de la cromatina. Las simulaciones incluso predicen límites de dominio sutiles adicionales que son difíciles de detectar experimentalmente, lo que sugiere que este modelo físico puede descubrir características de pequeña escala ocultas en datos ruidosos.
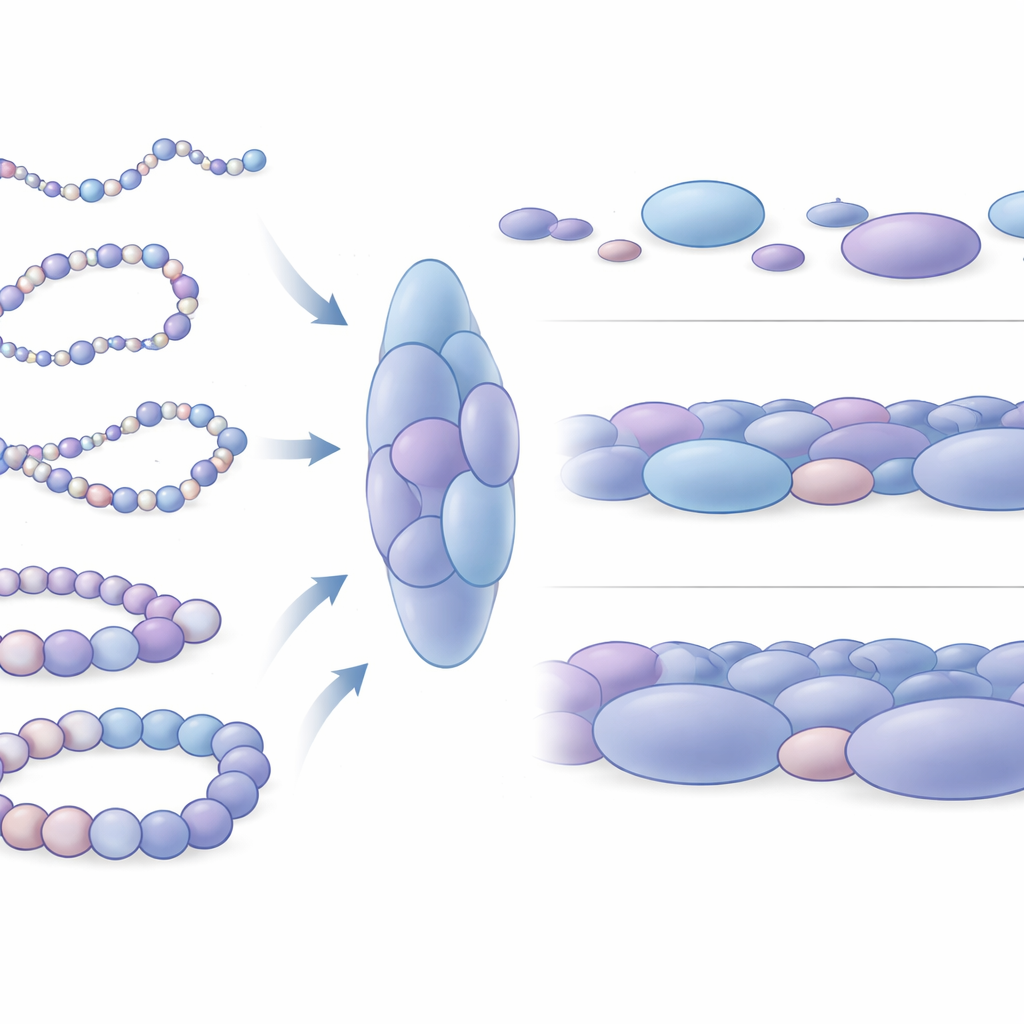
Cómo las diferencias de empaquetamiento reflejan la actividad génica
Los investigadores preguntaron luego cómo difieren estos grumos alrededor de genes activos frente a genes silenciosos. Se centraron en cuatro tramos bien estudiados de ADN humano, incluidos dos genes que ayudan a mantener las células madre en un estado flexible y no diferenciado (Nanog y Lin28A) y dos genes de control del desarrollo (HoxB4 y HoxA13) que están apagados en las mismas células. En torno a los genes inactivos, los grumos eran de media más grandes y más densamente empaquetados, con nucleosomas formando arreglos locales más cerrados. En contraste, los grumos cerca de genes activos eran más pequeños, algo más sueltos y más variados. A una escala mayor, el ADN alrededor de genes activos exploraba muchas más formas distintas y era mecánicamente más flexible, mientras que las regiones alrededor de genes silenciosos se comportaban como segmentos de cromatina más rígidos. Esta diferencia mecánica probablemente influye en la facilidad con la que elementos reguladores distantes pueden encontrarse y cooperar con los interruptores génicos.
Por qué esto importa para entender el control génico
En conjunto, los hallazgos dibujan un panorama en el que el genoma se construye a partir de agrupamientos dinámicos de nucleosomas cuya tamaño, forma y espaciamiento ayudan a determinar si los genes cercanos son accesibles o están bloqueados. El nuevo modelo conecta datos experimentales de contactos, mapas de nucleosomas y principios físicos en un único marco que explica cómo los genes de células madre pueden permanecer flexibles e interactivos mientras que los genes del desarrollo permanecen secuestrados en barrios más rígidos y compactos. Para el público general, la idea clave es que la actividad génica no está gobernada solo por la secuencia del ADN; también depende de cómo ese ADN se pliega en estructuras tridimensionales. Al revelar los grumos de nucleosomas como bloques básicos de ese plegamiento, este trabajo ofrece una vía potente para vincular la arquitectura microscópica del genoma con procesos a gran escala como el desarrollo, la identidad celular y la enfermedad.
Cita: Mittal, R., Heermann, D.W. & Bhattacherjee, A. An experimentally-informed polymer model reveals high resolution organization of genomic loci. Nat Commun 17, 2338 (2026). https://doi.org/10.1038/s41467-026-68928-w
Palabras clave: plegamiento de la cromatina, grupos de nucleosomas, organización 3D del genoma, regulación génica, modelado de polímeros