Clear Sky Science · es
Expansión clonal de células T CD8 citotóxicas en ARIA asociada a lecanemab
Por qué importa esto para las personas con Alzheimer
El lecanemab es uno de los primeros fármacos capaces de eliminar la amiloide del cerebro y ralentizar de forma modesta la pérdida de memoria en la enfermedad de Alzheimer. Pero algunos pacientes tratados con esta terapia desarrollan hinchazón cerebral o pequeños sangrados en el cerebro, cambios que se ven en las resonancias magnéticas y que se agrupan bajo el término anomalías de imagen relacionadas con la amiloide (ARIA). Este estudio plantea una pregunta crucial para pacientes y familias: ¿qué está ocurriendo en el sistema inmunitario cuando aparece ARIA, y podría algún día una simple analítica de sangre ayudar a predecir quién corre más riesgo?
La promesa y el riesgo de un nuevo tratamiento para el Alzheimer
El lecanemab es un anticuerpo administrado por infusión que se dirige a los agregados de una proteína llamada beta‑amiloide, una de las marcas de la enfermedad de Alzheimer. Al facilitar la eliminación de amiloide, puede ralentizar moderadamente el deterioro cognitivo. Sin embargo, este beneficio conlleva una preocupación de seguridad: algunas personas desarrollan ARIA, que puede incluir zonas de hinchazón cerebral o hemorragias puntiformes. Estos efectos secundarios requieren controles frecuentes por resonancia magnética y pueden limitar quién recibe el fármaco. No todos son igualmente vulnerables: los portadores de una variante genética llamada APOE4 tienen mayor riesgo, pero los genes por sí solos no explican por qué aparece ARIA, sobre todo al inicio del tratamiento. Dado que el lecanemab se administra por vía sanguínea, los autores razonaron que estudiar con detalle las células inmunitarias en sangre podría revelar señales de alarma tempranas o incluso mecanismos que vinculen el tratamiento con el daño vascular cerebral. 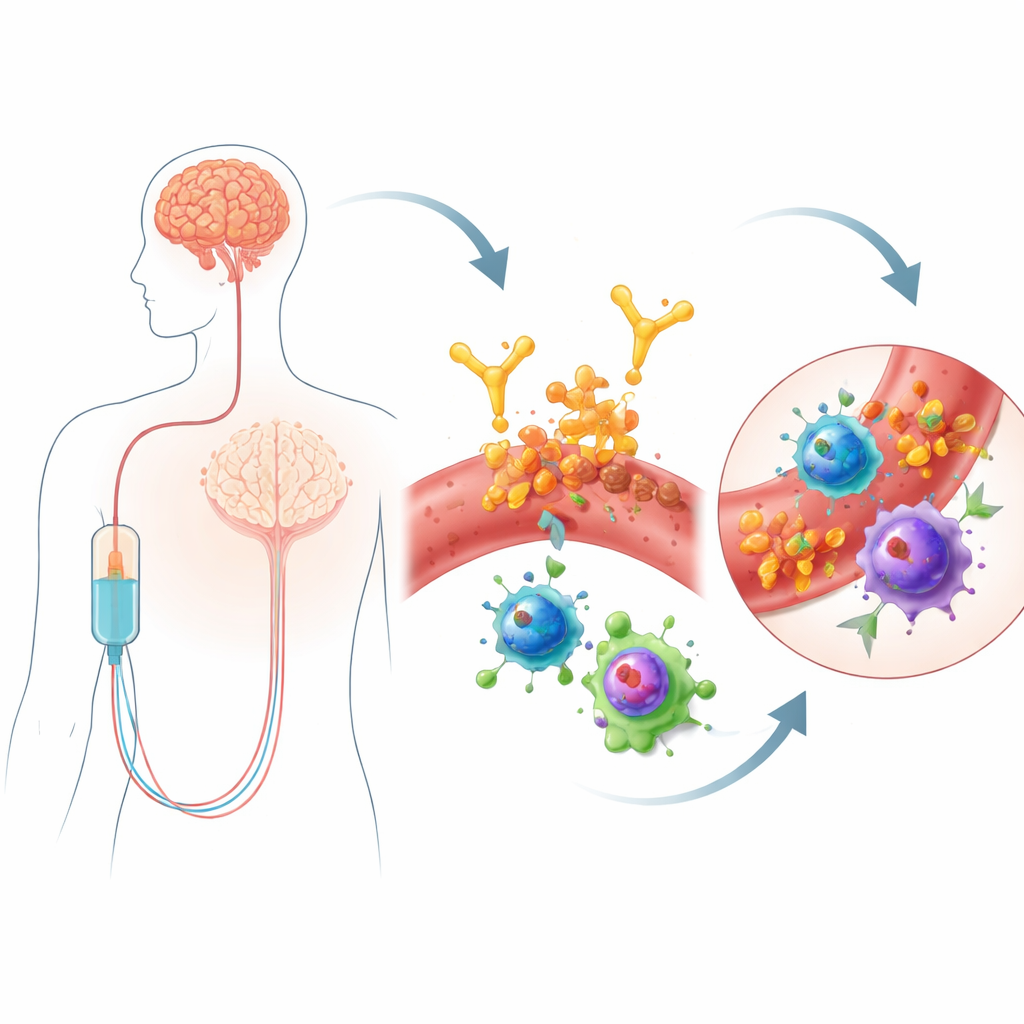
Rastreo de las células inmunitarias en pacientes que sí y que no desarrollaron ARIA
Los investigadores estudiaron a seis personas con Alzheimer que recibían lecanemab en una clínica regional de la memoria. Tres desarrollaron distintas formas de ARIA, y tres pacientes emparejados (similares en edad, sexo, genotipo APOE y número de infusiones) no lo hicieron. Se extrajo sangre justo antes de las infusiones, y el equipo empleó un enfoque intensivo "multiómico": secuenciación de ARN de célula única para leer qué genes estaban activados en miles de células inmunitarias individuales, etiquetas basadas en anticuerpos para definir tipos celulares, secuenciación de los receptores de células T para seguir clones, y metabolómica dirigida para medir cientos de pequeñas moléculas implicadas en el metabolismo celular. Esto les permitió no sólo preguntar qué tipos celulares estaban presentes, sino cuán activos eran, qué combustible utilizaban y si familias específicas de células T se estaban expandiendo en respuesta a algún estímulo.
Expansión de células T asesinas altamente armadas
Surgió un patrón claro en los pacientes que desarrollaron ARIA. En comparación con los controles, tenían una proporción mayor de células T CD8 "asesinas" y menos células T CD4 auxiliares. Dentro del grupo CD8, destacaron dos subgrupos: células de memoria efectora y una forma terminalmente diferenciada conocida como células TEMRA. Estas células TEMRA son como soldados veteranos—altamente especializadas para el ataque, con un fuerte aparato para matar células diana. En los pacientes con ARIA, las TEMRA eran más numerosas, mostraban mayor expansión clonal (es decir, familias concretas de células T se habían multiplicado) y presentaban programas génicos asociados con citotoxicidad, migración a través de vasos sanguíneos y señales de estimulación crónica. Estados similares de células T se han observado en el envejecimiento, infecciones crónicas, esclerosis múltiple y en el líquido cefalorraquídeo de personas con Alzheimer, donde pueden acumularse cerca de vasos sanguíneos y de la superficie cerebral.
Reprogramación metabólica y comunicación con otras células inmunitarias
El equipo también encontró que estas células efectoras CD8 habían reprogramado su metabolismo. En lugar de depender principalmente de la producción eficiente de energía en las mitocondrias, cambiaron hacia la glucólisis, una vía más rápida pero menos eficiente para generar energía que sostiene actividades intensas y de corta duración. Las mediciones de metabolitos en las células sanguíneas corroboraron esto: los niveles de lactato y piruvato aumentaron, mientras que componentes clave del ciclo del ácido cítrico disminuyeron, un patrón típico de células inmunitarias inflamatorias. Los monocitos, otro tipo de glóbulo blanco, mostraron cambios complementarios. En los pacientes con ARIA, los monocitos activaron genes para la presentación de antígenos, la adhesión a otras células y la producción de quimiocinas—señales químicas que atraen a las células T. El modelado computacional de pares ligando‑receptor sugirió que los monocitos estaban enviando señales de activación y de homing más fuertes a las células efectoras CD8, creando un entorno que fomenta que estas células asesinas interactúen con las paredes de los vasos sanguíneos.
Códigos de dirección que orientan a las células T hacia los vasos cerebrales
Puesto que este estudio sólo muestreó sangre, los autores recurrieron a un conjunto de datos independiente de célula única procedente de cerebros de pacientes tratados con lecanemab para preguntar si los mismos programas de células T se vinculaban a nichos vasculares en el cerebro. Cuando proyectaron sus subconjuntos CD8 sobre este mapa cerebral, las células TEMRA y las de memoria efectora de los pacientes con ARIA mostraron "códigos de dirección" transcripcionales—combinaciones de moléculas de adhesión y receptores de quimiocinas—que coincidían con células endoteliales (vasos sanguíneos) en el cerebro enfermo. Estas firmas sugieren que las células T asesinas expandidas no sólo están altamente armadas y metabólicamente activadas, sino también predispuestas a dirigirse e interactuar con vasos sanguíneos cerebrales estresados en los sitios de eliminación de amiloide. 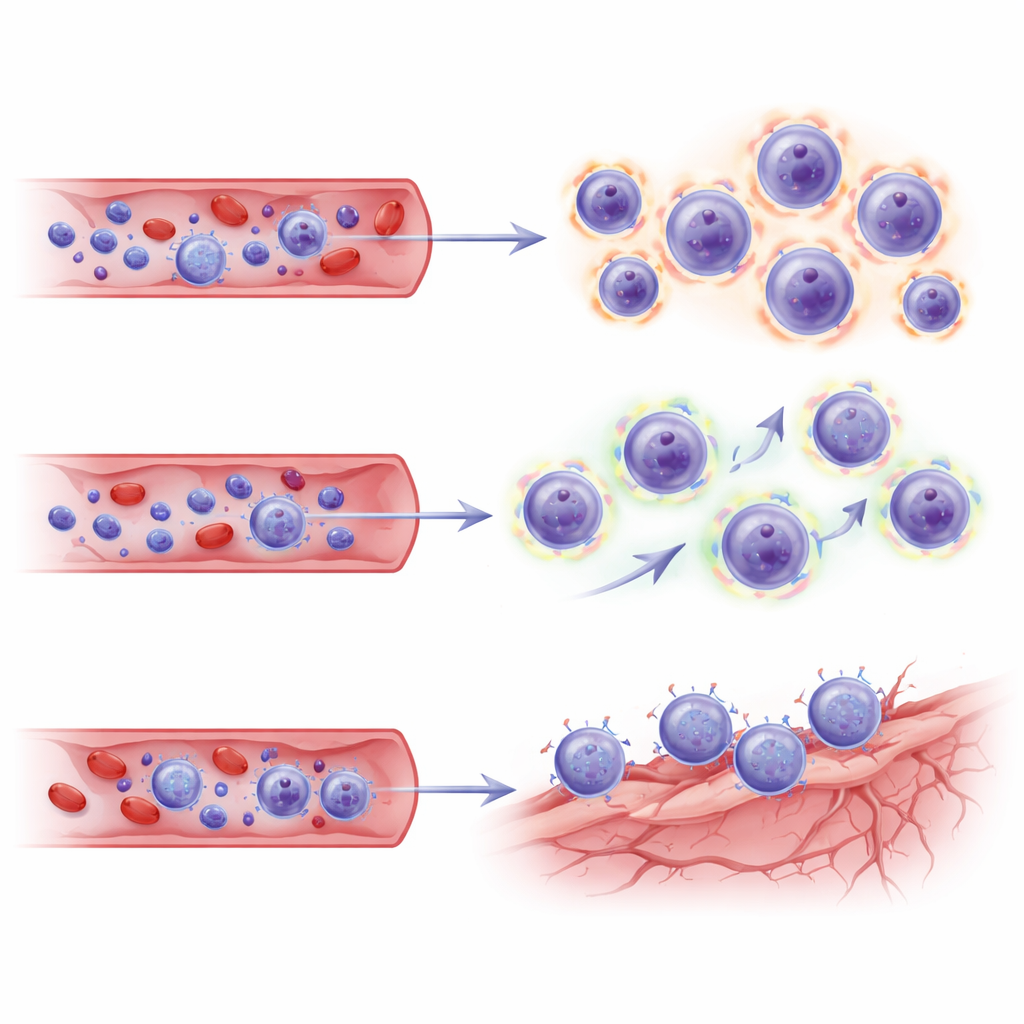
Qué podría significar esto para pacientes y cuidados futuros
En conjunto, este estudio pequeño pero detallado describe ARIA como algo más que un efecto secundario pasivo de la eliminación de amiloide. En cambio, parece vinculado a una respuesta inmunitaria coordinada en la sangre: expansión y activación metabólica de clones específicos de células T asesinas, un refuerzo de las señales provenientes de monocitos y rasgos moleculares que favorecen la interacción con los vasos sanguíneos cerebrales. El trabajo no prueba que estas células causen ARIA—los cambios inmunitarios podrían ser una reacción al daño vascular en lugar de su origen—pero ofrece hipótesis comprobables y un plan para biomarcadores basados en sangre. En el futuro, medir la abundancia y el estado metabólico de las células T CD8 TEMRA, junto con moléculas señalizadoras clave, podría ayudar a identificar a los pacientes con mayor riesgo de ARIA, orientar los programas de seguimiento o incluso inspirar estrategias dirigidas para atenuar temporalmente esta respuesta inmunitaria sin perder los beneficios de las terapias que eliminan la amiloide.
Cita: Johnson, L.A., Saito, K., Pallerla, A.V. et al. Clonal expansion of cytotoxic CD8⁺ T cells in lecanemab-associated ARIA. Nat Commun 17, 2180 (2026). https://doi.org/10.1038/s41467-026-68921-3
Palabras clave: Enfermedad de Alzheimer, lecanemab, células inmunitarias, vasos sanguíneos cerebrales, efectos secundarios del tratamiento