Clear Sky Science · es
Las proteínas TMEM63 actúan como escramblasas lipídicas activadas mecánicamente y moduladas por colesterol que contribuyen a la mecano-resiliencia de la membrana
Cómo las células se mantienen íntegras bajo esfuerzo físico
Las células de nuestro organismo están constantemente comprimidas, estiradas y sacudidas, ya sea en corazones que laten, músculos en actividad o tumores que empujan tejidos. Este estudio revela cómo una familia de proteínas de membrana, llamadas OSCA/TMEM63, ayuda a las células a sobrevivir a tales fuerzas mecánicas al reorganizar las grasas de su capa externa. Entender este sistema amortiguador incorporado podría aportar nuevas perspectivas sobre trastornos de la audición, la mielinización nerviosa e incluso la diseminación del cáncer.
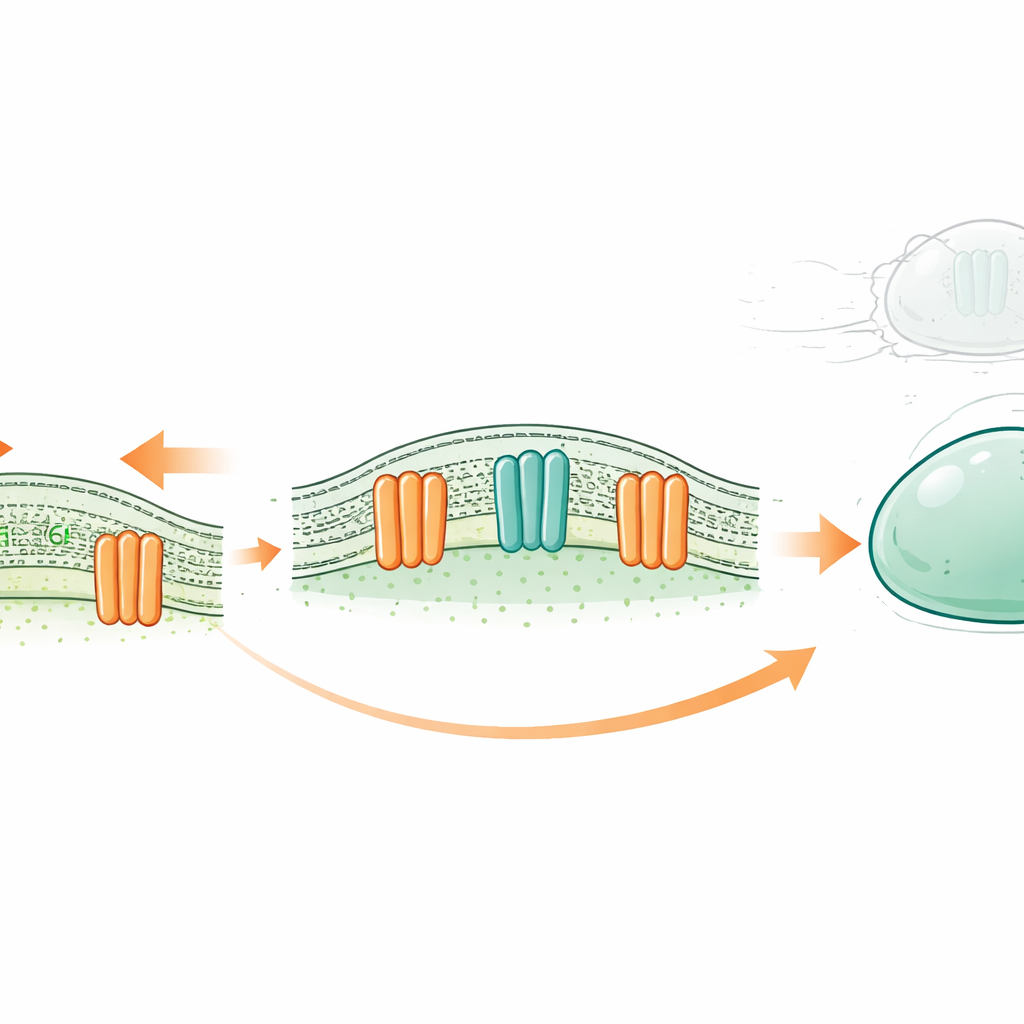
Un nuevo tipo de amortiguador celular
Cada célula está envuelta por una delgada membrana oleosa formada por dos capas de moléculas parecidas a grasas llamadas lípidos. Tradicionalmente, se pensaba que ciertas proteínas de membrana actuaban solo como canales iónicos—pequeñas válvulas que permiten el paso de partículas cargadas en respuesta a estímulos como el estiramiento. Se sabe que la familia OSCA/TMEM63, presente desde plantas hasta humanos, se abre en respuesta a la tensión de la membrana. Trabajos estructurales previos insinuaron que, a diferencia de los canales iónicos clásicos, sus poros están parcialmente recubiertos por lípidos. Esto planteó una posibilidad provocadora: ¿podrían estos canales también funcionar como “escramblasas”, volteando lípidos entre las capas interna y externa de la membrana cuando la célula está sometida a fuerza?
Observando cómo los lípidos cruzan la membrana
Para probar esta idea, los autores combinaron simulaciones por ordenador con sistemas reduccionistas de laboratorio construidos a partir de componentes purificados. En las simulaciones, versiones abiertas de varias proteínas OSCA y TMEM63 se insertaron en membranas modelo. Moléculas lipídicas se movieron espontáneamente a través de una ranura en estas proteínas de un lado de la bicapa al otro, formando un cinturón que conectaba las dos hojas mientras dejaba un camino lleno de agua para los iones. En experimentos paralelos, el equipo construyó “burbujas” artificiales gigantes (vesículas) que contenían lípidos fluorescentes y proteínas concretas. Cuando un agente externo apagara la fluorescencia en la superficie externa, cualquier caída adicional de la señal solo podía explicarse por lípidos que giraban desde la capa interior hacia el exterior. Las vesículas que contenían OSCA1.1, OSCA1.2, OSCA2.2 o TMEM63A/B mostraron esa pérdida adicional de fluorescencia, lo que indica escrambling activo, mientras que canales de control que no escramblean lípidos no lo hicieron.
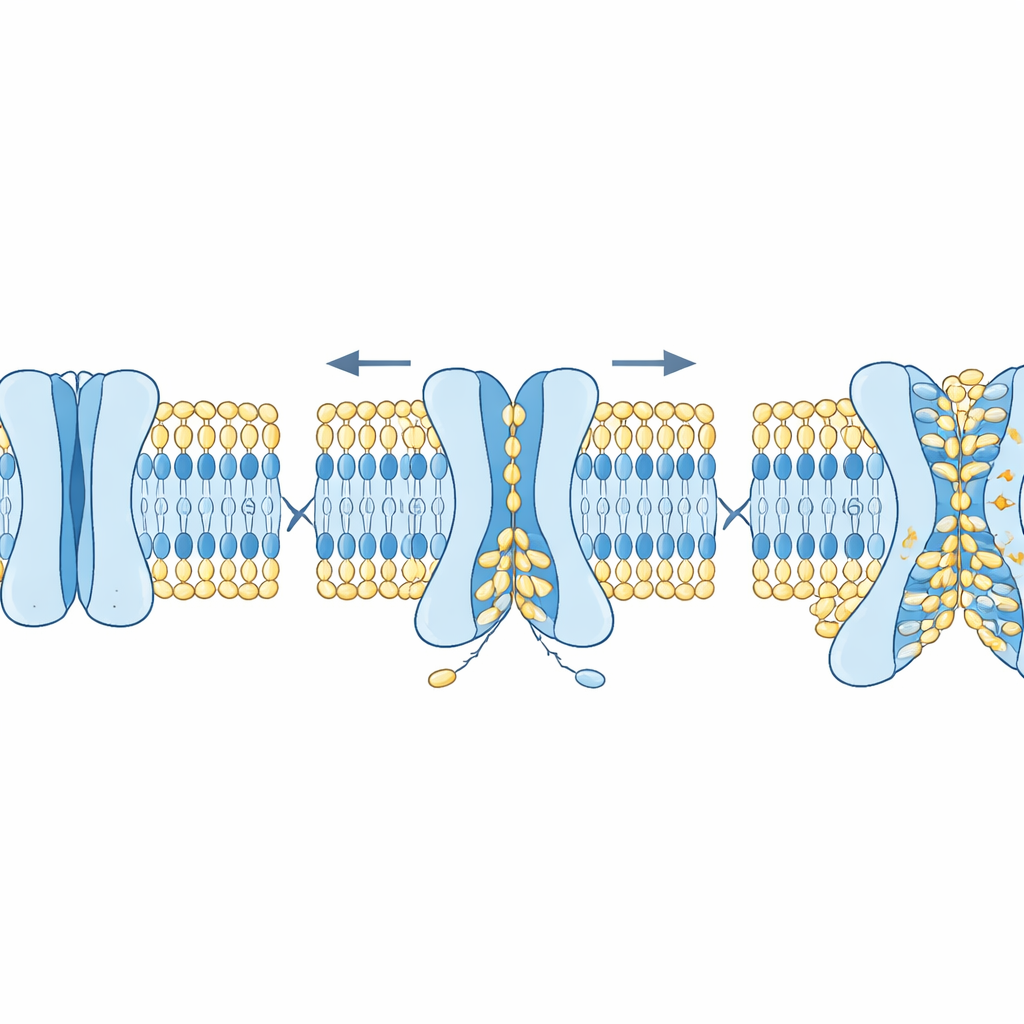
Cómo la estructura y el colesterol afinan el proceso
Los investigadores preguntaron luego qué rasgos de las proteínas TMEM63 controlan este comportamiento dual. Usando AlphaFold2, generaron muchas formas plausibles de las proteínas humanas TMEM63, que iban desde cerradas hasta progresivamente abiertas. Las simulaciones revelaron que un puñado de aminoácidos voluminosos actúa como “cuellos de botella” en la ranura. Un residuo limita principalmente el flujo iónico, mientras que otros bloquean el movimiento lipídico. Mutar el cuello de botella iónico aumentó la conductancia eléctrica sin cambiar mucho el escrambling de lípidos, mientras que mutar la compuerta lipídica hizo que los lípidos se voltearan con mayor facilidad e incluso provocó que las células mostraran señales de “cómeme” en su superficie sin ningún estímulo adicional. Otro regulador clave fue el colesterol, un componente que rigidiza las membranas celulares. Añadir colesterol a membranas modelo ralentizó notablemente el escrambling de lípidos y estabilizó el estado cerrado de TMEM63A, tanto en simulaciones como en estructuras por crio‑microscopía electrónica donde el colesterol se alojaba en sitios específicos de la proteína.
La fuerza mecánica como interruptor
Si el colesterol mantiene el escrambling bajo control dentro de las células, ¿qué lo activa en el momento oportuno? El equipo usó moléculas azucaradas en forma de anillo llamadas ciclodextrinas para extraer selectivamente lípidos de las membranas y así aumentar la tensión sin eliminar el colesterol. En vesículas de tamaño celular, la adición de ciclodextrina activó el escrambling lipídico por TMEM63A solo cuando la proteína estaba presente, demostrando que el estrés mecánico por sí solo puede desencadenar el volteo. En células vivas, enfoques similares mostraron que la eliminación leve de colesterol por sí sola no era suficiente; se requería un reto mecánico posterior para observar un escrambling fuerte. Cuando células diseñadas para expresar TMEM63A fueron estiradas repetidamente, expusieron rápidamente ciertos lípidos en su superficie externa, un sello distintivo del escrambling, mientras que las células carentes de estas proteínas mostraron mucho menos cambio.
Protegiendo a las células de la rotura
Más allá de voltear lípidos, el escrambling activado mecánicamente modificó el comportamiento físico de las membranas bajo estrés extremo. En vesículas artificiales expuestas a alta fuerza, las que carecían de escramblasas tendían a romperse, mientras que las vesículas que contenían TMEM63A o una escramblasa conocida se encogían, formaban túbulos finos y en gran medida permanecían intactas. En una línea celular de cáncer cerebral humano que expresa de forma natural TMEM63A y TMEM63B, reducir los niveles de cualquiera de las dos proteínas aumentó la probabilidad de que las células se rompieran cuando se las sometió a estrés mecánico intenso. En conjunto, estos hallazgos respaldan un modelo en el que las proteínas OSCA/TMEM63 actúan como válvulas que se abren bajo tensión y difuminan temporalmente la diferencia habitual entre las caras interna y externa de la membrana. Al permitir que los lípidos se redistribuyan rápidamente, ayudan a igualar el estrés y a prevenir desgarros catastróficos.
Qué significa esto para la salud y la enfermedad
En términos sencillos, este trabajo demuestra que algunos canales sensibles al estiramiento hacen más que conducir señales eléctricas: también reorganizan la piel externa de la célula para ayudarla a sobrevivir al apretón. Las proteínas TMEM63 emergen como escramblasas lipídicas activadas mecánicamente cuya actividad está finamente modulada por la composición de la membrana, en particular por el colesterol. Este mecanismo de mecano‑resiliencia puede ser importante allí donde las células se exponen a grandes fuerzas, desde las fibras nerviosas aislantes y las células sensoras del oído hasta las células cancerosas que navegan por tejidos densos. Comprender y, eventualmente, manipular esta función dual de canal iónico‑escramblasa podría abrir nuevas vías para proteger tejidos vulnerables—o, por el contrario, para hacer que células cancerosas difíciles de eliminar sean más frágiles.
Cita: Lin, Y., Zhou, Z., Han, Y. et al. TMEM63 proteins act as mechanically activated cholesterol modulated lipid scramblases contributing to membrane mechano-resilience. Nat Commun 17, 2717 (2026). https://doi.org/10.1038/s41467-026-68919-x
Palabras clave: canales iónicos mecanosensibles, escrambling de lípidos, mecánica de la membrana celular, regulación por colesterol, proteínas TMEM63 OSCA