Clear Sky Science · es
Un péptido críptico neurotóxico derivado del empalme críptico dependiente de TDP-43 de PKN1
Amenazas ocultas dentro de las células cerebrales
Muchas enfermedades cerebrales, incluida la esclerosis lateral amiotrófica (ELA) y la enfermedad de Alzheimer, implican agregados de una proteína llamada TDP-43. Los científicos saben que cuando esta proteína deja de funcionar correctamente, las neuronas pierden mensajes vitales y acaban muriendo. Este estudio revela un giro más sorprendente: la falla de TDP-43 también puede hacer que las células cerebrales fabriquen una mini‑proteína hasta ahora desconocida y tóxica, que a su vez daña los circuitos de la memoria. Comprender a este actor oculto podría abrir nuevas vías para el diagnóstico y el tratamiento de demencias devastadoras.
Cómo un corrector celular mantiene el ARN en orden
Dentro de las neuronas, TDP-43 actúa como un corrector del ARN, los mensajes intermedios que hay entre el ADN y las proteínas. Se une a secuencias cortas específicas y bloquea la inserción de “piezas extra” errantes en esos mensajes. Cuando TDP-43 se pierde o se reubica, como en la ELA y en muchos casos de Alzheimer, esas piezas extra —llamadas exones crípticos— pueden colarse en el ARN. Hasta ahora, la mayoría de los exones crípticos conocidos simplemente causaban la pérdida de la proteína normal al volver inestable el mensaje y provocar su degradación rápida. No estaba claro si tales eventos también podrían generar nuevas proteínas dañinas.
Un empalme críptico crea un fragmento tóxico
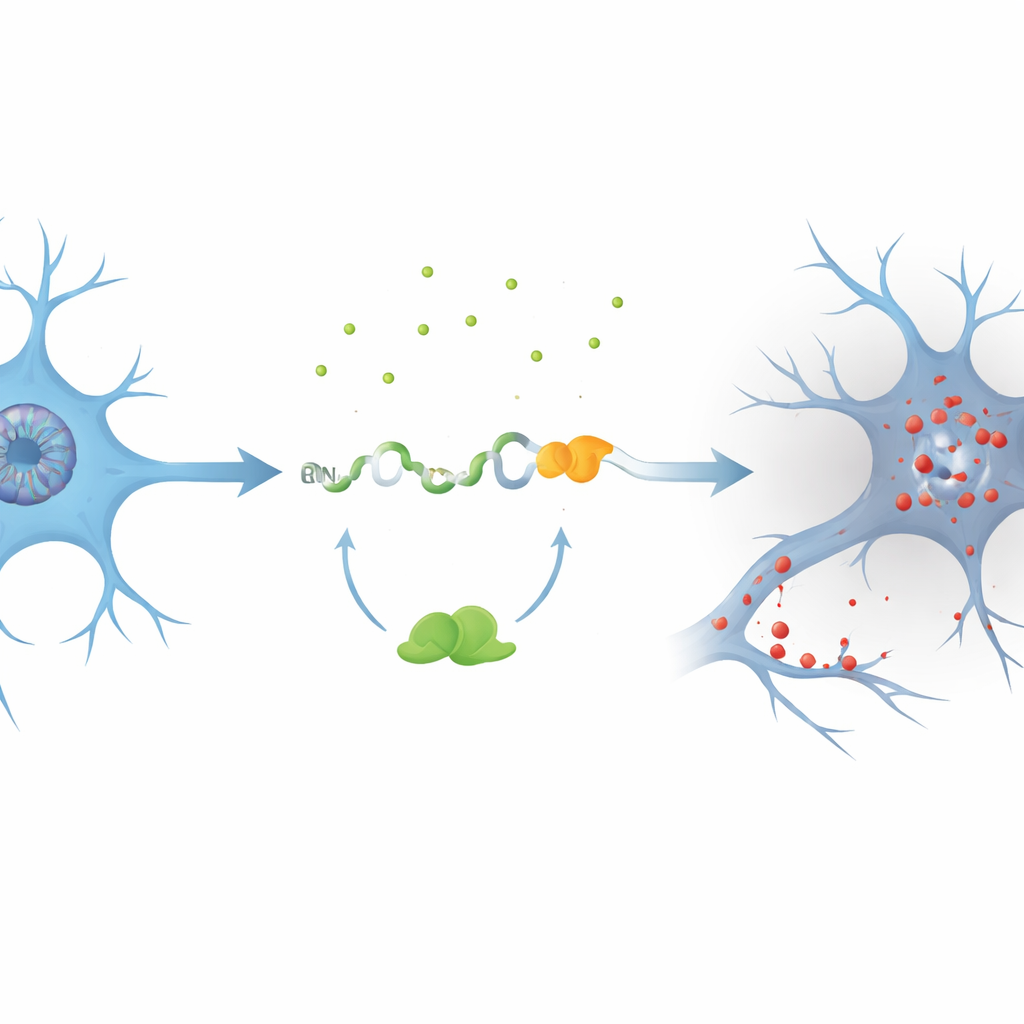
Los autores se centraron en un gen llamado PKN1, que ayuda a mantener el armazón interno y el flujo de señales de las neuronas. Usando modelos celulares con TDP-43 reducido, descubrieron un exón críptico hasta entonces no reconocido, denominado PKN1‑5a1, insertado entre dos segmentos normales del ARN de PKN1. Esta inserción introduce una señal de parada temprana, produciendo un ARN acortado. De manera notable, parte de este mensaje defectuoso escapa al sistema de control de calidad de la célula y se traduce en un fragmento estable de la proteína PKN1 que contiene solo sus primeros 207 aminoácidos. El equipo llamó a este producto truncado PKN207. Demostraron que TDP-43 normalmente previene este error uniéndose a varias regiones ricas en UG que flanquean el exón críptico; cuando esa unión se pierde, el exón se empalma y se produce PKN207.
Pruebas en cerebros de pacientes y grandes conjuntos de datos
Para ver si este evento ocurre en la enfermedad humana, los investigadores analizaron datos de secuenciación de ARN de cientos de muestras de cerebro y médula espinal de ELA. Encontraron una activación amplia del exón críptico PKN1‑5a1 en regiones conocidas por verse afectadas por la patología de TDP-43, como la corteza motora y la médula espinal, pero no en el cerebelo, relativamente preservado. Luego generaron anticuerpos altamente específicos que reconocen solo la cola única de PKN207, no la proteína PKN1 de longitud completa. En tejido hipocampal de pacientes con Alzheimer que también mostraban TDP-43 anómalo y fosforilado, estos anticuerpos detectaron una banda distintiva correspondiente a PKN207, mientras que tal banda estaba ausente en cerebros de control. Conjuntos de datos adicionales de Alzheimer confirmaron que el exón críptico se activa incluso en fases tempranas de la enfermedad, lo que sugiere que este error molecular puede comenzar mucho antes de que los síntomas sean evidentes.
Una mini‑proteína con gran impacto en la memoria
Encontrar PKN207 en cerebros humanos enfermos planteó la cuestión clave: ¿es dañina? Para probarlo, el equipo utilizó virus para impulsar la producción de PKN1 normal o de PKN207 específicamente en el hipocampo —una región cerebral crítica para la memoria— de ratones jóvenes. Meses después, ambos grupos de ratones mostraron un aprendizaje deteriorado en el laberinto acuático de Morris, nadando más tiempo para encontrar una plataforma oculta. Su líquido cefalorraquídeo contenía niveles más altos de una proteína estructural, la cadena ligera de neurofilamento, un marcador de daño axonal. En neuronas en cultivo, aumentar PKN207 provocó lesión celular, medida por la fuga de una enzima indicativa de daño de membrana. El perfil proteico detallado del hipocampo reveló cambios amplios en vías vinculadas a la fuerza sináptica (potenciación a largo plazo) y en enfermedades neurodegenerativas conocidas, con una alteración especialmente marcada de moléculas que sostienen una señalización eficiente y un andamiaje de fibras nerviosas sano.
Cómo el fragmento altera el cableado cerebral
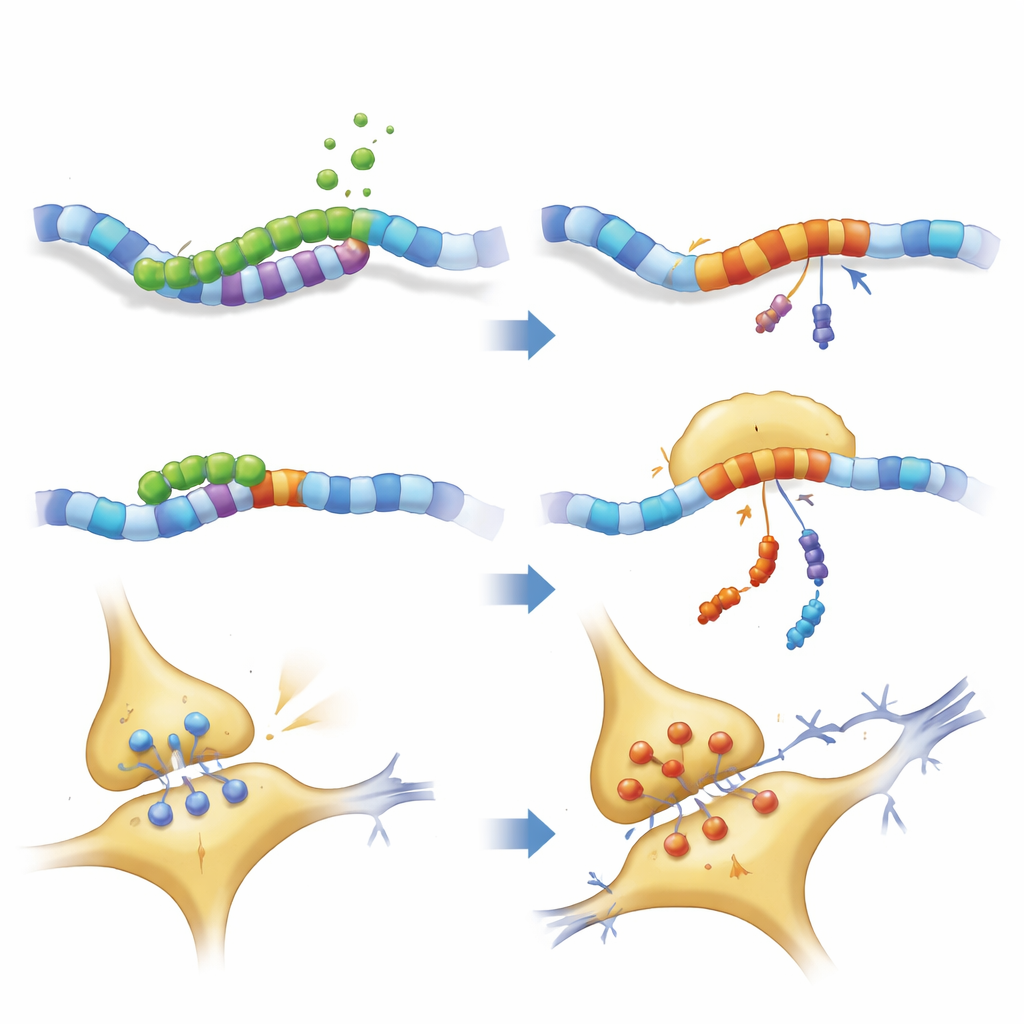
Un examen más detallado de la estructura neuronal mostró que tanto PKN1 de longitud completa como PKN207 alteraban la red de neurofilamentos que da forma a los axones y ayuda a transportar carga. Proteínas clave de motor y andamiaje se redujeron, mientras que algunos componentes de los neurofilamentos se acumularon, insinuando atascos de tráfico y posible agregación. Registros eléctricos de cortes hipocampales confirmaron que los ratones que expresaban PKN207 tenían una potenciación a largo plazo debilitada: el proceso por el cual las sinapsis se fortalecen tras actividad repetida y que es una base celular ampliamente aceptada para el aprendizaje y la memoria. Aunque PKN207 carece del dominio enzimático de PKN1, su presencia fue suficiente para imitar y a veces superar los efectos disruptivos de la proteína completa, lo que implica que la región N-terminal compartida puede, por sí sola, interferir con la homeostasis neuronal.
Por qué este hallazgo importa para las enfermedades cerebrales
Este trabajo añade una nueva capa a nuestra comprensión de los trastornos relacionados con TDP-43. En lugar de limitarse a causar pérdida de ARN esenciales, la falla de TDP-43 también puede engendrar una micro‑proteína estable y tóxica que socava las sinapsis y la cognición. El exón críptico PKN1‑5a1 y su péptido producto PKN207 destacan ahora como posibles biomarcadores de la disfunción temprana de TDP-43 y como dianas candidatas para terapias que corrijan el empalme o bloqueen el fragmento nocivo. Más en general, el estudio sugiere que otros exones ocultos podrían igualmente dar lugar a péptidos impulsores de la enfermedad, orientando a los investigadores hacia un panorama rico —y hasta ahora pasado por alto— de culpables moleculares en la neurodegeneración.
Cita: Yang, M., Wang, Q., Yan, R. et al. A neurotoxic cryptic peptide arising from TDP-43-dependent cryptic splicing of PKN1. Nat Commun 17, 2963 (2026). https://doi.org/10.1038/s41467-026-68916-0
Palabras clave: TDP-43, empalme críptico, PKN1, neurodegeneración, Alzheimer y ELA