Clear Sky Science · es
Proteínas FOX opuestas controlan epigenéticamente el equilibrio lítico‑latente del herpesvirus
Por qué importan los herpesvirus ocultos
Mucha gente alberga virus del herpes simple de por vida, a menudo sin saberlo. Estos virus pueden permanecer en silencio dentro de las neuronas durante años y luego reactivarse de forma abrupta, causando calenturas, enfermedad ocular o problemas más graves en personas con sistemas inmunitarios debilitados. Qué mantiene al virus dormido la mayor parte del tiempo y qué lo reactiva ha sido un misterio de larga data. Este estudio descubre una pieza clave de ese sistema de control: una lucha de poder entre dos grupos opuestos de proteínas humanas que remodelan el ADN viral y determinan si el herpes permanece silente o comienza a producir nuevos virus.
Dos equipos celulares que tiran en direcciones opuestas
Los autores se centraron en una gran familia de proteínas humanas que se unen al ADN, llamadas proteínas FOX, que normalmente ayudan a regular nuestros propios genes en el desarrollo y el metabolismo. Al ensayar muchos miembros de la familia FOX en células tipo neuronal, encontraron dos bandos claros. Un grupo (incluyendo proteínas como FOXF1) potenció de forma marcada la replicación del virus del herpes simple tipo 1 (VHS‑1) y varios herpesvirus «alfa» relacionados. Otro grupo (FOXK1 y FOXK2) hizo lo contrario, suprimiendo enérgicamente el crecimiento viral. Este equilibrio no fue idéntico en todos los tipos celulares: las células no neuronales y las neuronas estresadas tendían a producir más de las FOX activadoras, mientras que las neuronas sensoriales en reposo producían muy poco de ellas pero niveles altos de las FOXK represoras.
Cómo las neuronas favorecen el estado silencioso
El equipo comparó la actividad de los genes FOX a través de muchos tipos celulares humanos y de ratón y en animales infectados. Las neuronas sensoriales, el hábitat natural de la latencia del VHS‑1, mostraron un patrón que favorece el silencio: fuerte expresión de FOXK1 y FOXK2 y baja expresión de la mayoría de las FOX activadoras. En ratones, la infección temprana y señales de estrés posteriores, como el calor o la lesión tisular, elevaron selectivamente los niveles de varios genes Fox activadores sin reducir los represores. En neuronas de ratón cultivadas y en ratones vivos, eliminar o reducir FOXK facilitó la replicación del VHS‑1 y su reactivación desde la latencia. Por el contrario, forzar a las neuronas a producir más proteínas FOX activadoras fue suficiente para desencadenar la reactivación incluso sin desencadenantes químicos, lo que demuestra cuán sensible es el estado viral a este equilibrio de FOX.
Aferrarse al ADN viral y abrirlo o cerrarlo
Para entender el mecanismo subyacente, los investigadores mapearon dónde se sitúan las proteínas FOX en el genoma viral. Encontraron que tanto la FOX activadora FOXF1 como la represora FOXK1 se unen ampliamente al ADN del VHS‑1, no solo en unos pocos motivos de secuencia específicos. Esta unión depende de una región conservada de las proteínas FOX que agarra la columna vertebral del ADN más que letras individuales, lo que les permite adherirse casi en cualquier lugar. Una vez en su posición, los dos bandos reclutan socios moleculares distintos que remodelan la cromatina, la combinación de ADN y sus proteínas de empaquetamiento. Las FOX activadoras, especialmente FOXF1, se asocian con CBP y P300, enzimas que añaden grupos acetilo a las histonas y aflojan la cromatina. Esto hace que el ADN viral sea más accesible y potencia la actividad de genes virales tempranos, medianos y tardíos. FOXK1, en contraste, actúa con factores como SIN3A y MAX vinculados a la desacetilación de histonas y la represión génica, compactando la cromatina viral y manteniendo los genes apagados.
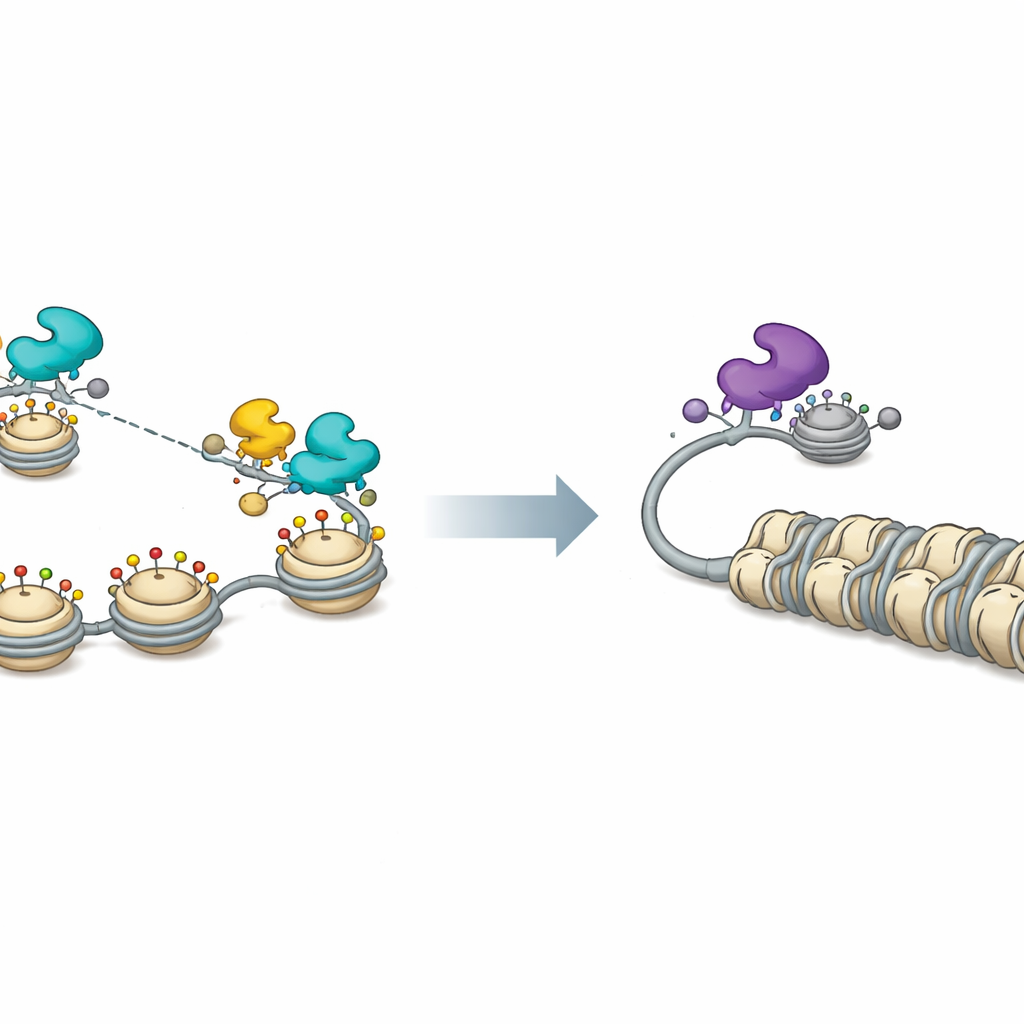
Un interruptor de cromatina para el sueño y la vigilia viral
Las mediciones de la cromatina viral confirmaron esta imagen. Cuando FOXF1 estaba presente, las histonas sobre el ADN viral mostraban marcas o modificaciones químicas asociadas con cromatina abierta y activa, y la accesibilidad general de los promotores virales aumentó en todo el genoma. La expresión de FOXF1 también dispersó pequeñas estructuras nucleares llamadas cuerpos nucleares PML que normalmente contribuyen a mantener reprimido el ADN viral. Bloquear CBP y P300 borró muchos de estos efectos activadores y redujo la expresión génica viral impulsada por FOXF1. En el lado represor, los investigadores mostraron que los socios asociados a FOXK1 y la actividad de desacetilasas de histonas eran importantes para mantener baja la replicación del VHS‑1; la inhibición química de las desacetilasas aumentó la producción viral y debilitó la supresión mediada por FOXK1.
Qué significa esto para controlar una infección de por vida
En conjunto, el trabajo sugiere que si el VHS‑1 está activo o dormido depende en gran medida de la mezcla de proteínas FOX en su neurona huésped. Las neuronas sensoriales en reposo favorecen de forma natural el estado represor dominado por FOXK, empujando al virus hacia una forma profundamente silente y con la cromatina compactada. Los estreses u otras condiciones que aumentan las FOX activadoras pueden inclinar este equilibrio, abriendo la cromatina viral y permitiendo que el ciclo lítico se reinicie. Al revelar esta lucha epigenética, el estudio pone de relieve nuevas vías por las que los científicos podrían algún día empujar a los virus del herpes hacia una latencia más firme e inofensiva o, alternativamente, forzarlos a salir del escondite en condiciones controladas para poder eliminarlos.
Cita: Xiang, Y., Yang, X., Zhang, J. et al. Counteracting FOX proteins epigenetically control the herpesvirus lytic-latent balance. Nat Commun 17, 2256 (2026). https://doi.org/10.1038/s41467-026-68915-1
Palabras clave: latencia del virus herpes simple, factores de transcripción FOX, cromatina viral</keyword:c> <keyword>regulación epigenética, reactivación viral