Clear Sky Science · es
Ampliando el potencial dañino del ADN de nucleasas metaloartificiales con química click
Construyendo tijeras moleculares más inteligentes
La quimioterapia a menudo actúa dañando el ADN de las células cancerosas, pero los fármacos actuales pueden ser herramientas toscas que también perjudican tejido sano. Este estudio explora una nueva clase de «tijeras moleculares» altamente programables formadas por cobre y pequeños fragmentos orgánicos ensamblados mediante química click. Al ajustar su forma y cómo se sujetan al ADN, los investigadores pretenden crear agentes que corten el material genético con mayor precisión, abriendo vías hacia futuros tratamientos anticancerígenos y antibacterianos.
Encajando un cortador de tres brazos
El equipo utiliza la química click catalizada por cobre, un método galardonado con el Nobel conocido por su fiabilidad, para ensamblar una familia de moléculas denominadas ligandos Tri-Click (TC). Cada molécula TC es un núcleo de tres brazos que puede alojar tres iones de cobre a la vez, formando un racimo compacto capaz de atacar el ADN. Al intercambiar distintos grupos «donantes» químicos en el extremo de cada brazo —basados en nitrógeno, oxígeno o azufre—, los científicos probaron sistemáticamente cómo cambios estructurales sutiles afectan la unión al cobre, el reconocimiento del ADN y la actividad biológica. Entre varios diseños nuevos, las versiones que incorporan donantes nitrogenados planos y cíclicos destacaron como especialmente prometedoras para sujetar el ADN con firmeza.
Encontrando una molécula principal que ama las hendiduras del ADN
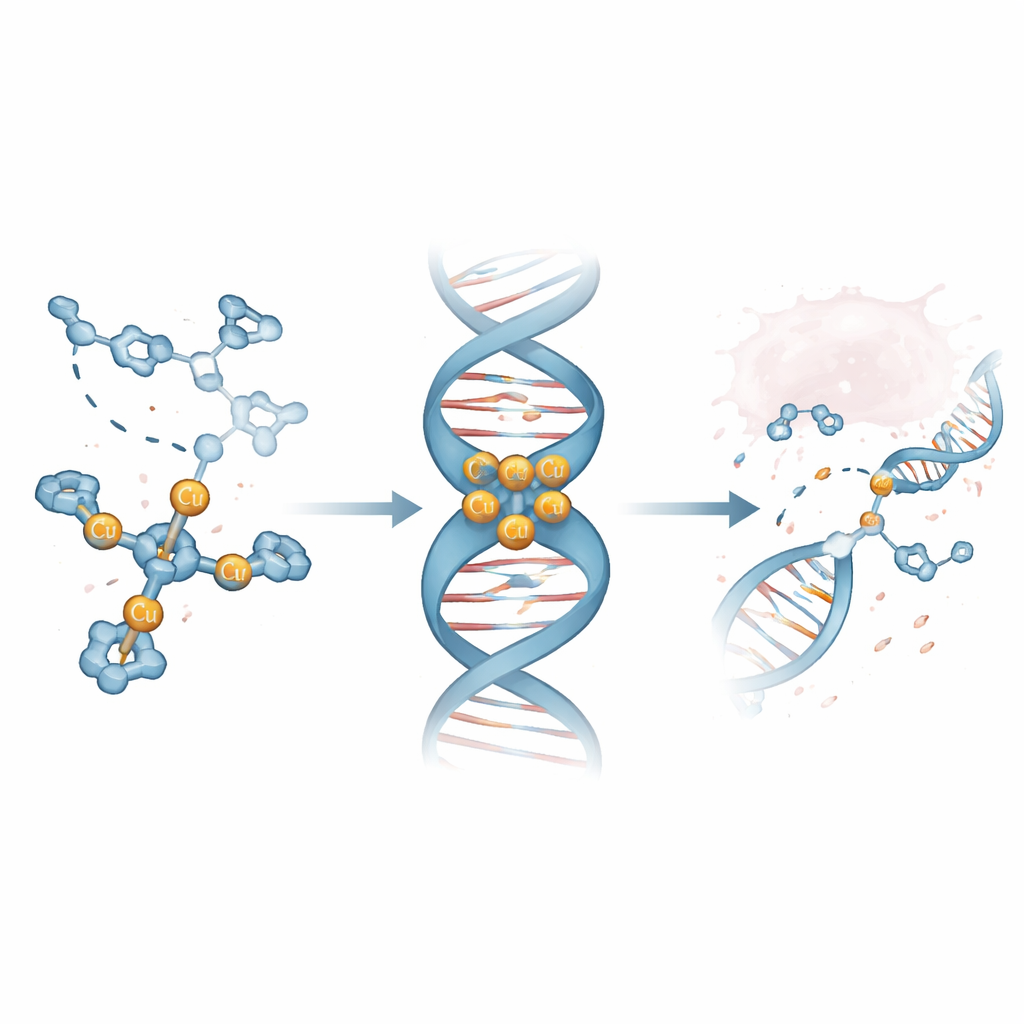
Mediante espectrometría de masas y métodos ópticos, los investigadores demostraron que un complejo, denominado Cu3-TC-Py, forma de forma fiable un racimo de tres coppers que es estable en solución. Experimentos de competencia con colorantes fluorescentes unidos a ADN de timo de ternera revelaron que Cu3-TC-Py desplaza estos colorantes a concentraciones muy bajas, lo que indica una unión fuerte al ADN. Pruebas posteriores en fragmentos cortos de ADN en forma de horquilla mostraron que este complejo prefiere alojarse en la surco menor —el valle más estrecho que recorre la doble hélice— y que favorece especialmente tramos ricos en pares de bases G y C. Simulaciones por ordenador de alta resolución respaldaron este retrato, mostrando el complejo de tres brazos situado en el surco, sus cargas positivas agarrando el ADN cargado negativamente y compactando sutilmente la hélice.
De la unión fuerte al colapso y la rotura del ADN
A nivel de molécula única, el equipo observó largas hebras de ADN confinadas en canales de tamaño nanométrico mientras interactuaban con Cu3-TC-Py. A dosis bajas, el complejo competía con un colorante de estiramiento, desplazándolo a medida que el complejo se unía en las hendiduras. A dosis más altas, el ADN comenzó a encogerse y luego a condensarse por completo, coherente con una fuerte atracción electrostática entre el racimo de cobre y la columna vertebral del ADN. Cuando ADN plasmídico se expuso al complejo en presencia de un agente reductor, las hebras pasaron de su forma nativa enrollada a formas relajadas y luego completamente linealizadas, un patrón que señala la formación de roturas de una y dos cadenas. Pruebas adicionales con captadores de radicales implicaron a especies de oxígeno de corta vida —como superóxido, oxígeno singlete y radicales hidroxilo— como las verdaderas herramientas de corte generadas cerca del complejo unido.
Atacando el ADN en células cancerosas y bacterianas
Yendo más allá del ADN purificado, los investigadores examinaron cómo se comporta Cu3-TC-Py dentro de células vivas. En paneles de células cancerosas, los ligandos libres que contienen grupos aromáticos ricos en nitrógeno mostraron una inhibición del crecimiento mucho más fuerte que diseños anteriores, y el complejo de cobre completamente formado resultó aún más potente, matando varias líneas celulares cancerosas a concentraciones micromolares. Mediciones de cobre intracelular revelaron que Cu3-TC-Py transporta cobre de manera eficiente hacia el interior celular y provoca una acumulación de ADN dañado, detectada mediante un método de imagen asistido por reparación que marca las lesiones a lo largo de hebras genómicas estiradas. En bacterias, la microscopía mostró que el tratamiento perturbó rápidamente el cromosoma bacteriano compacto, dispersando el ADN por toda la célula y reproduciendo la fragmentación severa observada con un antibiótico fuertemente dañino del ADN, consistente con una destrucción genética generalizada.
Por qué importan estas tijeras diseñadas
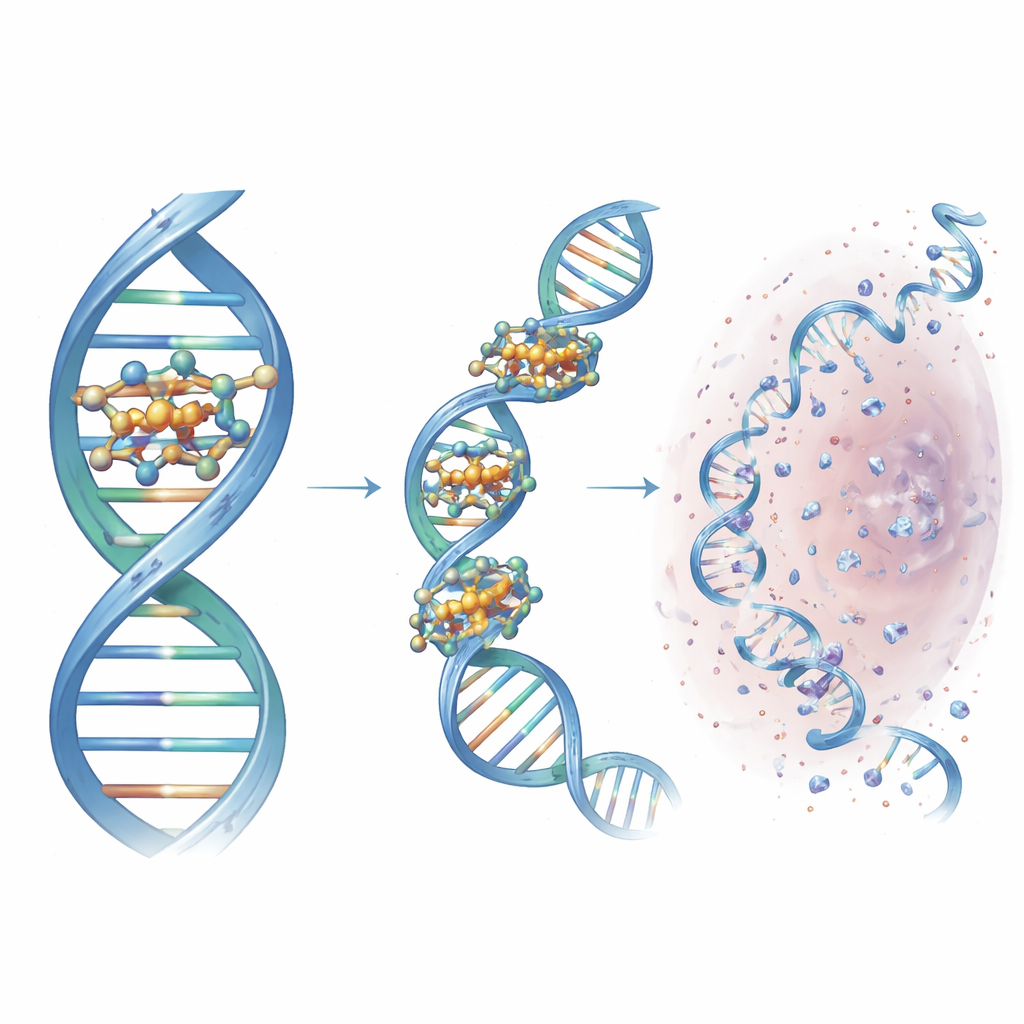
Para un público no especialista, el mensaje clave es que los investigadores han convertido un andamiaje simple y modular de química click en una máquina de corte de ADN finamente afinada. Al elegir los grupos nitrogenados cíclicos adecuados, crearon un racimo de cobre compacto que se acopla en una hendidura específica del ADN, junta las hebras y genera localmente especies reactivas de oxígeno que seccionan la doble hélice. Este compuesto líder, Cu3-TC-Py, daña el ADN de forma eficiente tanto en células cancerosas como bacterianas y muestra cómo el diseño racional puede afinar la acción de fármacos basados en metales. Aunque queda mucho trabajo antes de su uso clínico, el estudio traza reglas de diseño para las próximas generaciones de tijeras moleculares que podrían algún día ofrecer terapias contra el cáncer más dirigidas y nuevas estrategias antimicrobianas.
Cita: Gibney, A., Sidarta, M., Delahunt, E. et al. Expanding the DNA damaging potential of artificial metallo-nucleases with click chemistry. Nat Commun 17, 2309 (2026). https://doi.org/10.1038/s41467-026-68911-5
Palabras clave: química click, daño al ADN, complejos de cobre, agentes anticancerígenos, nucleasas artificiales