Clear Sky Science · es
Reutilización evolutiva de un complejo tio-lasico metabólico que permite la biosíntesis de antibióticos
Cómo los microbios cotidianos reinventan su química
Muchos de los antibióticos y medicamentos de los que dependemos son elaborados discretamente por bacterias. Estos pequeños químicos emplean enzimas —máquinas moleculares— para construir compuestos defensivos complejos. Este estudio revela cómo un enzima central del metabolismo, antes dedicado a funciones básicas de mantenimiento celular, ha sido reconfigurado evolutivamente en bacterias orales para fabricar un potente antibiótico. Comprender esta transformación no solo muestra cómo la naturaleza inventa nueva química, sino que también ofrece claves para diseñar fármacos y biocatalizadores de nueva generación.
De la metabolism básico al armamento químico
Todas las células vivas dependen de un conjunto de enzimas conservadas que gestionan su metabolismo central, como descomponer grasas y construir moléculas esenciales. Uno de esos grupos, llamado superfamilia de las tiolasas, normalmente ayuda a procesar moléculas energéticas pequeñas como acetil‑CoA y sustenta vías vitales para la síntesis de lípidos y otros componentes celulares. Los autores descubrieron que en varias especies orales de Streptococcus, un complejo trifásico basado en tiolasa —formado por proteínas relacionadas con HMGS, ACAT y una tercera proteína auxiliar— ha abandonado su papel metabólico ancestral. En su lugar, este complejo completa la biosíntesis de un antibiótico llamado reutericyclin A, que ayuda a estas bacterias a competir en el ambiente concurrido de la boca.
Un nuevo tipo de reacción enzimática sobre un andamiaje antibiótico
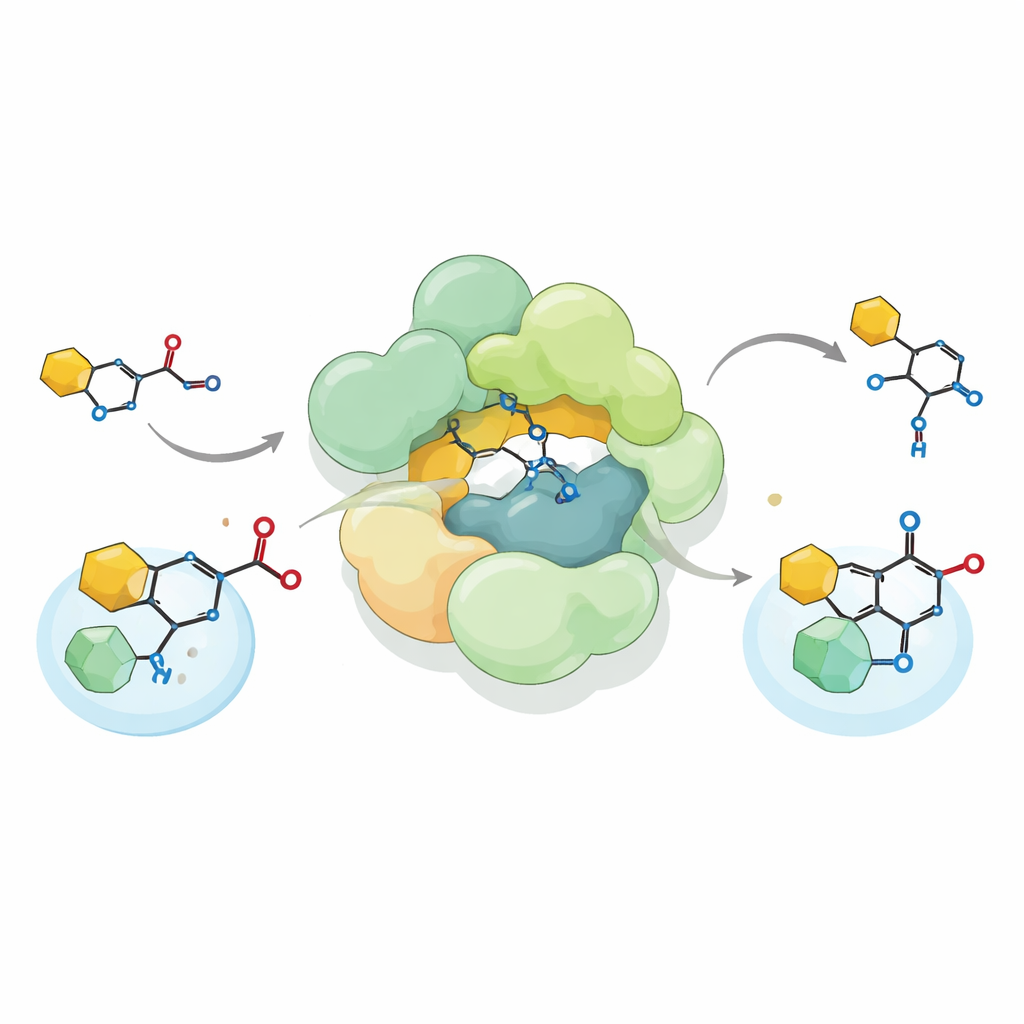
Al reconstruir el complejo de Streptococcus en el laboratorio y alimentarlo con un precursor químicamente sintetizado de reutericyclin A, los investigadores demostraron que el complejo realiza una inusual reacción de formación de enlaces carbono–carbono conocida como acilación C de Friedel–Crafts. En lugar de unir un grupo acetilo al oxígeno, como hacen muchas enzimas, instala ese grupo directamente sobre un átomo de carbono de un anillo pirrolidina-2,4-diona —una parte importante del andamiaje de reutericyclin. El complejo acepta tanto donantes acetilo naturales como acetil‑CoA como varios donantes artificiales, y puede incluso ejecutar la reacción en sentido inverso, rompiendo el enlace que creó. Esta flexibilidad amplía el repertorio conocido de aciltransferasas biológicas y sugiere cómo tales enzimas podrían adaptarse para construir productos químicos diversos.
Reaprovechamiento de un andamiaje proteico conservado
Mediante microscopía crioelectrónica de alta resolución, el equipo resolvió la estructura tridimensional del complejo de Streptococcus, denominado SmaATase. A pesar de su nueva función, SmaATase mantiene una notable semejanza arquitectónica con un complejo relacionado en arqueas que participa en la vía del mevalonato para sintetizar lípidos isoprenoides. Ambos son grandes ensamblajes multiméricos construidos a partir de módulos repetidos y presentan una cavidad compartida donde la coenzima A (CoA) puede unirse y desplazarse entre sitios activos. Sin embargo, residuos catalíticos clave que son esenciales para la reacción metabólica original están ausentes o alterados en la versión bacteriana. Pruebas bioquímicas confirman que SmaATase ya no puede sintetizar el producto ancestral HMG‑CoA y, en su lugar, utiliza acetil‑CoA únicamente como donante para sus nuevos sustratos de pequeñas moléculas.
Un rastro evolutivo desde el metabolismo hacia los antibióticos
Para entender cómo pudo desarrollarse tal reutilización, los autores compararon secuencias y actividades de complejos relacionados en muchas bacterias y arqueas. Identificaron más de mil clústeres génicos que contienen el mismo trío de tipos enzimáticos. Algunos todavía sostienen la química clásica de las tiolasas; otros, como los de Pseudomonas, alimentan diferentes antibióticos de pequeñas moléculas. Un complejo representativo de Pseudomonas fluorescens parece situarse a mitad de camino en este trayecto evolutivo: su dominio similar a HMGS está inhabilitado, pero su unidad similar a ACAT todavía realiza una reacción más convencional sobre sustratos ligados a CoA. En SmaATase y su homólogo de Pseudomonas que produce el compuesto protector de cultivos DAPG, cambios adicionales alrededor del sitio activo han adaptado las enzimas para reconocer aceptores no estándar como anillos aromáticos o núcleos de ácido tetramícico.
Por qué un pequeño grupo acetilo marca una gran diferencia
En última instancia, la ganancia biológica de esta reforma molecular es evidente. Cuando el equipo probó los antibióticos acetilados reutericyclin A y DAPG frente a un panel de bacterias Gram‑positivas, estas moléculas mostraron una fuerte actividad letal, mientras que sus precursores no acetilados fueron mucho más débiles o prácticamente inactivos. Ese pequeño grupo acetilo, colocado en la posición precisa por el complejo enzimático reutilizado, convierte un andamiaje modesto en un arma poderosa, permitiendo a Streptococcus en la boca o a Pseudomonas en torno a las raíces de las plantas superar a sus competidores. Este trabajo demuestra cómo la evolución puede reciclar marcos enzimáticos existentes con mutaciones mínimas pero estratégicas, transformando maquinaria metabólica rutinaria en herramientas especializadas de defensa química —y ofreciendo un plano para ingenieros que desean diseñar nuevos catalizadores de formación de enlaces carbono–carbono para el descubrimiento de fármacos y la biología sintética.
Cita: Liao, G., Sun, R., Shen, Z. et al. Evolutionary repurposing of a metabolic thiolase complex enables antibiotic biosynthesis. Nat Commun 17, 2196 (2026). https://doi.org/10.1038/s41467-026-68910-6
Palabras clave: evolución enzimática, biosíntesis de productos naturales, química de antibióticos, reaprovechamiento metabólico, acilación de Friedel–Crafts