Clear Sky Science · es
Ingeniería de plásmidos con orígenes de replicación sintéticos
Por qué importa reescribir el ADN microbiano
Muchas de las herramientas que sustentan la biotecnología moderna, desde la producción de insulina hasta circuitos génicos avanzados, dependen de pequeños círculos de ADN llamados plásmidos. Estos caballos de batalla genéticos transportan genes diseñados hacia bacterias, pero su diseño básico ha cambiado poco en décadas. Este estudio muestra que el núcleo mismo de los plásmidos —las secuencias que indican a las células cuándo y con qué frecuencia copiarlos— puede ser completamente reinventado. Al reconstruir este “motor de copiado” desde cero, los autores crean plásmidos que son más fáciles de ajustar, combinar y programar, abriendo la puerta a diagnósticos, biofabricación y biología sintética más flexibles.
Herramientas antiguas con límites ocultos
Los plásmidos evolucionaron naturalmente como ADN móvil, ayudando a las bacterias a compartir rasgos como resistencia a antibióticos o nuevas formas de utilizar fuentes de alimento. En el laboratorio, los ingenieros toman prestados estos plásmidos para portar genes útiles, pero la mayoría se basa en unos pocos diseños clásicos descubiertos en los años 80. Esos diseños antiguos ocultan una maraña de partes genéticas superpuestas que controlan cuántas copias de un plásmido hay en cada célula y si distintos plásmidos pueden coexistir. Como estas partes están fusionadas, cambiar una característica puede romper de forma impredecible otra. Como resultado, los científicos se ven limitados a un menú corto de plásmidos con números de copia fijos y compatibilidad limitada, lo que restringe la complejidad que pueden alcanzar los sistemas diseñados.
Reconstruir el motor de copiado desde cero
Los investigadores se centraron en un origen de replicación ampliamente utilizado de la familia de plásmidos pMB1. En su forma natural, este origen utiliza una conversación finamente equilibrada entre dos ARN—uno que inicia la replicación del ADN y otro que la apaga—para mantener el número de plásmidos bajo control. El equipo primero “refactorizó” este sistema: separaron genes superpuestos, desactivaron un promotor oculto y colocaron piezas clave en casetes genéticos separados y limpios. Solo esto demostró que la función central del origen podía preservarse mientras se simplificaba su disposición, convirtiendo una parte desordenada moldeada por la evolución en algo más parecido a una máquina modular con componentes accesibles.
Instalar mandos de control sintéticos
Con la lógica de control original expuesta, los autores la reemplazaron por reguladores totalmente sintéticos. Conectaron el cebador de replicación a interruptores de ARN diseñados que actúan como reguladores de intensidad: pequeños ARN controladores pueden activar o bloquear la producción del cebador y, en consecuencia, la replicación del plásmido. Al elegir variantes de interruptores diferentes y emparejarlas con promotores de diversa intensidad, ajustaron el número de copias de los plásmidos a lo largo de más de dos órdenes de magnitud. También exploraron distintas disposiciones físicas de los casetes de control en el ADN, descubriendo arreglos que mejoraron la estabilidad y les permitieron reducir la región de replicación a un núcleo funcional y compacto, al tiempo que añadían sistemas auxiliares naturales que evitan enredos problemáticos entre plásmidos.
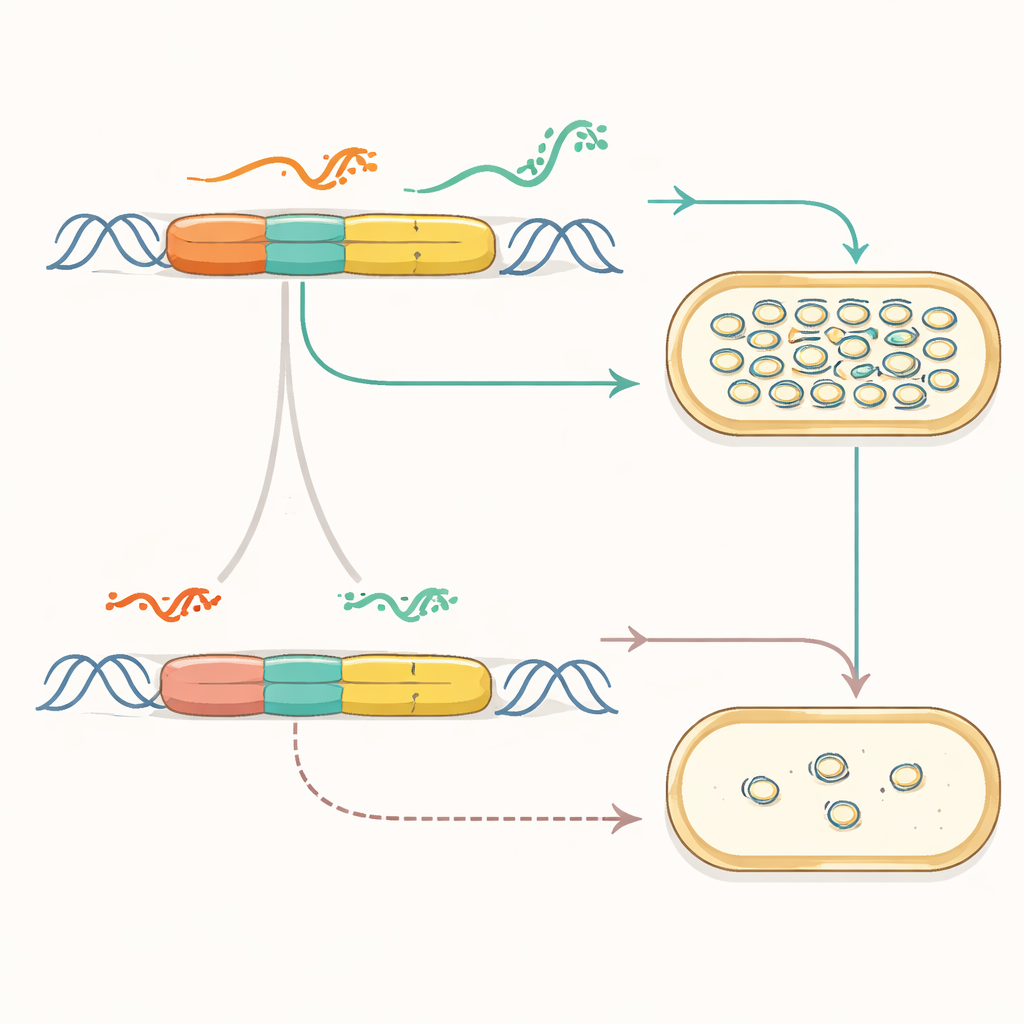
Convertir señales químicas en conteos de ADN
Una vez que el motor de copiado fue modular, el equipo mostró que podía conectarse para detectar el entorno. Vincularon el origen sintético a promotores inducibles y estructuras de ARN llamadas riboswitches, que cambian de forma en respuesta a pequeñas moléculas. En estos nuevos plásmidos, añadir un químico como IPTG o cumato provocaba que el número de copias del plásmido —y por tanto la señal de un reportero— aumentara o disminuyera. Se pudieron combinar múltiples señales de modo que una molécula impulsara la replicación mientras otra la frenaba. Los investigadores incluso construyeron pares de plásmidos, cada uno respondiendo a un químico distinto, y siguieron sus números de copia cambiantes en la misma célula mediante secuenciación de ADN, convirtiendo efectivamente los conteos de plásmidos en una etiqueta identificadora del historial ambiental.
Muchos plásmidos personalizados en una sola célula
Una prueba clave de este enfoque fue si varios plásmidos controlados de forma independiente podían coexistir. Apoyándose en una biblioteca de reguladores de ARN ortogonales, el equipo construyó seis plásmidos distintos, cada uno con su propio origen sintético y marcador antibiótico, e introdujo los seis a la vez en E. coli. La secuenciación completa de plásmidos durante varios días confirmó que los seis permanecían presentes, aunque sus abundancias relativas variaron. Los intentos de lograr lo mismo con seis plásmidos convencionales fracasaron, lo que subraya cómo el diseño refactorizado y los sistemas de estabilidad añadidos hacen que los nuevos plásmidos sean más compatibles y robustos cuando se agrupan en una sola célula.
Qué significa esto para la biotecnología futura
Para un público no especializado, la conclusión es clara: los autores han transformado los plásmidos de herramientas rígidas y uniformes en una plataforma personalizable. Sus orígenes de replicación sintéticos actúan como motores enchufables cuya velocidad, sensibilidad e entradas pueden elegirse a demanda. Esto hace posible construir bacterias que registren exposiciones químicas como cambios en el número de copias del ADN, probar muchas vías genéticas en paralelo distribuyéndolas entre múltiples plásmidos o equilibrar finamente crecimiento y producción en cepas industriales. Aunque persisten algunos compromisos en estabilidad, este trabajo muestra que la mecánica central de la replicación de plásmidos ya no está vetada a la ingeniería, abriendo nuevo espacio para la innovación en biología sintética.
Cita: Liu, B., Seet, Z.R.D., Peng, X. et al. Engineering plasmids with synthetic origins of replication. Nat Commun 17, 2255 (2026). https://doi.org/10.1038/s41467-026-68907-1
Palabras clave: plásmidos sintéticos, origen de replicación, reguladores de ARN, control del número de copias, biología sintética