Clear Sky Science · es
El receptor de succinato 1 restringe la hematopoyesis y previene la progresión de la leucemia mieloide aguda
Cuando el combustible celular se sale de control
Nuestra sangre se renueva constantemente gracias a una pequeña población de células madre escondidas en la médula ósea. Este estudio investiga cómo un subproducto metabólico común, el succinato, y su sensor en la superficie celular actúan como un freno sobre este sistema de renovación. Cuando ese freno falla, el equilibrio entre la producción sanguínea sana y el crecimiento canceroso puede inclinarse hacia la leucemia mieloide aguda (LMA), un cáncer sanguíneo agresivo. Comprender este interruptor de control oculto podría conducir a tratamientos más precisos que dominen la enfermedad restaurando las propias salvaguardias del organismo.
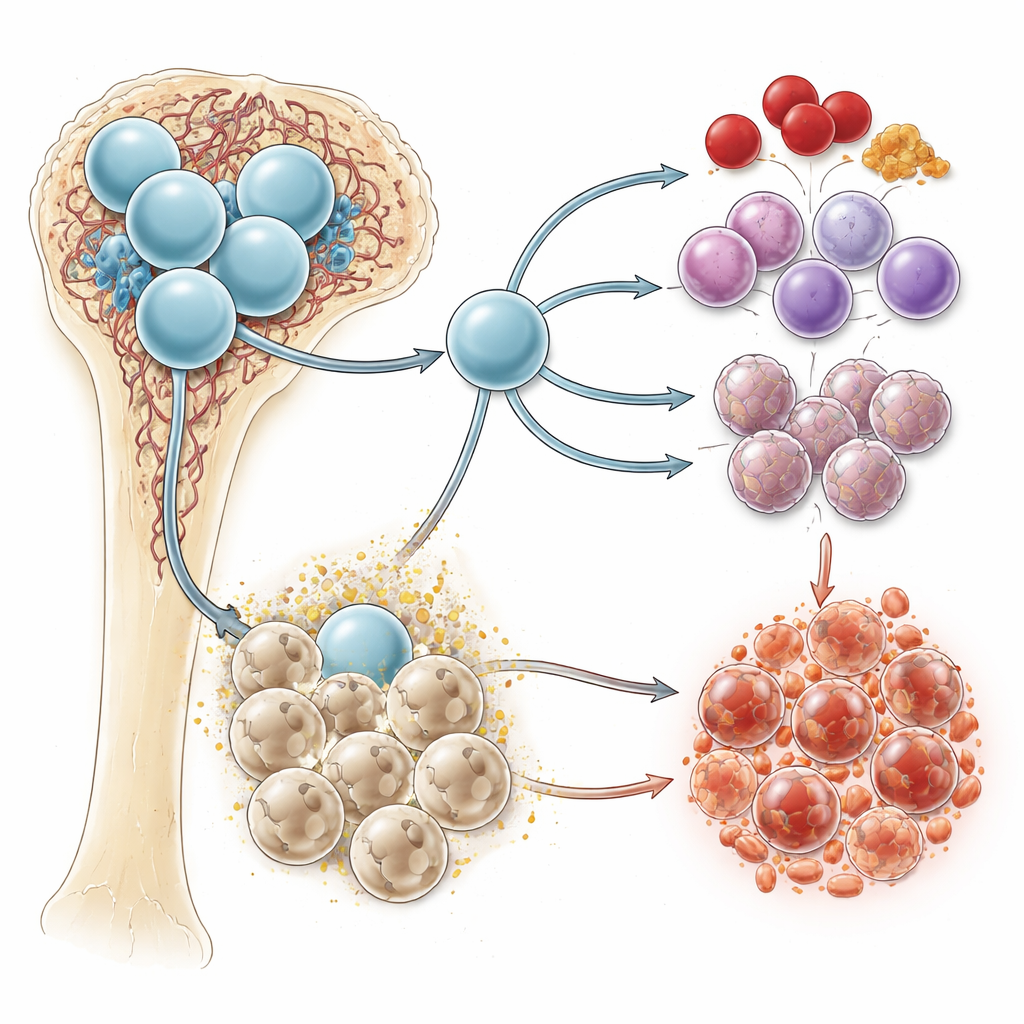
Una señal química con doble papel
El succinato es un subproducto habitual de cómo las células queman combustible, especialmente dentro de las mitocondrias, las centrales energéticas celulares. En condiciones de bajo oxígeno —como las que se encuentran en la médula ósea— el succinato tiende a acumularse. Puede actuar dentro de las células, alterando el metabolismo y las respuestas inflamatorias, y también puede salir al exterior para hacer de señal. En la superficie celular, un receptor llamado SUCNR1 detecta el succinato y transmite su presencia hacia el interior. Trabajos previos vincularon al succinato y a SUCNR1 con la inflamación y entornos favorables al cáncer, pero su papel directo en la formación de la sangre y la leucemia no estaba claro.
Una señal de advertencia en pacientes con leucemia
Los investigadores analizaron datos de expresión génica de cientos de pacientes con LMA y descubrieron que los niveles de SUCNR1 varían ampliamente entre individuos. Los pacientes cuyas células leucémicas producían poco SUCNR1 tuvieron una supervivencia global y una supervivencia libre de progresión más cortas, incluso tras ajustar por edad, sexo y subtipos clínicos estándar. Ciertos subgrupos genéticos de LMA tendían a mostrar niveles particularmente bajos de SUCNR1. Cuando el equipo trasplantó células humanas de LMA carentes de SUCNR1 en ratones inmunodeficientes y luego inyectó a los animales ácido succínico (que en el organismo se convierte en succinato), la carga leucémica en la médula ósea aumentó. Esto sugiere que, en cánceres con poco SUCNR1, el succinato adicional puede en realidad alimentar la progresión de la enfermedad en lugar de frenarla.
El freno oculto sobre las células madre sanguíneas
Para entender cómo actúa SUCNR1 en la formación normal de la sangre, los científicos recurrieron a ratones genéticamente modificados. Cuando SUCNR1 se eliminó ya fuese en todo el animal o solo en las células formadoras de sangre, la médula ósea se volvió hiperactiva. Las células madre y progenitoras se expandieron, y tanto las células mieloides (como monocitos y granulocitos) como las células B aumentaron en sangre y bazo. Estas células con características de progenitor sobrevivieron mejor y formaron más colonias en placas de laboratorio, aunque eran ligeramente menos capaces de restablecer la producción sanguínea cuando se trasplantaron en competencia con células normales. Una línea de ratones con un reportero especial mostró que solo un subconjunto de células madre y progenitoras expresa realmente SUCNR1; esas células SUCNR1-positivas tenían un potencial de injerto particularmente limitado. En conjunto, el receptor actuaba como una restricción sobre el tamaño y la actividad del reservorio de células madre.
De la defensa equilibrada al sobreimpulso inflamatorio
Un perfil detallado de expresión génica de las células madre y progenitoras carentes de SUCNR1 reveló un cambio notable. Las firmas de células madre primitivas y en calma se vieron atenuadas, mientras que se reforzaron genes vinculados a la inflamación, especies reactivas de oxígeno y células sanguíneas maduras. Dos moléculas destacaron: S100A8 y S100A9, un par de “alarminas” que amplifican la señal inflamatoria. Estos factores aumentaron tanto dentro del compartimento de células madre como en el líquido circundante de la médula ósea. Cuando el equipo trató a ratones deficientes en SUCNR1 con tasquinimod, un fármaco que bloquea la señalización de S100A9, la expansión excesiva de células madre y progenitoras, así como la sobreproducción de células mieloides y B, se revirtieron en gran medida. En otras palabras, gran parte del daño por la pérdida de SUCNR1 pudo deshacerse interrumpiendo el circuito de alarma S100A8/S100A9.
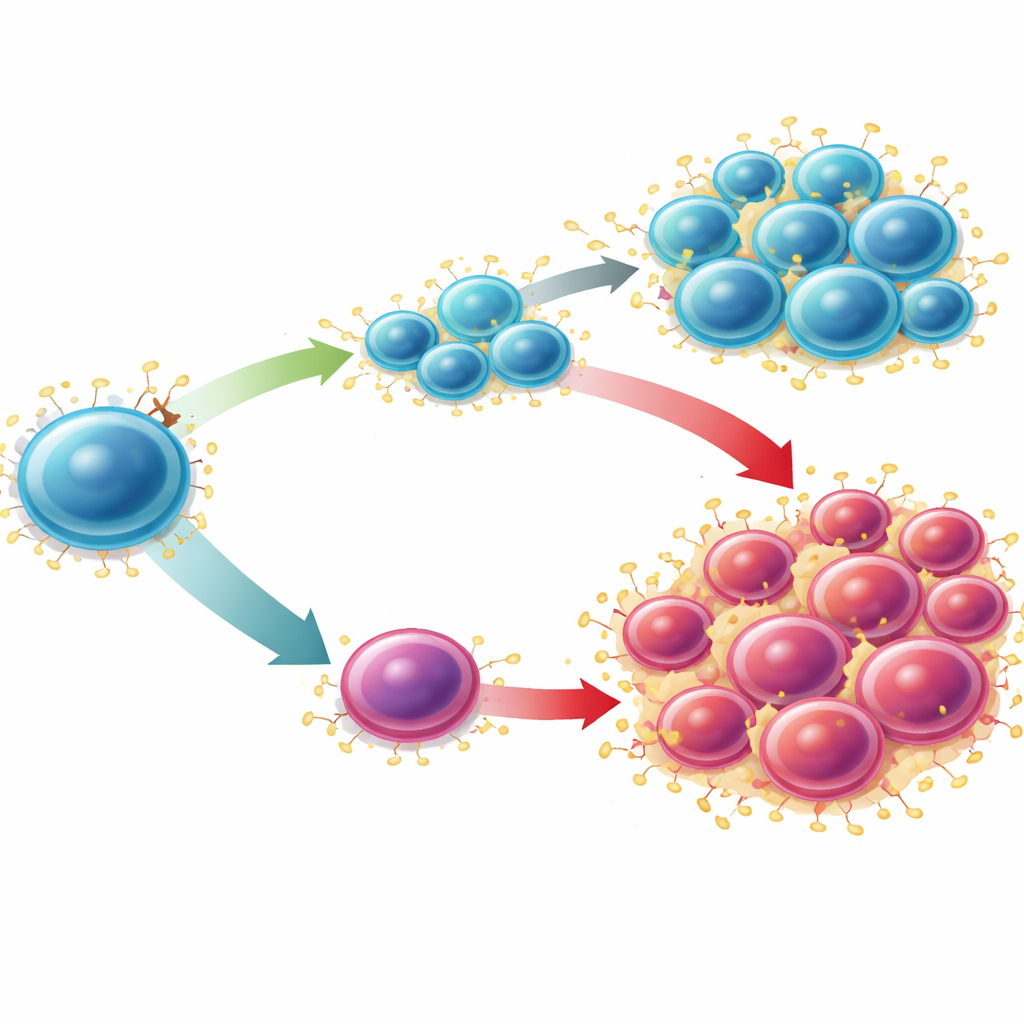
Convertir una vulnerabilidad en una estrategia terapéutica
Los científicos preguntaron entonces si esta vía podría explotarse terapéuticamente en LMA. En una leucemia agresiva de ratón impulsada por la mutación MLL-AF9 —donde los niveles de Sucnr1 son muy bajos— bloquear S100A9 con tasquinimod, especialmente cuando se combinaba con un compuesto potente que activa SUCNR1, redujo las células con carácter de célula madre leucémica y disminuyó la carga de la enfermedad en médula ósea y bazo. Los análisis de datos de ARN unicelular de modelos humanos de LMA tratados con el quimioterápico citarabina mostraron que los cúmulos celulares resistentes eran ricos en S100A8 y S100A9, mientras que SUCNR1 era escaso y se asociaba con un subconjunto distinto, metabólicamente activo, que se redujo tras el tratamiento. En líneas celulares humanas de leucemia, la activación de SUCNR1 aumentó la muerte celular inducida por la quimioterapia y pudo desencadenar apoptosis por sí sola cuando SUCNR1 se sobreexpresó. En conjunto, estos hallazgos sitúan a SUCNR1 bajo no solo como un marcador de mal pronóstico, sino también como una debilidad: las células leucémicas que han perdido este freno pueden depender en gran medida del eje S100A8/S100A9 y ser particularmente sensibles a estrategias que reactiven la señalización de SUCNR1 o bloqueen la alarma aguas abajo.
Una nueva palanca para domar la leucemia
Para un lector no especializado, el mensaje central es que un subproducto metabólico aparentemente mundano, el succinato, y su receptor SUCNR1 constituyen un sistema de seguridad inesperado en la formación de la sangre. Cuando SUCNR1 está presente y activo, mantiene las células madre bajo control y evita el crecimiento desbocado. Cuando SUCNR1 se pierde o está bajo —frecuente en algunos pacientes con LMA— el succinato y alarminas inflamatorias como S100A8 y S100A9 pueden empujar a las células madre y progenitoras hacia una sobreexpansión y la leucemia. Combinando fármacos que atenúen esta alarma inflamatoria con agentes que restauren o imiten la señalización de SUCNR1, podría ser posible reconducir el sistema hacia una producción sanguínea equilibrada y mejorar la eficacia de la quimioterapia existente.
Cita: Cuminetti, V., Boet, E., Heugel, M. et al. Succinate receptor 1 restricts hematopoiesis and prevents acute myeloid leukemia progression. Nat Commun 17, 2403 (2026). https://doi.org/10.1038/s41467-026-68906-2
Palabras clave: leucemia mieloide aguda, receptor de succinato, células madre hematopoyéticas, metabolismo y cáncer, señalización inflamatoria