Clear Sky Science · es
Oxidasas de alcohol diseñadas catalizan transesterificación en medio acuoso sin hidrólisis competitiva
Por qué importa esta historia enzimática
Muchos productos cotidianos, desde medicamentos y aromas alimentarios hasta biodiésel, dependen de un tipo simple de enlace químico llamado éster. Fabricar y ajustar estos ésteres de manera eficiente, económica y respetuosa con el medio ambiente es un objetivo clave en la química verde. El problema es que el agua, el disolvente ideal desde el punto de vista de la seguridad y la sostenibilidad, suele sabotear estas reacciones al romper los ésteres tan rápido como se forman. Este estudio revela una enzima diseñada que puede construir ésteres en agua mientras ignora casi por completo el agua circundante, abriendo una vía hacia una química industrial más limpia.
Convertir una enzima conocida a un nuevo trabajo
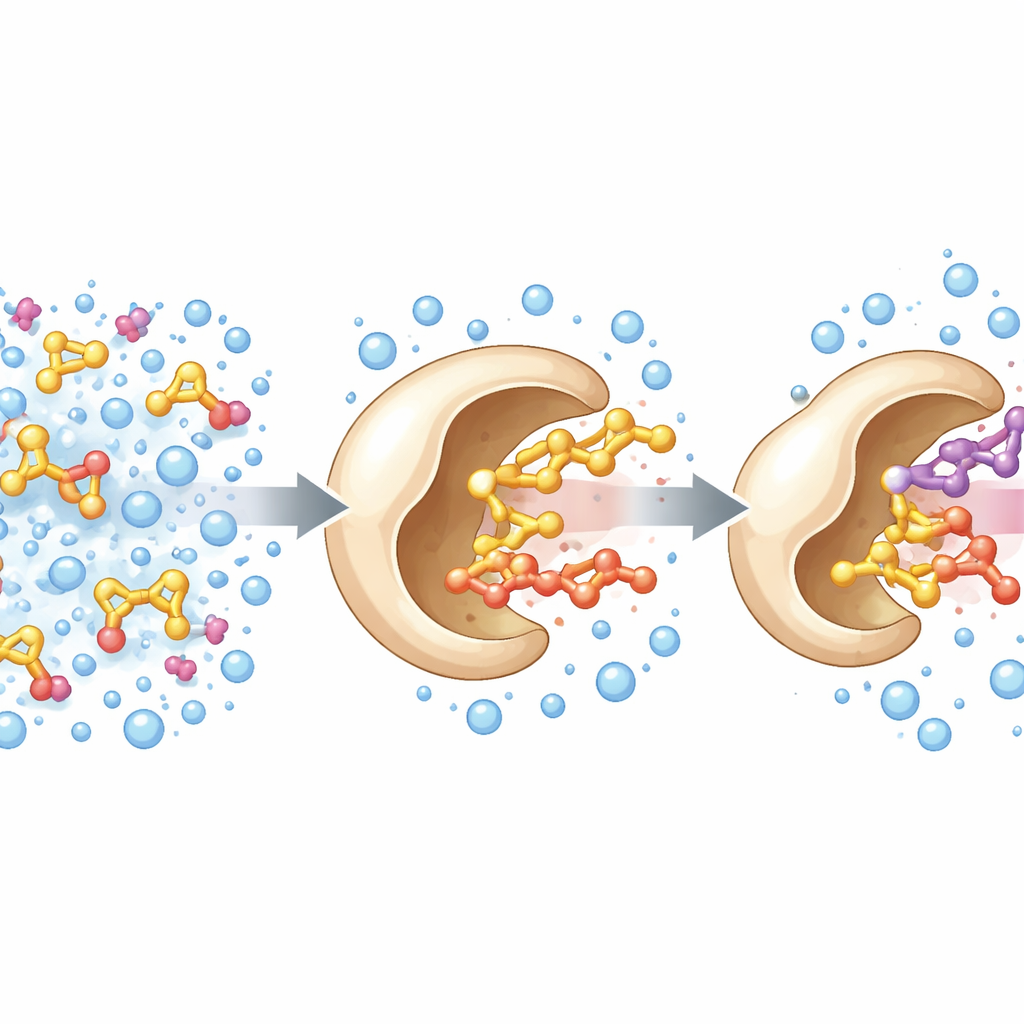
Los investigadores partieron de una enzima conocida, una alcohol oxidasa de un hongo que descompone la madera. En la naturaleza, esta enzima usa un cofactor flavínico para ayudar a extraer electrones de alcoholes pequeños como el metanol. El equipo se propuso ampliar su alcance para que pudiera manejar alcoholes más voluminosos, que son más relevantes para productos químicos finos y aromas. Utilizando la estructura tridimensional de la enzima como hoja de ruta, se centraron en tres aminoácidos que forman una especie de puerta de entrada al sitio activo. Al aleatorizar estas posiciones y cribar las variantes resultantes, descubrieron un triple mutante—denominado PcAOx‑VPN—que podía procesar eficientemente alcoholes mayores como el alcohol bencílico mientras perdía gran parte de su actividad original hacia los más pequeños como el metanol.
Talento inesperado: construir ésteres en agua
Al evaluar PcAOx‑VPN en mezclas diseñadas para disolver sustratos oleosos, el equipo observó picos adicionales en sus lecturas analíticas. Estos resultaron ser productos acetilados: la enzima estaba transfiriendo un grupo acilo desde un donador de ester activado a alcoholes, una reacción conocida como transesterificación. De manera notable, esto tuvo lugar en tampón acuoso, algo que normalmente conduce a una fuerte hidrólisis competitiva, donde el agua ataca y destruye el éster. Aquí, PcAOx‑VPN unió eficientemente alcoholes y donadores acílicos como el acetato de vinilo para formar nuevos ésteres, a menudo con rendimientos superiores al 80% y con reacciones secundarias solo modestamente presentes. La misma enzima incluso actuó sobre una amplia variedad de alcoholes, incluidos cadenas lineales, aromáticos, quirales y que contienen azufre, y mostró una marcada preferencia por una de las formas espejo en varios casos.
Mantener el agua fuera del camino
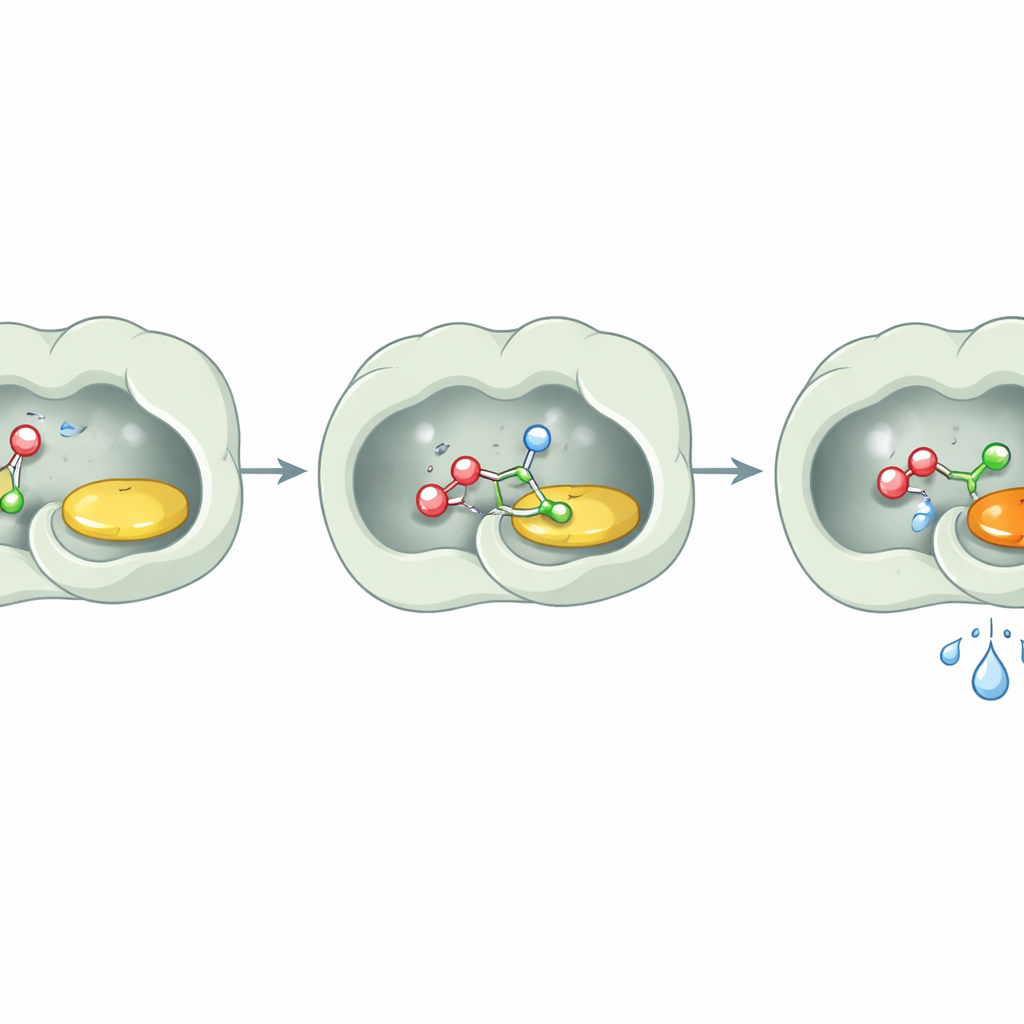
Una sorpresa clave fue lo que la enzima no hizo: no hidrolizó los ésteres de forma apreciable. Incluso después de largas incubaciones con sustratos éster y agua, PcAOx‑VPN los dejó esencialmente intactos a menos que se añadiera un donador acílico adicional. Los estudios estructurales ofrecen una explicación sencilla. El sitio activo está revestido con aminoácidos en gran parte oleosos y aromáticos que crean una cavidad altamente hidrofóbica. El análisis detallado no mostró moléculas de agua cercanas al cofactor flavínico, y herramientas computacionales confirmaron que el canal de acceso al sitio activo también es poco amigable para el agua. En esencia, la enzima construye una pequeña sala seca dentro de un mundo acuoso. Los alcoholes y los ésteres activados pueden entrar y reaccionar, pero las moléculas de agua se mantienen a distancia, de modo que nunca tienen la oportunidad de deshacer el producto.
Cómo funciona probablemente la reacción en el interior
Experimentos mecanísticos y análisis por mutación revelaron que dos aminoácidos, una histidina y una asparagina, son centrales tanto para el papel natural de oxidación de la enzima como para su nuevo talento en transesterificación. La histidina actúa como una base, ayudando a retirar un protón del alcohol entrante y haciéndolo más reactivo, mientras que la asparagina estabiliza el estado cargado que resulta. Juntos, promueven el ataque del alcohol sobre el donador acílico para formar un intermedio de vida corta que colapsa en el éster deseado. El estado oxidado del cofactor flavínico también es necesario: en condiciones sin oxígeno, cuando el flavín se reduce, la transesterificación se detiene y se reanuda solo al reintroducir aire. Cabe destacar que, cuando el mismo trío de mutaciones se introdujo en oxidasas relacionadas de otros hongos, esas enzimas también ganaron una actividad robusta de transesterificación, lo que sugiere que este comportamiento puede generalizarse.
Qué implica esto para una química más verde
Para no especialistas, el mensaje central es que los autores han enseñado a una enzima conocida a hacer un truco nuevo: construir ésteres útiles directamente en agua, mientras ignora de forma efectiva la tendencia del agua a deshacer el trabajo. Al tallar un bolsillo seco y amigable con el aceite dentro de una proteína y ajustar unos pocos aminoácidos clave, crearon un catalizador que favorece a los alcoholes sobre el agua como socios de reacción. Dado que el mismo principio de diseño funciona en enzimas relacionadas, este enfoque podría extenderse a una familia de catalizadores para fabricar aromas, fragancias, productos químicos finos y posiblemente biocombustibles en procesos más seguros y sostenibles que dependan menos de disolventes orgánicos agresivos y más del agua.
Cita: Wu, B., Ma, Y., Feng, C. et al. Engineered alcohol oxidases catalyse transesterification in aqueous media without competing hydrolysis. Nat Commun 17, 2183 (2026). https://doi.org/10.1038/s41467-026-68899-y
Palabras clave: ingeniería de enzimas, biocatálisis, química verde, síntesis de ésteres, flavoproteínas