Clear Sky Science · es
La inhibición de la señalización TGF‑β en microglía estimula la neurogénesis adulta en el hipocampo y reduce conductas ansiosas en ratones adultos
Por qué las células inmunitarias del cerebro importan para el ánimo y la memoria
La mayoría de nosotros pensamos en las células inmunitarias como vigilantes del cuerpo, no como moduladoras de nuestros pensamientos y sentimientos. Este estudio desafía esa idea al mostrar que la microglía —las células inmunitarias que residen en el cerebro— puede influir de manera potente en el nacimiento de nuevas neuronas en el hipocampo, una región importante para la memoria y la emoción. Al apagar una vía de señalización específica en la microglía de ratones adultos, los investigadores aumentaron la producción y la supervivencia de nuevas neuronas y observaron cambios medibles en conductas de tipo ansioso.
La modesta guardería cerebral para nuevas neuronas
En mamíferos adultos, todavía nacen nuevas neuronas en unas pocas “guarderías” especializadas. Una de las más importantes es la zona subgranular del hipocampo, que ayuda a separar recuerdos similares, apoya el aprendizaje y contribuye a la regulación del estado de ánimo. En condiciones normales, muchas de estas células recién nacidas mueren antes de madurar por completo. Su número puede aumentar o disminuir en respuesta al ejercicio, entornos enriquecidos, estrés, ictus o epilepsia. La microglía vigila constantemente este entorno, pero no estaba claro si su estado reactivo, “inflamado”, favorece o perjudica esta neurogénesis adulta.
Desactivar un freno clave en la microglía
El equipo se centró en una molécula de señalización llamada TGF‑beta, que normalmente mantiene a la microglía en un estado calmado y homeostático. Usando ratones genéticamente modificados, desactivaron selectivamente la señalización de TGF‑beta en microglía durante la edad adulta —bien eliminando la propia ligando TGF‑beta o bien los receptores (ALK5 o TβRII) que la detectan. Esto empujó a la microglía hacia un perfil reactivo y proinflamatorio sin provocar una pérdida neuronal generalizada. En este estado, la microglía aumentó en número y cambió de forma, lo que indica activación, pero las células de soporte vecinas llamadas astrocitos permanecieron en gran medida sin cambios.
Más neuronas nuevas, mejor supervivencia y ansiedad alterada
Cuando se bloqueó la señalización de TGF‑beta en la microglía, la “guardería” hipocámpica produjo un aumento de neuronas inmaduras marcadas por la proteína DCX. Este pico apareció aproximadamente tres semanas después del cambio genético y condujo a un aumento sostenido de neuronas completamente maduras semanas después. El seguimiento cuidadoso de las células en división mostró que el efecto principal fue una mejor supervivencia de las neuronas recién nacidas, no simplemente una división celular más rápida. Eliminar por completo la microglía con un fármaco no reprodujo este efecto, lo que sugiere que no es la ausencia de microglía lo que importa, sino el perfil reactivo específico creado cuando se silencia TGF‑beta. A nivel conductual, los ratones con microglía deficiente en TGF‑beta pasaron más tiempo en los brazos abiertos de laberintos elevados, un indicador común de reducción de conductas ansiosas o desinhibición. Estos cambios desaparecieron cuando la microglía volvió a un estado más normal en algunos modelos, pero persistieron en otros donde la microglía permaneció reactiva.
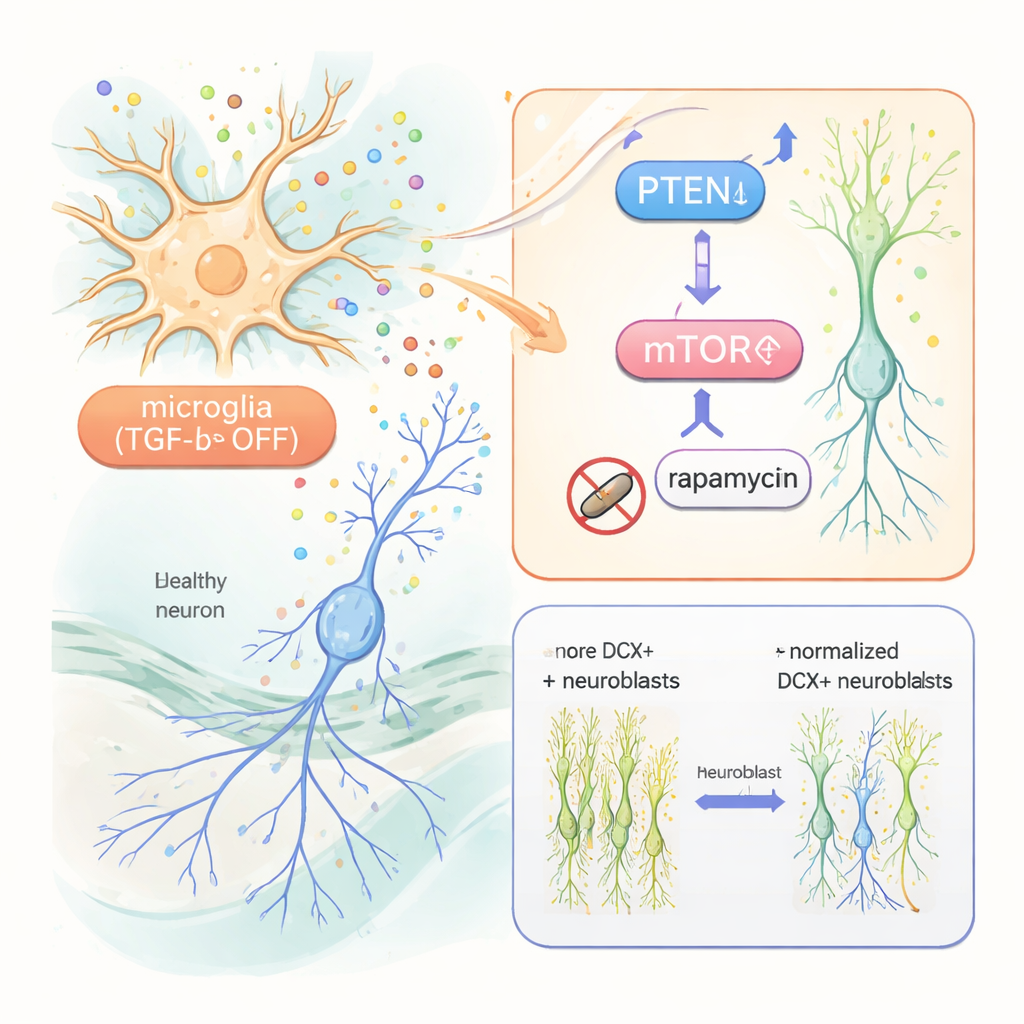
Descubriendo la vía dentro de las neuronas recién nacidas
Para entender cómo la microglía alterada se comunica con las neuronas recién nacidas, los investigadores usaron secuenciación de ARN a nivel de célula única en células hipocámpicas. Encontraron cambios amplios en la actividad génica no solo en la microglía sino también en las neuronas inmaduras. Entre los hallazgos clave hubo una reducción de PTEN, una proteína que normalmente restringe el crecimiento celular, y signos de mayor actividad en la vía mTOR, que promueve la supervivencia y el crecimiento celular. Curiosamente, factores de crecimiento bien conocidos como IGF‑1 y TNF‑alfa, aunque elevados en la microglía reactiva, resultaron no ser necesarios: incluso cuando se eliminaron genéticamente, el aumento de la neurogénesis se mantuvo. En contraste, cuando el equipo trató a los ratones con rapamicina, un fármaco que bloquea mTOR, el exceso de neuronas inmaduras y su exuberante ramificación volvieron a la normalidad. Las neuronas recién nacidas también mostraron niveles más altos de un marcador downstream de mTOR, que la rapamicina redujo.
Qué podría significar esto para la salud cerebral
En conjunto, los hallazgos sugieren que cuando se apaga la señalización TGF‑beta en la microglía, estas células adoptan un estado reactivo que favorece la supervivencia e integración de las neuronas hipocámpicas recién nacidas a través de una vía PTEN–mTOR dentro de esas neuronas. Esto, a su vez, se asocia con una menor conducta ansiosa en ratones, aunque también puede acompañarse de cambios en el aprendizaje y la memoria. Para un lector no especializado, el mensaje clave es que las propias células inmunitarias del cerebro pueden ajustar finamente cuántas neuronas nuevas se incorporan a nuestros circuitos de memoria —y que manipular cuidadosamente este sistema podría algún día ayudar a potenciar la neurogénesis beneficiosa o frenar neuronas que crecen de forma excesiva en condiciones como la epilepsia o tras una lesión cerebral.
Cita: Ware, K., Peter, J., Yazell, J. et al. Inhibition of TGF-β signaling in microglia stimulates hippocampal adult neurogenesis and reduces anxiety-like behavior in adult mice. Nat Commun 17, 1440 (2026). https://doi.org/10.1038/s41467-026-68885-4
Palabras clave: neurogénesis adulta, microglía, hipocampo, conducta ansiosa, señalización TGF‑beta