Clear Sky Science · es
La adaptación posraduccional mediada por PRMT3 al ayuno regula la flexibilidad metabólica
Por qué importa el momento de las comidas y el combustible corporal
Mucha gente prueba el ayuno o la alimentación con tiempo restringido para perder peso o mejorar el azúcar en sangre, pero los resultados pueden ser variables. Este estudio examina a fondo nuestro metabolismo para averiguar por qué. Centrándose en la grasa abdominal de ratones y en muestras humanas, los investigadores descubren un interruptor molecular que ayuda al tejido adiposo a decidir si quemar o almacenar combustible, y muestran cómo tanto el horario de las comidas como un fármaco pueden activar ese interruptor hacia una mejor salud.
Un motor flexible dentro de nuestra grasa
Nuestros cuerpos funcionan mejor cuando pueden cambiar sin problemas entre quemar grasa durante el ayuno y quemar azúcar después de las comidas. Esta “flexibilidad metabólica” a menudo se pierde en la obesidad, lo que dificulta manejar las oscilaciones en el suministro y la demanda de energía. El equipo estudió la grasa blanca visceral—la grasa profunda del abdomen fuertemente ligada a la diabetes y las enfermedades cardíacas—y encontró que etiquetas químicas específicas en las proteínas, llamadas grupos metilo, cambian con la ingesta y el ayuno. En ratones y en humanos, dos de estas marcas, MMA y ADMA, se acumulan en la grasa visceral a medida que aumentan el peso corporal y el índice de masa corporal, lo que sugiere que son marcadores de un metabolismo lento y menos adaptable.
Una señal de alimentación que endurece el metabolismo
Los investigadores se centraron en una enzima en las células grasas llamada PRMT3, que añade estas marcas de metilación. En ratones, los niveles de PRMT3 en la grasa visceral aumentan durante la noche cuando los animales comen y disminuyen durante el día cuando ayunan, siguiendo de cerca el patrón de MMA y ADMA. Este ritmo depende de la insulina y de una proteína de señalización clave, AKT: cuando la comida o la insulina inyectada activan AKT, PRMT3 se activa y sufre más modificaciones, lo que a su vez aumenta la cantidad de proteínas metiladas. Bloquear AKT o inhibir PRMT3 directamente aplana rápidamente esta señal de metilación, incluso imitando el efecto de un ayuno mucho más prolongado.
Reconectar las células grasas de almacenar a quemar
¿Qué hace realmente este etiquetado químico? El estudio demuestra que PRMT3 estabiliza una proteína transportadora llamada SLC25A1 en las mitocondrias—las fábricas de energía de la célula. SLC25A1 mueve citrato, un intermedio metabólico clave, fuera de las mitocondrias hacia el citosol donde alimenta la producción de nueva grasa. PRMT3 metila dos sitios específicos de arginina en SLC25A1, haciendo el transportador más estable y fomentando la exportación de citrato y la síntesis de grasa. Cuando se bloquea PRMT3, los niveles de SLC25A1 disminuyen, la exportación de citrato cae y las células grasas se orientan hacia la degradación de azúcar en lugar de la producción de más grasa. En ratones con dieta alta en grasa, un fármaco que bloquea PRMT3 reduce la grasa corporal, mejora el control glucémico y aumenta una medida llamada cociente respiratorio, lo que muestra que los animales cambian con más facilidad a quemar carbohidratos.
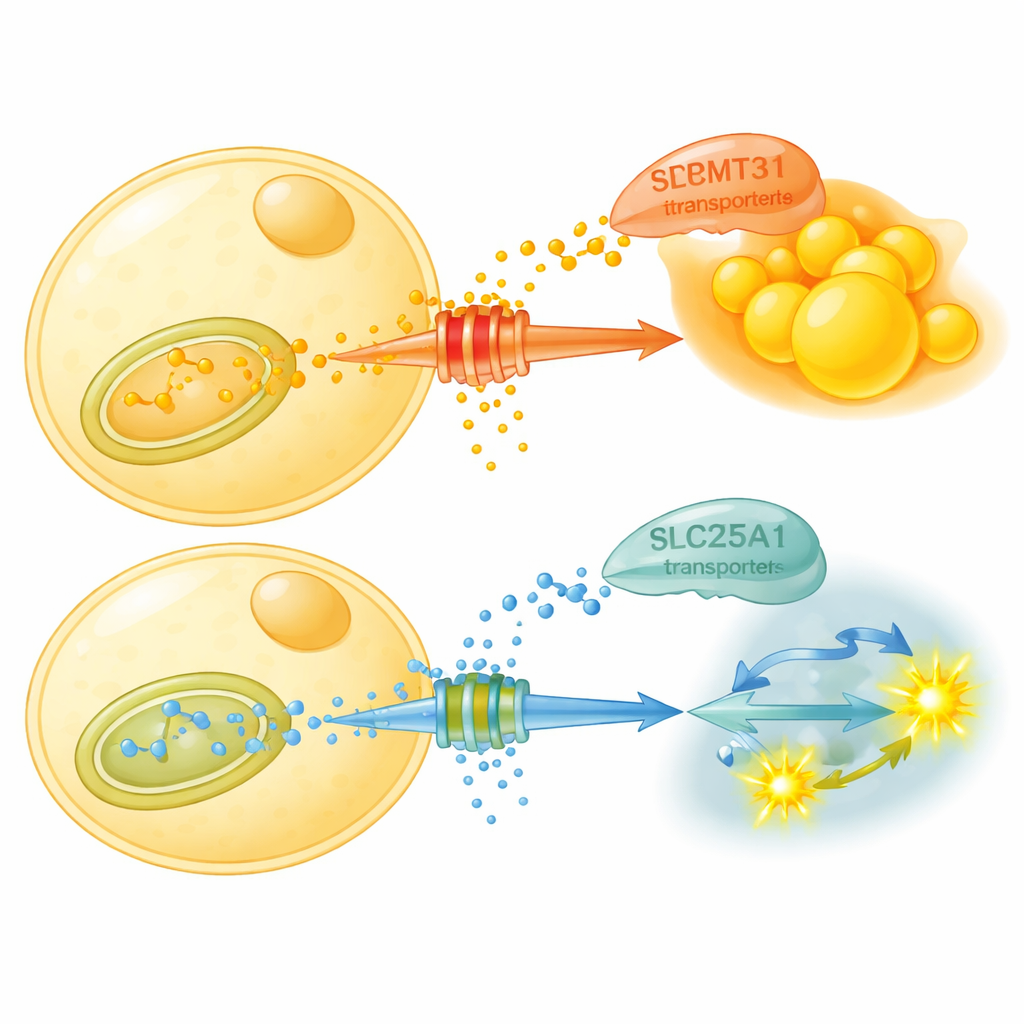
Los horarios de ayuno y los ajustes genéticos apuntan a la misma vía
Los investigadores preguntaron después si los patrones comunes de ayuno usan este mismo interruptor. Bajo un régimen de alimentación con tiempo restringido 16:8—16 horas de ayuno y 8 horas de ingesta—los ratones perdieron peso y manejaron mejor la glucosa sin comer menos en total. Su grasa visceral mostró niveles más bajos de PRMT3, SLC25A1 y proteínas metiladas, y su uso de combustible se volvió más flexible, especialmente por la noche cuando normalmente comen. De manera notable, administrar el fármaco que bloquea PRMT3 en momentos específicos del día produjo muchos de los mismos beneficios que el horario 16:8. Eliminar genéticamente SLC25A1 solo en las células grasas también protegió a los ratones de la hiperglucemia y la esteatosis hepática inducidas por la dieta, de nuevo impulsando la degradación de azúcares y el gasto energético en la grasa, incluso sin reducir la masa grasa.
Qué significa esto para futuras terapias
En conjunto, los hallazgos sugieren que la grasa abdominal profunda contiene un interruptor sensible al tiempo, controlado por la insulina, AKT, PRMT3 y SLC25A1, que determina si nuestros cuerpos se mantienen metabólicamente ágiles o se bloquean en un modo de almacenamiento. La alimentación con tiempo restringido parece empujar este interruptor hacia la flexibilidad al disminuir PRMT3 y sus efectos posteriores. Un fármaco que inhibe PRMT3 puede reproducir muchas de estas ventajas en ratones obesos, lo que insinúa una posible medicina futura que haga más accesibles los beneficios metabólicos del ayuno. Para los lectores cotidianos, el mensaje es que cuándo comemos, no solo qué comemos, puede remodelar cómo nuestro tejido graso maneja el combustible—con consecuencias importantes para el peso, el azúcar en sangre y la salud a largo plazo.
Cita: Huang, Z., Liu, X., Chen, X. et al. PRMT3-mediated post-translational adaptation to fasting regulates metabolic flexibility. Nat Commun 17, 2264 (2026). https://doi.org/10.1038/s41467-026-68883-6
Palabras clave: flexibilidad metabólica, alimentación con tiempo restringido, grasa visceral, metilación de proteínas, metabolismo de la glucosa