Clear Sky Science · es
Un nanodispositivo basado en ADN detecta la señalización purinérgica y promueve un interruptor inmune para resolver la inflamación
Apagar el sistema de alarma del cuerpo
Cuando nuestros tejidos resultan dañados, las células liberan una oleada de “señales de alarma” químicas que reclutan células inmunitarias para combatir infecciones y eliminar restos. Esta respuesta es vital, pero si la alarma suena con demasiada fuerza o durante demasiado tiempo, puede impulsar una inflamación dañina en pulmones, riñones y otros órganos. Este estudio describe un diminuto dispositivo programable basado en ADN que puede detectar cuándo la señal de alarma es excesiva y reducirla discretamente, ayudando al sistema inmune a pasar del modo de ataque al modo de reparación.
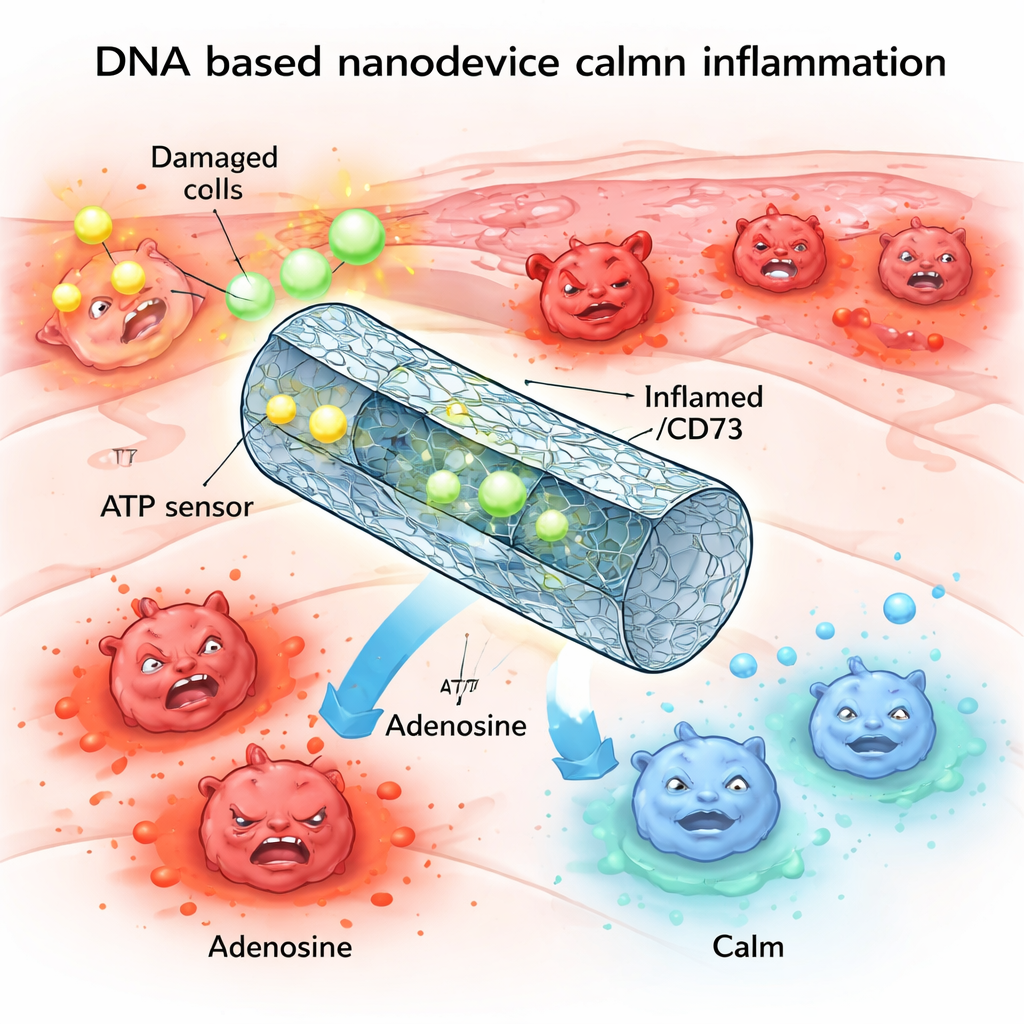
Una alarma química que puede ir demasiado lejos
Una de las moléculas de alarma clave del cuerpo es el ATP, más conocida como la “moneda energética” dentro de las células. Durante una lesión o estrés, grandes cantidades de ATP se filtran desde las células dañadas al espacio circundante. Allí, este ATP extracelular actúa como una señal de auxilio, uniéndose a receptores en las células inmunitarias y llevándolas hacia un estado altamente inflamatorio. En condiciones sanas, enzimas en las superficies celulares descomponen rápidamente el exceso de ATP hasta adenosina, una molécula relacionada que tiene un efecto calmante y antiinflamatorio. Pero en muchas enfermedades inflamatorias crónicas o graves, esta maquinaria de degradación está dañada, dejando niveles altos de ATP, adenosina baja y los tejidos atascados en un ciclo de daño.
Construyendo un tubo inteligente de ADN
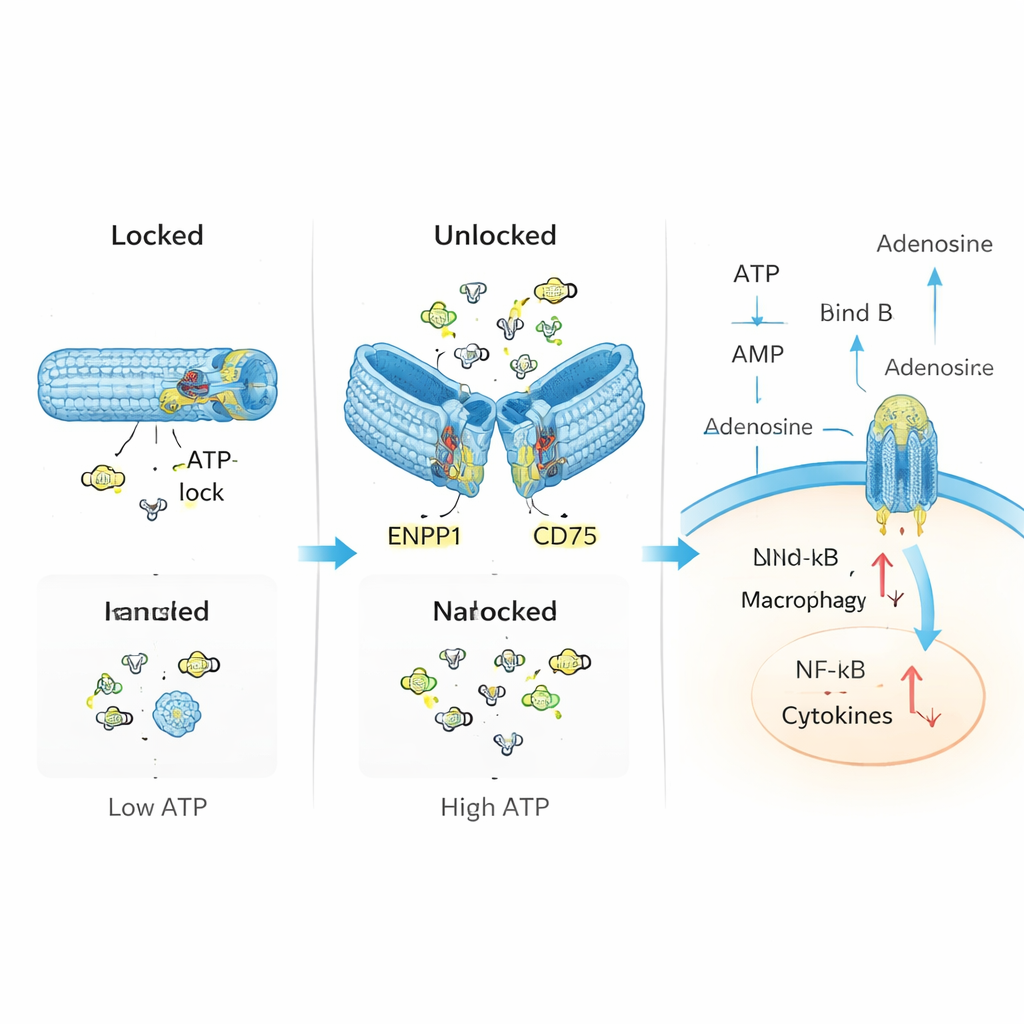
Los investigadores se propusieron imitar y reparar este sistema de control natural usando nanotecnología de ADN. Construyeron un tubo hueco de ADN, plegado de forma similar al origami, y lo equiparon con dos componentes principales: “sensores” que reconocen el ATP y enzimas que convierten ATP en adenosina. En su estado de reposo, bloqueado, el tubo se mantiene cerrado por segmentos cortos de ADN que funcionan también como sensores de ATP. Cuando los niveles de ATP superan un umbral típico de tejidos lesionados, el ATP se une a estos segmentos, provocando que el tubo se abra y exponga en su interior las enzimas ENPP1 y CD73. Estas luego degradan el exceso de ATP y generan adenosina, desplazando con suavidad el equilibrio químico local de peligro hacia resolución.
Demostrando que el interruptor funciona
En pruebas de laboratorio controladas, el equipo confirmó que su tubo de ADN permanece cerrado a bajos niveles de ATP pero se abre de forma fiable cuando el ATP es abundante, de manera similar a una válvula de emergencia. Una vez desbloqueado, el dispositivo convierte de forma sostenida ATP en productos intermedios y finalmente en adenosina, sin perjudicar notablemente la actividad de las enzimas. En células inmunitarias expuestas a alto ATP, este nanodispositivo redujo los subproductos tóxicos en las mitocondrias, disminuyó la activación de vías inflamatorias como NF-κB y el inflamasoma NLRP3, y potenció señales asociadas con las acciones calmantes de la adenosina. En otras palabras, el dispositivo hizo más que eliminar ATP; reconfiguró activamente el comportamiento celular de inflamatorio a regulador.
Viajando hasta los sitios de lesión
Diseñar un interruptor inteligente es una cosa; llevarlo al lugar correcto del cuerpo es otra. Para resolver este problema de entrega, los investigadores unieron sus tubos de ADN a la superficie de monocitos circulantes, un tipo de glóbulo blanco que de forma natural se dirige a tejidos inflamados. Usando un anclaje de ADN ligado a colesterol, “aparcaron” gran número de nanodispositivos en la membrana de cada célula, donde los dispositivos permanecieron mayormente en la superficie en lugar de ser internalizados por la célula. En modelos murinos de lesión aguda de pulmón y riñón, estos monocitos decorados se acumularon en órganos dañados con mucha más eficiencia que los dispositivos libres, y los nanodispositivos siguieron respondiendo de forma específica al ATP alto en el tejido lesionado.
Ayudando a que los tejidos reparen
En ratones con lesiones pulmonares o renales inducidas químicamente, el tratamiento con el dispositivo de ADN redujo el daño tisular, la acumulación de células inmunitarias y las moléculas mensajeras inflamatorias. La versión transportada por monocitos fue la más eficaz, ofreciendo una protección mayor que el dispositivo libre o las enzimas por sí solas. Análisis genéticos y metabólicos más profundos del tejido pulmonar mostraron que este enfoque no solo atenuó genes inflamatorios sino que también ayudó a restaurar el metabolismo energético alterado en las células. Es importante que los dispositivos mostraron baja toxicidad y no desencadenaron reacciones inmunes nocivas en animales sanos.
Por qué esto importa para terapias futuras
Para un público no especializado, el mensaje clave es que este trabajo demuestra un “termostato” molecular programable para la inflamación. Construido a partir de ADN y enzimas naturales, el nanodispositivo detecta cuando una señal de peligro es demasiado intensa y la convierte automáticamente en una señal calmante, ayudando a que las células inmunitarias se calmen y los tejidos se reparen. Aunque aún está en una etapa experimental temprana, esta estrategia sugiere una nueva clase de tratamientos que no se limitan a bloquear rutas inmunes en todo el cuerpo, sino que reequilibran localmente las señales químicas en los sitios de lesión, ofreciendo potencialmente un control más preciso sobre la inflamación dañina en múltiples enfermedades.
Cita: Li, W., Liu, S., Zhou, X. et al. A DNA-based nanodevice senses purinergic signaling and drives an immune switch for resolving inflammation. Nat Commun 17, 2030 (2026). https://doi.org/10.1038/s41467-026-68879-2
Palabras clave: nanodispositivo de ADN, ATP extracelular, inflamación, señalización por adenosina, nanomedicina