Clear Sky Science · es
La inmunoterapia anti-TLR2 modula la propagación de α-sinucleína de neuronas a oligodendrocitos en modelos de ratón y humanos
Por qué importa esta investigación
La atrofia de sistemas múltiples (ASM) es un trastorno cerebral infrecuente pero de rápida progresión que combina problemas de movimiento similares a los del Parkinson con fallos del equilibrio y del sistema autónomo, como caídas de la presión arterial. Los médicos pueden aliviar los síntomas, pero hoy por hoy no pueden frenar la enfermedad en sí. Este estudio revela cómo una proteína mal plegada se propaga entre las células cerebrales para dañar el “aislamiento de los cables” del cerebro y muestra que un tratamiento con anticuerpos dirigido puede interrumpir ese proceso en modelos celulares y animales. El trabajo apunta a una estrategia concreta, farmacológica, que algún día podría cambiar el curso de la ASM en lugar de limitarse a tratar sus síntomas.
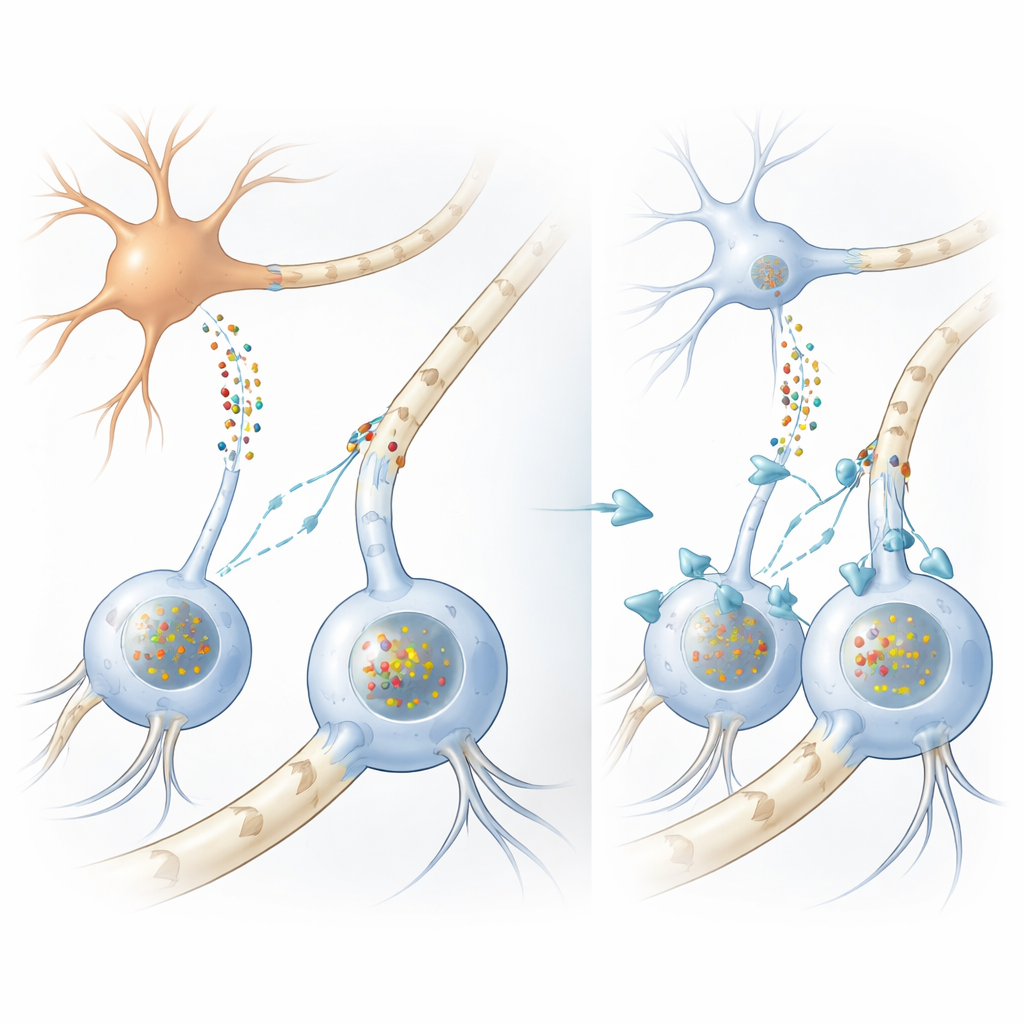
Cómo falla el cableado cerebral
En muchos trastornos del movimiento, incluido el Parkinson, se acumulan depósitos de una proteína llamada alfa-sinucleína dentro de las neuronas. En la ASM, sin embargo, los acúmulos más llamativos se forman dentro de células de soporte llamadas oligodendrocitos, que normalmente envuelven las fibras nerviosas con vainas grasas de mielina que aceleran las señales eléctricas. Curiosamente, los oligodendrocitos producen muy poca alfa-sinucleína por sí mismos, lo que deja un enigma de larga data: ¿de dónde proceden los enormes depósitos proteicos en estas células? Los autores confirmaron primero, usando muestras de cerebro humano y análisis de ARN a gran escala, que los oligodendrocitos efectivamente generan mucha menos alfa-sinucleína que las neuronas, reforzando la idea de que la proteína dañina debe llegar desde el exterior.
Proteína transferida de la neurona a la célula de soporte
Para probarlo, el equipo construyó varios modelos complementarios. En cultivos, hicieron crecer células humanas con aspecto de oligodendrocitos a partir de células madre neurales y las expusieron a medio recogido de células con aspecto neuronal que habían sido diseñadas para liberar grandes cantidades de alfa-sinucleína. Las células de soporte captaron esta proteína y desarrollaron acúmulos que se parecían mucho a las inclusiones gliales vistas en cerebros con ASM, con las mismas marcas químicas y proteínas accesorias. Cuando los investigadores examinaron una cepa de ratón que produce alfa-sinucleína humana mutante solo en las neuronas, volvieron a encontrar depósitos de la proteína humana dentro de oligodendrocitos en la materia blanca, a pesar de que esas células no expresaban el gen humano. En conjunto, estos experimentos demuestran que la alfa-sinucleína puede moverse de las neuronas a los oligodendrocitos y formar allí inclusiones similares a las de la enfermedad.
La puerta en la superficie celular
A continuación, los científicos se preguntaron cómo la proteína entra en los oligodendrocitos. Trabajos previos habían identificado al sensor inmune Toll-like receptor 2 (TLR2) en la superficie celular como un punto de acoplamiento de la alfa-sinucleína en neuronas y microglía. Al analizar conjuntos de datos de expresión génica de cerebros con ASM, el equipo encontró que los oligodendrocitos de los pacientes presentaban niveles inusualmente altos de TLR2 en comparación con controles, y que un mayor TLR2 se asociaba con niveles más bajos de genes relacionados con la mielina, como la proteína básica de la mielina. Esta relación no aparecía en varios conjuntos de datos independientes de Parkinson, sugiriendo que la sensibilidad de los oligodendrocitos a la alfa-sinucleína vía TLR2 es una característica distintiva de la ASM más que un rasgo general de todos los trastornos por sinucleína.
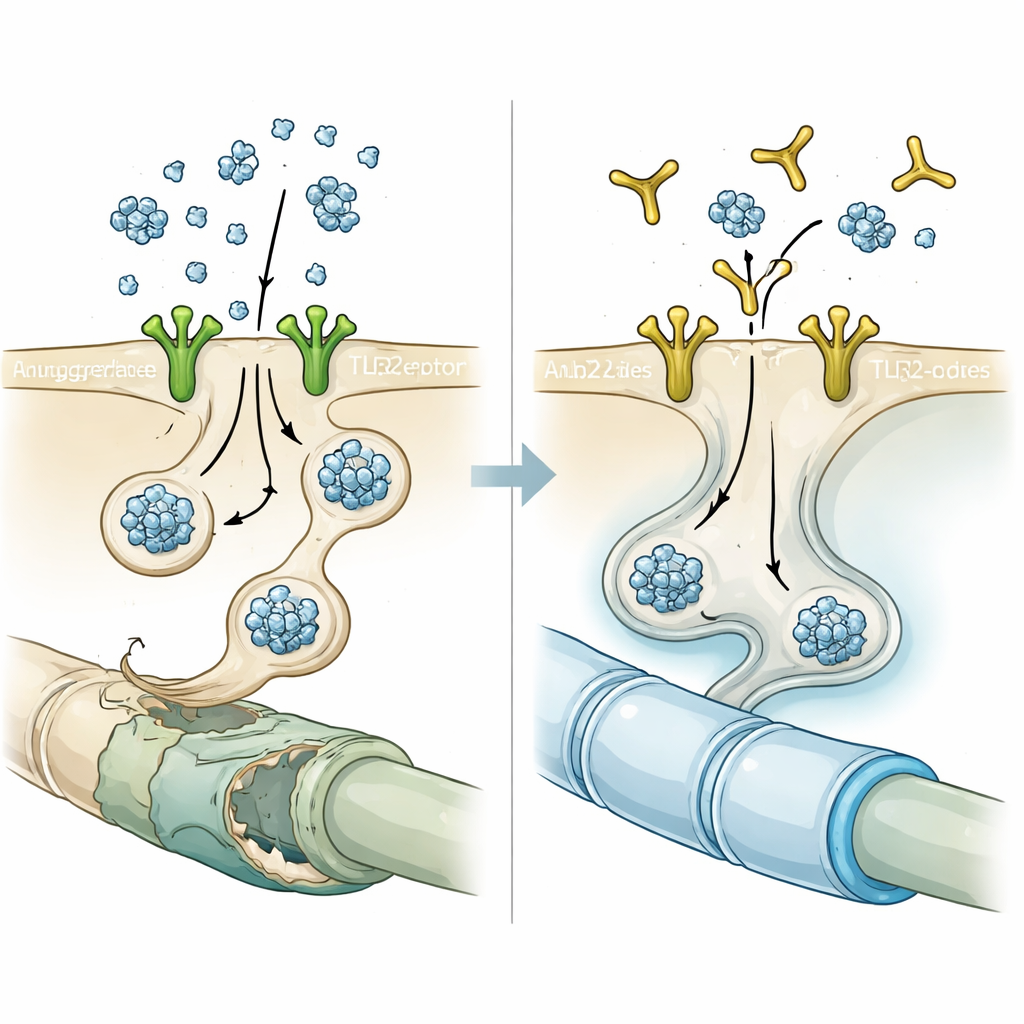
Bloquear la puerta con un anticuerpo
Con esta pista, los investigadores probaron NM-101, un anticuerpo diseñado para unirse a TLR2 y evitar su activación. En cultivos celulares, un pretratamiento breve de los oligodendrocitos con NM-101 antes de añadir la alfa-sinucleína derivada de neuronas redujo drásticamente el número y la intensidad de los acúmulos tipo inclusión. En ratones que sobreproducían alfa-sinucleína neuronal o que recibieron inyecciones de fibrillas de alfa-sinucleína preformadas, infusiones semanales de NM-101 disminuyeron la proteína agregada en la materia blanca, atenuaron las respuestas inflamatorias de microglía y astrocitos, y redujeron la activación de una enzima inflamatoria llamada caspasa-1 dentro de los oligodendrocitos. Los animales tratados vivieron más y rindieron mejor en pruebas motoras, lo que sugiere que los efectos protectores del anticuerpo fueron funcionalmente significativos y no solo curiosidades microscópicas.
Rescatando el aislamiento dañado
Puesto que los oligodendrocitos son los productores de mielina del cerebro, el equipo examinó si la transferencia de alfa-sinucleína dañaba la mielina y si bloquear TLR2 podía ayudar. La secuenciación de ARN a nivel de célula única de oligodendrocitos derivados de humanos expuestos a alfa-sinucleína en medio condicionado por neuronas reveló cambios amplios: pérdida del estado maduro productor de mielina y desplazamiento hacia un perfil más inmaduro, parecido a progenitores, con muchos genes clave de la mielina reprimidos. Estudios paralelos de expresión génica en oligodendrocitos capturados mediante microdisección láser de pacientes con ASM y del modelo murino mostraron una firma compartida: reducción de la expresión de genes implicados en la formación y el mantenimiento de la mielina. Bajo el microscopio electrónico, la materia blanca de los ratones con alfa-sinucleína mostraba vainas de mielina más delgadas y desorganizadas. El tratamiento con NM-101 revirtió muchos de estos cambios, engrosando la mielina, restaurando los niveles de proteínas de la mielina y normalizando la expresión de genes necesarios para la maduración de los oligodendrocitos.
Qué significa todo esto para futuros tratamientos
El estudio respalda una narrativa clara: en la ASM, la alfa-sinucleína producida por las neuronas puede propagarse a los oligodendrocitos a través de TLR2 en su superficie, donde se acumula, desencadena inflamación, descarrila el programa de desarrollo de las células y erosiona el recubrimiento de mielina del cableado cerebral. Al bloquear TLR2 con un anticuerpo dirigido, los investigadores pudieron interrumpir esta cadena de acontecimientos en ratones y modelos celulares humanos, reduciendo las inclusiones tóxicas, calmando la inflamación, reparando la mielina y mejorando la supervivencia y el movimiento. Aunque el NM-101 aún requiere ensayos rigurosos en personas, el trabajo establece la transferencia proteica dependiente de TLR2 como un impulsor central de la patología similar a la ASM y destaca la inmunoterapia anti-TLR2 como una estrategia prometedora para ralentizar o prevenir esta devastadora enfermedad.
Cita: Bae, EJ., Ham, S., Jeong, Y.W. et al. Anti-TLR2 immunotherapy modulates neuron-to-oligodendrocyte propagation of α-synuclein in mouse and human models. Nat Commun 17, 2175 (2026). https://doi.org/10.1038/s41467-026-68870-x
Palabras clave: atrofia de sistemas múltiples, alfa-sinucleína, oligodendrocitos, daño de la mielina, inmunoterapia