Clear Sky Science · es
Olig2 actúa como una barrera inducible para la conversión in vivo de astrocitos en neuronas
Convertir las células de soporte del cerebro en neuronas
El cerebro adulto tiene una capacidad limitada para reemplazar neuronas perdidas, lo que constituye un obstáculo importante en enfermedades como el accidente cerebrovascular, el Alzheimer y las lesiones medulares. Una idea prometedora es convertir directamente las células vecinas de “soporte” denominadas astrocitos en nuevas neuronas mediante terapia génica. Este estudio plantea una pregunta clave: ¿qué impide que esa conversión funcione con eficacia dentro del cerebro vivo y pueden liberarse esos frenos?
Un freno oculto en la transformación celular
Los astrocitos normalmente ayudan a nutrir las neuronas, mantener la química cerebral y responder a las lesiones. En ciertos estados patológicos, pueden comportarse de forma algo similar a células madre, lo que alimenta la esperanza de que puedan reprogramarse in situ en neuronas. Los científicos ya saben que una clase de genes llamada factores de transcripción proneurales —como Ngn2, Ascl1 y NeuroD1— puede empujar a los astrocitos hacia una identidad neuronal. Sin embargo, en animales, esta conversión de astrocitos a neuronas sigue siendo frustrantemente ineficiente. Los autores sospecharon que, más allá de las defensas preexistentes, los astrocitos podrían activar una nueva barrera inducible cuando se desencadena la reprogramación.
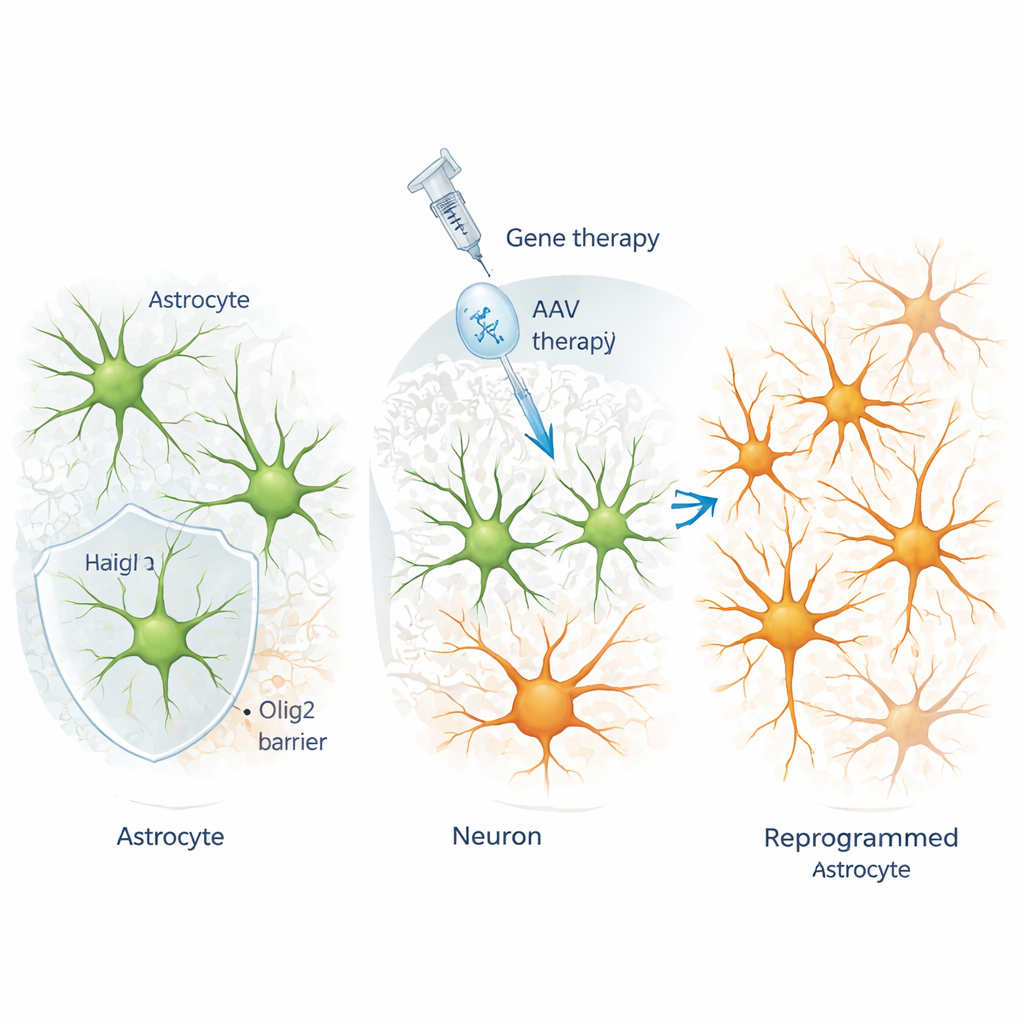
Una proteína llamada Olig2 interviene para resistir el cambio
Trabajando en la corteza de ratón adulto, los investigadores entregaron factores de reprogramación a astrocitos usando virus diseñados que son altamente selectivos para estas células. Descubrieron que siempre que un factor bHLH (hélice–bucle–hélice) como Ngn2, Ascl1 o NeuroD1 se forzaba en astrocitos, otra proteína bHLH, Olig2, se activaba de forma muy marcada. En condiciones normales, Olig2 se encuentra en células de la línea de oligodendrocitos, no en astrocitos corticales maduros. Experimentos de trazado cuidadosos mostraron que las células adicionales positivas para Olig2 tras el tratamiento no procedían de la proliferación de precursores de oligodendrocitos; en cambio, los propios astrocitos objetivo de la conversión estaban activando Olig2 en respuesta a la señal de reprogramación.
Eliminar el freno triplica la conversión y produce neuronas funcionantes
Para probar si Olig2 es realmente una barrera, el equipo utilizó ARN de horquilla corta para reducir específicamente Olig2 en astrocitos a los que también se les proporcionó Ngn2. Silenciar Olig2 redujo sus niveles proteicos en estas células casi hasta cero y tuvo un efecto llamativo: la proporción de astrocitos marcados que se convirtieron en neuronas aumentó aproximadamente tres veces en comparación con Ngn2 solo. A lo largo de varias semanas, muchas células pasaron por una etapa intermedia, perdiendo marcadores típicos de astrocitos antes de adquirir plenamente marcadores neuronales. Registros eléctricos en cortes cerebrales mostraron que las células convertidas disparaban potenciales de acción y, en aproximadamente la mitad de los casos, recibían entradas sinápticas excitadoras e inhibidoras —rasgos indicativos de integración funcional en circuitos locales.
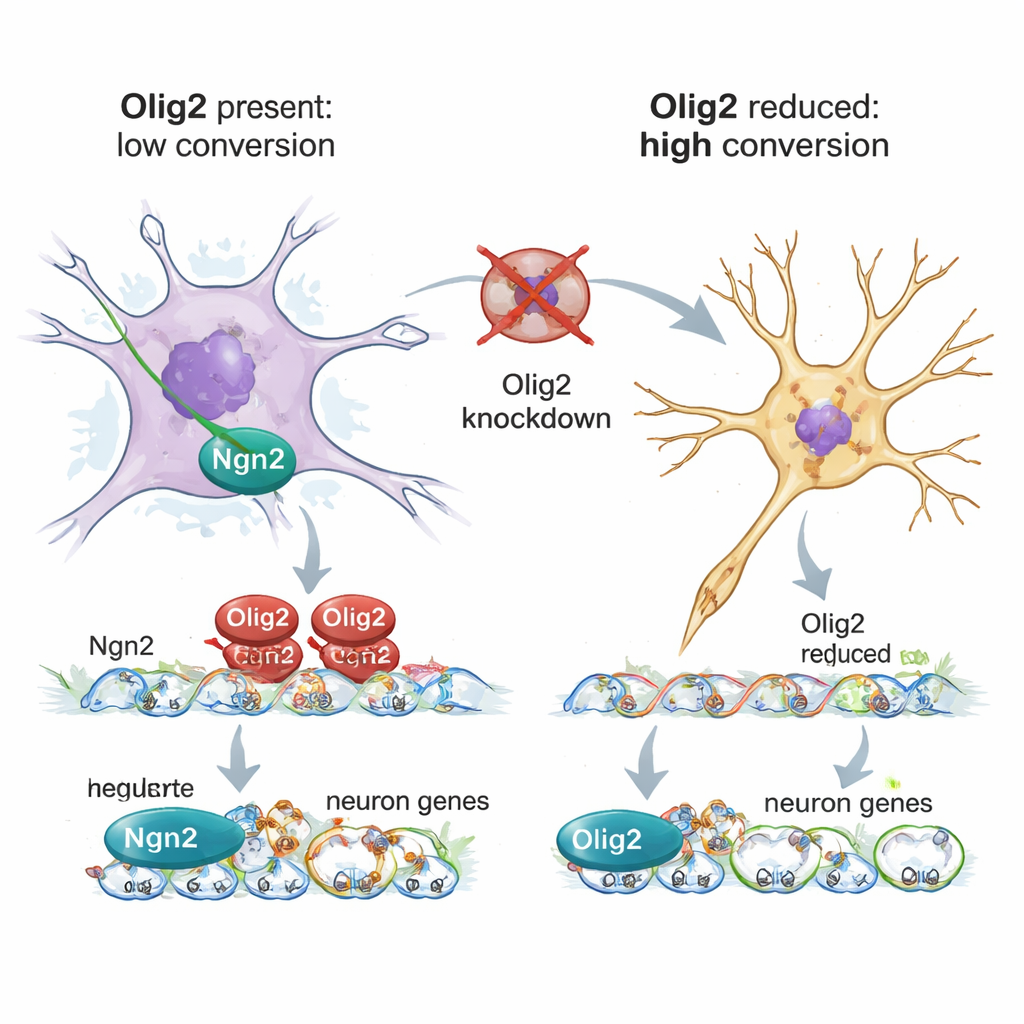
Cómo Olig2 bloquea el cambio hacia el programa neuronal
Mediante secuenciación de ARN unicelular, los autores perfilaron miles de astrocitos individuales expuestos a Ngn2, con o sin reducción de Olig2. Cuando Olig2 estaba presente, los astrocitos solo cambiaban parcialmente su expresión génica: algunas vías metabólicas y de síntesis proteica se alteraban, pero los genes centrales de astrocitos permanecían activos y muchos genes necesarios para construir neuronas seguían silenciados. Cuando Olig2 se redujo, los astrocitos suprimieron con mayor firmeza su programa de célula de soporte madura y aumentaron la expresión de genes asociados con células madre neurales, neurogénesis y crecimiento axonal. Un método complementario, CUT&Tag, mapeó dónde se une Olig2 en el ADN de estos astrocitos reprogramados. Olig2 se localizó en regiones reguladoras de muchos genes proneurogénicos —incluido el propio Ngn2—, coherente con un papel como represor directo que tanto atenúa el factor de reprogramación como mantiene apagados los genes neuronales.
Reconectar la identidad celular levantando una defensa inducible
En conjunto, el trabajo revela que los astrocitos montan una defensa activa e inducible contra ser transformados en neuronas: una vez que se introduce un factor proneural como Ngn2, este activa Olig2, que a su vez restringe a Ngn2 y bloquea genes neuronales clave. Desactivar Olig2 no resuelve todos los problemas —las eficiencias de conversión siguen siendo modestas—, pero aumenta sustancialmente el rendimiento de nuevas neuronas funcionales y desplaza el metabolismo y la expresión génica de los astrocitos hacia un estado similar al neuronal. Para el lector no especializado, la conclusión es que la reparación cerebral exitosa puede requerir no solo pisar el acelerador con factores proneuronales, sino también liberar frenos recién descubiertos como Olig2 que las células usan para proteger su identidad.
Cita: Lai, C., Hou, K., Li, W. et al. Olig2 acts as an inducible barrier to in vivo astrocyte-to-neuron conversion. Nat Commun 17, 2033 (2026). https://doi.org/10.1038/s41467-026-68869-4
Palabras clave: conversión de astrocitos a neuronas, reprogramación celular, Olig2, terapia génica, neuroregeneración