Clear Sky Science · es
La evolución coordinada de familias génicas moldea el genoma de los Mucorales dimórficos
Un hongo, dos cuerpos
Algunos hongos pueden vivir una doble vida, alternando entre una forma unicelular tipo “levadura” y una forma ramificada tipo “moho”. Esta capacidad para cambiar de forma les ayuda a sobrevivir en ambientes cambiantes y, en ciertos casos, a invadir tejidos humanos. El estudio resumido aquí revela cómo un grupo de estos hongos, los Mucorales, reorganiza y utiliza sus genes para sostener ambos estilos de vida dentro de un único genoma.
Por qué importan los hongos cambiformes
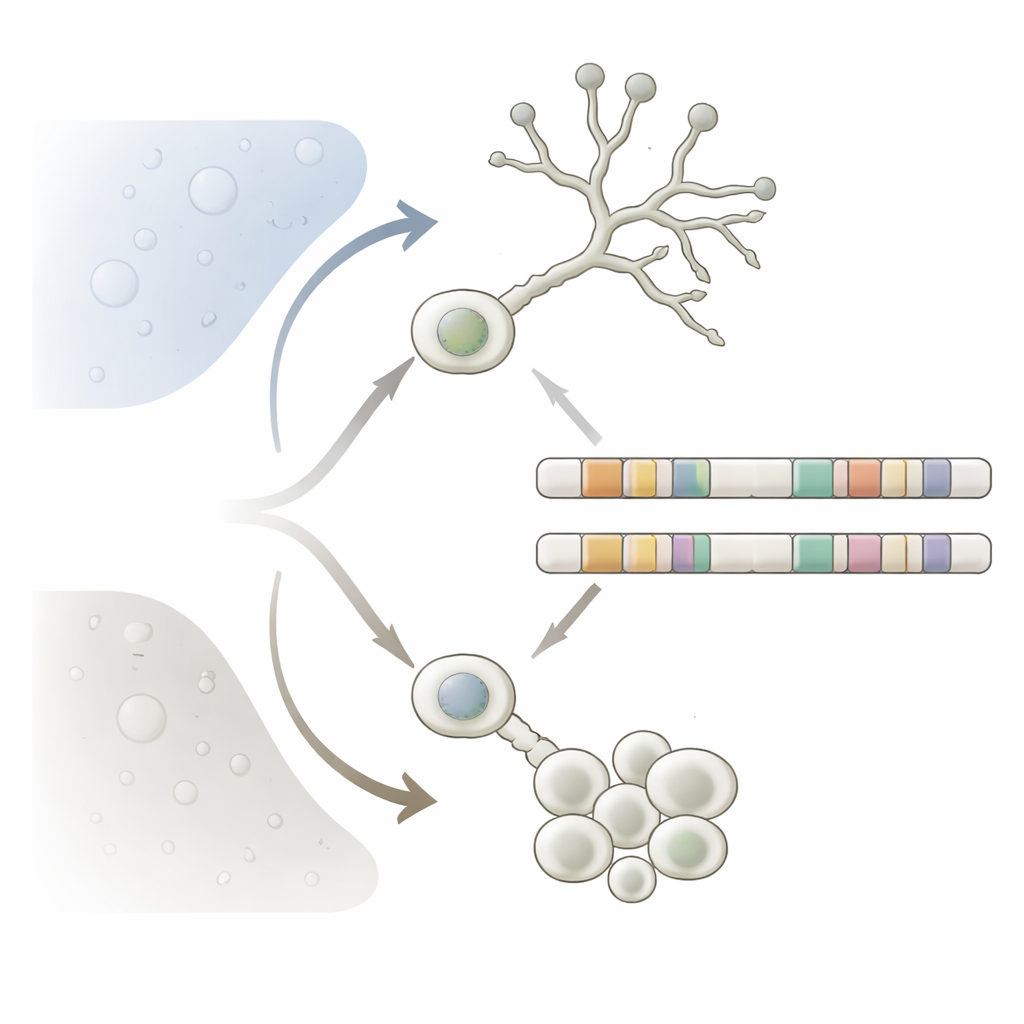
Los hongos dimórficos son relevantes no solo para la ecología sino también para la salud humana. En los Mucorales, la forma de levadura está compuesta por células redondas aisladas que favorecen condiciones con poco oxígeno y ricas en azúcares y crecen por gemación. La forma micelial forma filamentos largos que prosperan en ambientes ricos en oxígeno y pueden invadir tejidos y superficies. En varias especies de Mucorales, solo la forma filamentosade es fuertemente infecciosa, causando mucormicosis, una enfermedad grave en personas con sistemas inmunitarios debilitados. Entender cómo estos hongos cambian de forma puede revelar por qué son tan adaptables, por qué resisten algunos fármacos y qué rasgos genéticos distinguen a las especies dimórficas peligrosas de sus parientes inofensivos.
Un genoma diseñado para el cambio
Los autores se centraron en el hongo modelo Mucor lusitanicus y lo siguieron a través de cuatro etapas: levadura, micelio temprano, el retroceso hacia levadura y micelio maduro. Secuenciando ARN, midieron qué genes estaban activos en cada estado. Hallaron que cerca del 70% de todos los genes cambian su actividad durante el cambio de forma, mucho más que en muchos otros hongos. Las células de levadura tienden a activar genes para el metabolismo básico y la síntesis de componentes celulares, mientras que los micelios favorecen genes implicados en señalización interna y el citoesqueleto, que soporta el crecimiento filamentoso. Esta amplia reprogramación muestra que el dimorfismo no es un ajuste menor sino una reconfiguración a nivel de todo el organismo.
Genes duplicados con funciones divididas
Un hallazgo clave es que muchos genes aparecen en pares o pequeñas familias cuyas copias se han especializado en una u otra forma. El equipo revisó primero un ejemplo conocido: dos genes ferroxidasa y dos genes transportadores de hierro que, en conjunto, importan hierro, un nutriente vital. Un miembro de cada par se usa en la levadura y el otro en el micelio. Eliminar las copias específicas de la levadura debilitó el crecimiento en ese estado pero dejó en gran medida intacto el crecimiento micelial, y lo contrario ocurrió con las copias miceliales. Extendiéndose a todo el genoma, los investigadores identificaron 490 de esas “familias dimórficas” en las que al menos una copia es específica de la levadura y otra del micelio. En conjunto, aproximadamente uno de cada nueve genes del genoma pertenece a dichas familias, abarcando muchos roles celulares distintos. Esto sugiere que, en lugar de depender de una única versión de una proteína para funcionar en todos los contextos, el hongo ha evolucionado versiones gemelas ajustadas a las condiciones muy diferentes de la vida líquida y con poco oxígeno de la levadura frente a la vida sólida y rica en oxígeno del micelio.
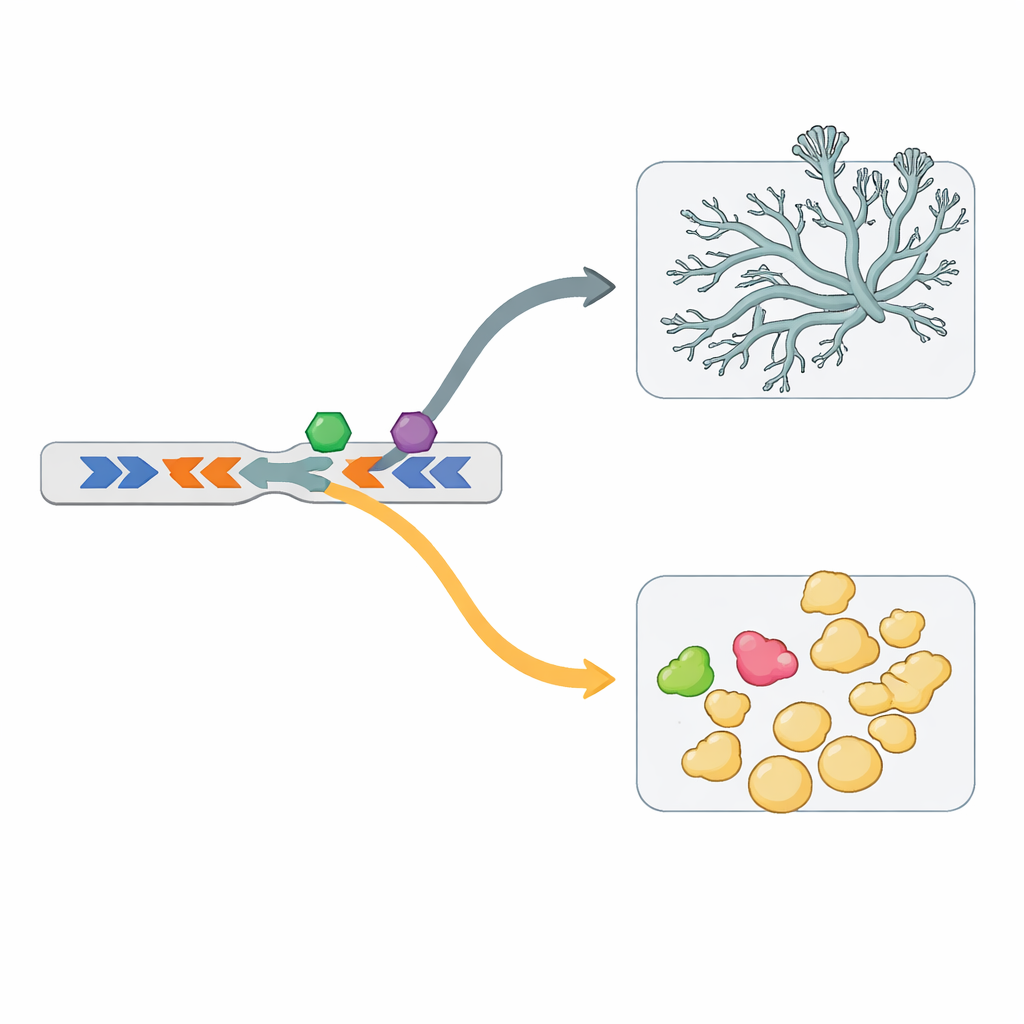
Genes cara a cara y nuevos interruptores de control
El genoma no solo duplica genes, sino que también los dispone en configuraciones especiales. Muchos de los genes de importación de hierro, por ejemplo, se sitúan en pares “cara a cara”: dos genes colocados en direcciones opuestas que comparten una región de control central. Un par así está activo en la levadura y el par vecina lo está en el micelio. Intercambiar experimentalmente estas regiones de control compartidas invirtió el momento en que se activaba cada gen, demostrando que esta disposición funciona como un interruptor coordinado. Un análisis de todo el genoma encontró más de mil pares cara a cara de este tipo, con cientos implicados en el dimorfismo. Las regiones de control compartidas para los pares vinculados a levadura y micelio llevan motivos de ADN distintos, lo que implica que son leídos por factores reguladores diferentes.
Reguladores maestros y pistas evolutivas
Para encontrar esos reguladores, los investigadores usaron el ADN de control compartido de los genes de importación de hierro como cebo para captar proteínas que se unen allí. Identificaron dos proteínas previamente no caracterizadas, denominadas DFL y DKL, y crearon cepas mutantes que carecían de cada una. Estos mutantes mostraron una alteración marcada en el cambio de forma: los mutantes en DKL ya no podían formar levadura, y ambos mutantes perdieron el patrón normal de activación génica a lo largo de miles de genes relacionados con el dimorfismo. Al comparar especies emparentadas, el equipo observó que los Mucorales dimórficos tienden a conservar familias génicas duplicadas específicas de la forma, estructuras cara a cara y el gen dfl, mientras que hongos cercanamente relacionados que no cambian de forma suelen carecer de estos rasgos. Este patrón sugiere que estos rasgos genómicos evolucionaron conjuntamente como un kit de herramientas para el dimorfismo y pueden servir como marcadores para predecir qué especies probablemente sean cambiantes de forma.
Qué significa esto para las enfermedades fúngicas
En términos sencillos, este trabajo muestra que los hongos Mucorales han reconstruido sus genomas en torno al desafío de vivir dos vidas separadas. Lo resuelven duplicando genes importantes, afinando una copia para la levadura y la otra para el micelio, conectando muchos de ellos en unidades de control cara a cara y usando reguladores dedicados para coordinar qué versión se utiliza en cada momento. Dado que la forma invasiva y causante de enfermedad suele ser el micelio, y porque algunos de los genes afectados gestionan la captación de hierro y la sensibilidad a fármacos, estos hallazgos apuntan a nuevas maneras de predecir qué hongos pueden volverse peligrosos y a diseñar tratamientos que interrumpan su capacidad de cambiar de forma.
Cita: Tahiri, G., Navarro-Mendoza, M.I., Lax, C. et al. Coordinated gene family evolution shapes the genome of dimorphic Mucorales. Nat Commun 17, 2148 (2026). https://doi.org/10.1038/s41467-026-68866-7
Palabras clave: dimorfismo fúngico, Mucorales, duplicación génica, regulación del genoma, patogénesis fúngica