Clear Sky Science · es
Apilamiento antiparalelo de pili Csu impulsa el montaje tridimensional del biofilm de Acinetobacter baumannii
Cómo los gérmenes hospitalarios construyen ciudades protegidas
Algunos de los gérmenes hospitalarios más resistentes sobreviven a los antibióticos refugiándose en comunidades viscosas y tridimensionales llamadas biófilms. Este estudio plantea una pregunta simple pero crucial: ¿cómo se unen las bacterias individuales para formar estructuras tan resistentes y estratificadas? Al aumentar la resolución con microscopios electrónicos avanzados, los investigadores descubrieron un “velcro” microscópico formado por filamentos pilosos que permite al patógeno peligroso Acinetobacter baumannii tejerse en agregados protectores en 3D. Comprender este andamiaje oculto podría abrir nuevas vías para deshacer los biófilms y mejorar la eficacia de los fármacos existentes.
Pelillos diminutos que mantienen unidas a las bacterias
A. baumannii, una causa principal de infecciones hospitalarias difíciles de tratar, está cubierta de finos pelos superficiales llamados pili Csu. Trabajos anteriores mostraron que estos pili son esenciales para formar biófilms robustos en forma de cúpula, pero nadie sabía cómo tejían las células en una estructura tridimensional. Usando varias técnicas de microscopía electrónica, los autores confirmaron primero que en cultivo líquido los pili suelen sobresalir por separado de cada bacteria, como púas de una bardana. Sin embargo, en colonias densas sobre superficies la imagen cambia drásticamente: muchos pili se empaquetan estrechamente, formando bandas anchas y planas que se extienden entre células vecinas, creando una malla extensa y de apariencia delicada en tres dimensiones. 
Escaleras planas construidas a partir de filamentos emparejados
Para entender cómo se forman estas bandas, el equipo purificó los pili Csu y observó su comportamiento aislado. A lo largo de días o semanas, filamentos individuales comenzaron a emparejarse y luego a fusionarse en "superpilas" multifilamento, formando finalmente una red tipo gel que reproducía de cerca las estructuras vistas en biófilms reales. La crio-microscopía electrónica de alta resolución reveló el diseño subyacente. Cada pilus no es un tubo liso, sino una varilla en zigzag. Cuando dos varillas yacen lado a lado en direcciones opuestas, se tocan en puntos de esquina repetidos, formando uniones laterales estables. Muchas de estas parejas antiparalelas pueden alinearse luego en una pila muy delgada en forma de lámina —esencialmente una escalera microscópica o una cinta que tiene un solo filamento de espesor pero muchos filamentos de ancho.
Un plano de construcción incorporado para el crecimiento 3D
Las estructuras detalladas muestran que esta capacidad de apilamiento está codificada en la geometría de los propios pili. El patrón en zigzag se repite en una distancia muy corta, creando muchos puntos de contacto potenciales a lo largo de cada filamento. Como resultado, una vez que dos pili se encuentran en la orientación correcta, puede formarse una cadena de uniones como una cremallera, extendiendo rápidamente la lámina. Es importante que la orientación de las varillas hace que los contactos se formen habitualmente entre pili de células diferentes, no de la misma, lo que promueve de forma natural la unión célula–célula. Las pilas permanecen flexibles y elásticas, de modo que el biófilm en crecimiento puede absorber esfuerzos físicos sin romperse. Los investigadores observaron que durante la división celular, las células hijas a menudo acaban con sus pili enfrentados, lo que favorece la formación de pilas exactamente donde se necesita para atar las células en un grupo 3D. 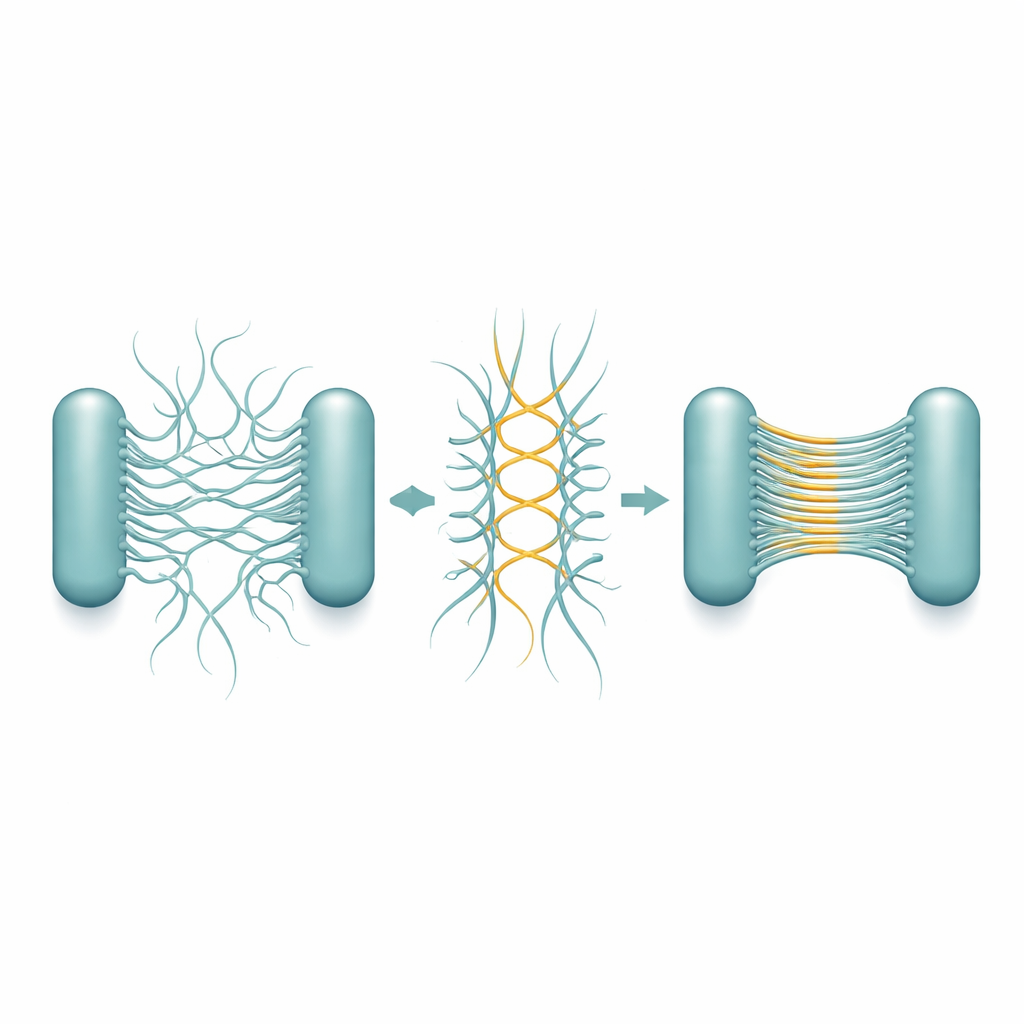
Adhesivo, relleno y andamiaje inicial
El estudio también examinó cómo contribuyen otros componentes del biófilm. Un polímero azucarado llamado PNAG y ADN suelto procedente de células rotas se sabe que se acumulan en biófilms maduros. La microscopía reveló estas sustancias llenando las estrechas hendiduras entre bacterias y envolviendo las pilas de pili, de manera similar al hormigón vertido alrededor de barras de acero. Aun así, cuando el equipo eliminó PNAG y ADN, las bacterias siguieron formando balsas organizadas mantenidas únicamente por las pilas de pili Csu. Esto muestra que los pili construyen el andamiaje primario, mientras que el material circundante lo cementa y estabiliza posteriormente.
Nuevos puntos débiles en las fortalezas bacterianas
En términos sencillos, este trabajo explica cómo A. baumannii utiliza sus pelos superficiales para entrelazarse en racimos resistentes y multicapa que los fármacos y las células inmunitarias tienen dificultades para penetrar. Los pili actúan primero como ganchos para agarrar superficies y luego como correas flexibles que se apilan en láminas planas, ligando a las células vecinas en todas las direcciones. Polímeros azucarados y ADN llenan después los huecos, convirtiendo esta red de correas en una fortaleza sólida. Al localizar precisamente la forma en que los pili se adhieren entre sí, el estudio señala un nuevo blanco: fármacos o moléculas que bloqueen los contactos pilus–pilus podrían debilitar los andamios del biófilm desde dentro, facilitando la eliminación de infecciones bacterianas persistentes.
Cita: Malmi, H., Pakharukova, N., Paul, B. et al. Antiparallel stacking of Csu pili drives Acinetobacter baumannii 3D biofilm assembly. Nat Commun 17, 2508 (2026). https://doi.org/10.1038/s41467-026-68860-z
Palabras clave: biófilms, Acinetobacter baumannii, pili, resistencia a antibióticos, crio-microscopía electrónica