Clear Sky Science · es
Detección temprana del destino celular aberrante y la reparación mediante células progenitoras circulantes en pacientes con osificación heterotópica
Cuando crece hueso donde no debería
A veces, tras una lesión grave o una cirugía de articulación, el hueso comienza a crecer dentro de músculos y otros tejidos blandos donde no pertenece. Esta condición, denominada osificación heterotópica, puede inmovilizar articulaciones, causar dolor intenso y hacer que los movimientos cotidianos sean casi imposibles. Los médicos hoy en día la detectan solo después de que el hueso aberrante ya se ha establecido, cuando es demasiado tarde para evitarlo. Este estudio plantea una pregunta sencilla pero potente: ¿podría una extracción de sangre rutinaria avisarnos con semanas de antelación de que este hueso oculto se está formando?
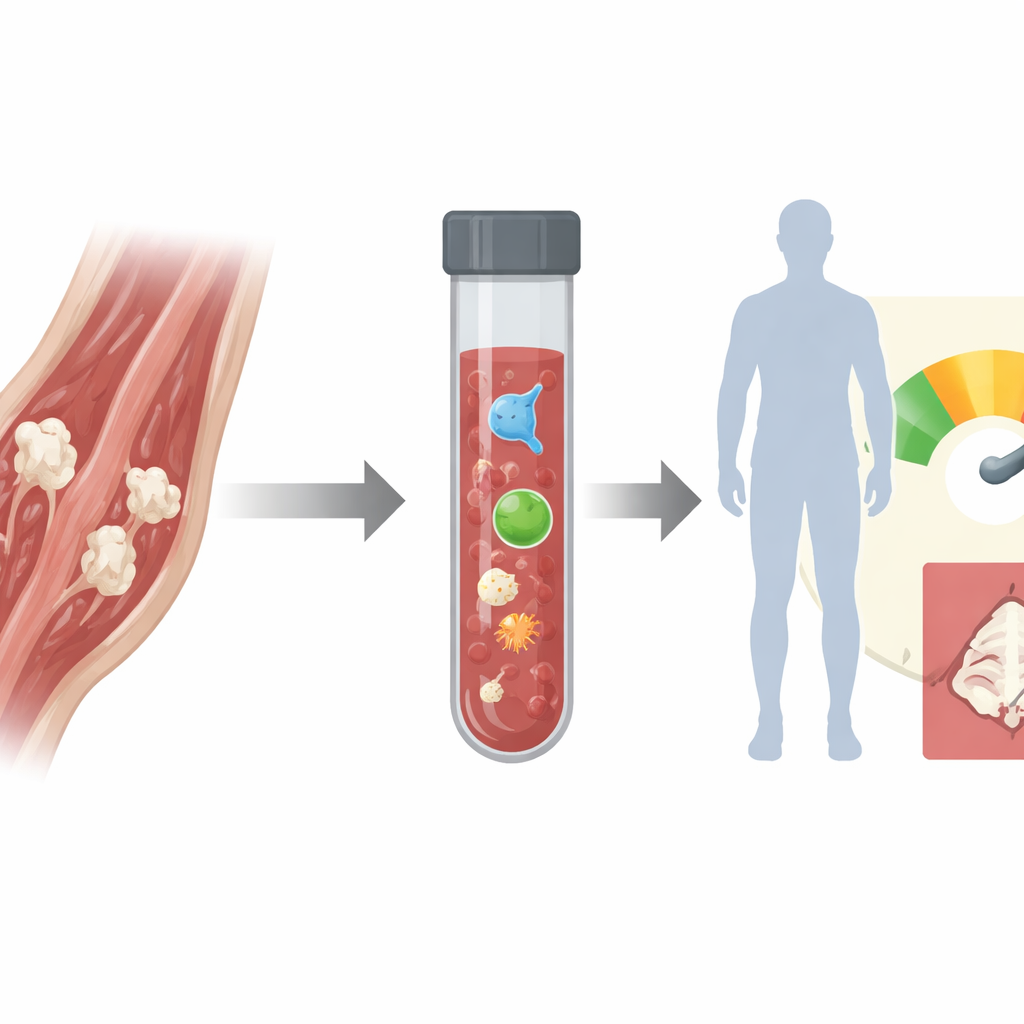
Una amenaza oculta tras lesiones y cirugías
La osificación heterotópica es sorprendentemente frecuente después de quemaduras graves, explosiones en combate, fracturas y, en especial, de las cirugías de reemplazo de cadera. Sin embargo, las herramientas actuales—radiografías, tomografías computarizadas y gammagrafías óseas—solo la detectan a las seis a ocho semanas, cuando el hueso nuevo ya está maduro. Existen tratamientos preventivos, como la radioterapia o fármacos antiinflamatorios potentes, pero tienen efectos secundarios graves y suelen administrarse de manera amplia porque no podemos saber quién los necesita realmente ni cuándo empezar o detenerlos. Como resultado, muchos pacientes reciben medicamentos arriesgados innecesariamente o pierden la ventana estrecha en la que esos fármacos podrían impedir que se forme hueso adicional.
Siguiendo células reparadoras raras en la sangre
El equipo de investigación se centró en un grupo especial de células reparadoras llamadas células progenitoras mesenquimales, que normalmente ayudan a reconstruir el hueso y el tejido conectivo. Tras ciertas lesiones, un número muy pequeño de estas células se filtra en el torrente sanguíneo. Utilizando un dispositivo microfluídico—un chip que puede separar células que fluyen por canales estrechos—los científicos pescaban estas raras células progenitoras mesenquimales circulantes de muestras de sangre de ratones y de pacientes sometidos a reemplazo de cadera. Descubrieron que, apenas horas después de una lesión que más tarde causaría hueso heterotópico, estas células circulantes muestran un patrón distintivo de genes activos que difiere tanto de las células sanguíneas normales como de la sangre tomada tras lesiones que no conducen a hueso adicional.
Convertir patrones génicos en una prueba de advertencia temprana
Al comparar la sangre de pacientes que sí y que no desarrollaron osificación heterotópica, y al correlacionar esos hallazgos con estudios detallados en ratones, el equipo identificó un conjunto de 32 genes que actúan en conjunto como una “huella” molecular de la formación ósea dañina. Luego emplearon algoritmos de aprendizaje automático para entrenar un modelo predictivo que se fija únicamente en los niveles de actividad de estos genes en las células progenitoras circulantes. En las muestras humanas, esta prueba basada en sangre identificó correctamente hasta el 90 por ciento de los casos futuros mientras evitaba falsas alarmas en todos los pacientes que permanecieron sanos. De forma notable, la firma génica apareció tan pronto como seis horas tras la cirugía o el trauma—más de un mes antes de que las imágenes estándar puedan detectar hueso nuevo.
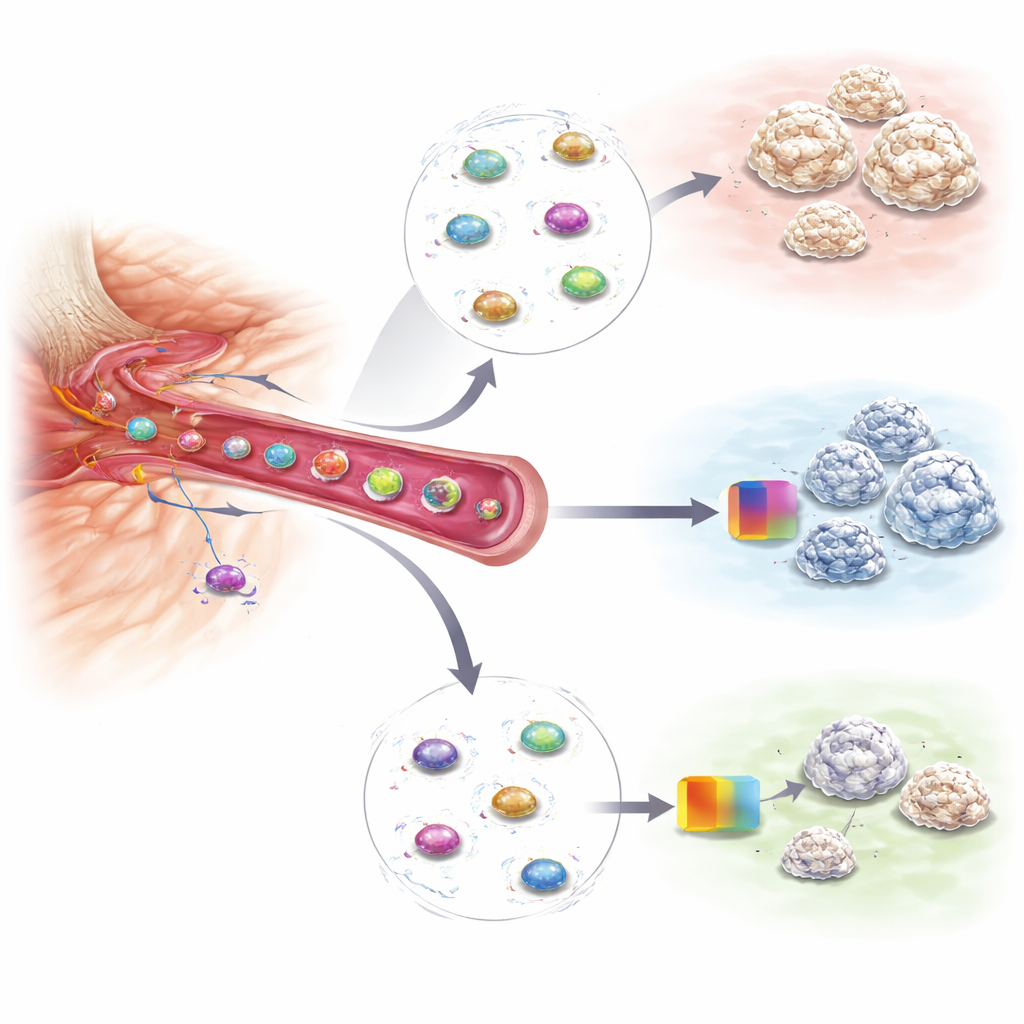
Comprobar si los tratamientos funcionan realmente
El mismo enfoque basado en sangre también demostró ser útil para monitorizar la terapia. En un modelo murino, los investigadores trataron animales lesionados con un fármaco que bloquea una enzima implicada en el endurecimiento de la matriz tisular y que se sabe que reduce la osificación heterotópica. Cuando el tratamiento fue efectivo, la firma génica en las células progenitoras circulantes descendió bruscamente, y los animales desarrollaron luego parches de hueso adicional mucho más pequeños. Otros tipos de lesiones que no provocan osificación heterotópica, como daños musculares o traumatismos craneales, no mostraron el mismo aumento en estas células ni en su patrón génico, lo que subraya la especificidad de la prueba. Esto sugiere que extracciones de sangre repetidas podrían tanto señalar a los pacientes de alto riesgo como revelar, casi en tiempo real, si un tratamiento preventivo está cumpliendo su objetivo.
Qué podría significar esto para los pacientes
En conjunto, los hallazgos apuntan a un futuro en el que una prueba sanguínea simple podría guiar una atención altamente personalizada tras lesiones graves o cirugías articulares. En lugar de tratar a todos por igual, los clínicos podrían identificar a las personas cuyas células reparadoras tienden a formar hueso en el lugar equivocado, iniciar terapias preventivas de manera temprana y detenerlas una vez que la firma génica peligrosa desaparezca. Más allá de la osificación heterotópica, biopsias líquidas similares de células reparadoras circulantes podrían ayudar a los médicos a seguir otras condiciones en las que la reparación tisular falla, como la artritis o la fibrosis. Para los pacientes, eso podría traducirse en menos complicaciones, cursos más cortos de medicamentos arriesgados y una mayor probabilidad de mantener la movilidad y vivir sin dolor.
Cita: Nunez, J., Holtz, M., Korlakunta, S. et al. Early detection of aberrant cell fate and repair using circulating progenitor cells in patients with heterotopic ossification. Nat Commun 17, 2231 (2026). https://doi.org/10.1038/s41467-026-68857-8
Palabras clave: osificación heterotópica, biopsia líquida, células progenitoras mesenquimales, reemplazo articular, diagnóstico precoz