Clear Sky Science · es
Degradación del electrodo negativo inducida por el electrodepositado de zinc en dos etapas y su recuperación en baterías de zinc
Por qué las baterías de zinc importan en la vida cotidiana
Almacenar electricidad de forma segura y económica es esencial para todo, desde respaldar paneles solares domésticos hasta estabilizar la red eléctrica. Las baterías de metal‑zinc son candidatas atractivas: el zinc es abundante, no tóxico y funciona en electrólitos acuosos mucho más seguros que los líquidos inflamables de muchas baterías de litio. Sin embargo, estas baterías prometedoras todavía se degradan y cortocircuitan con demasiada rapidez. Este artículo revela un proceso oculto de crecimiento en dos etapas en el electrodo de zinc que causa ese daño, y presenta una estrategia química de “autorreparación” que mantiene las baterías funcionando durante mucho más tiempo.
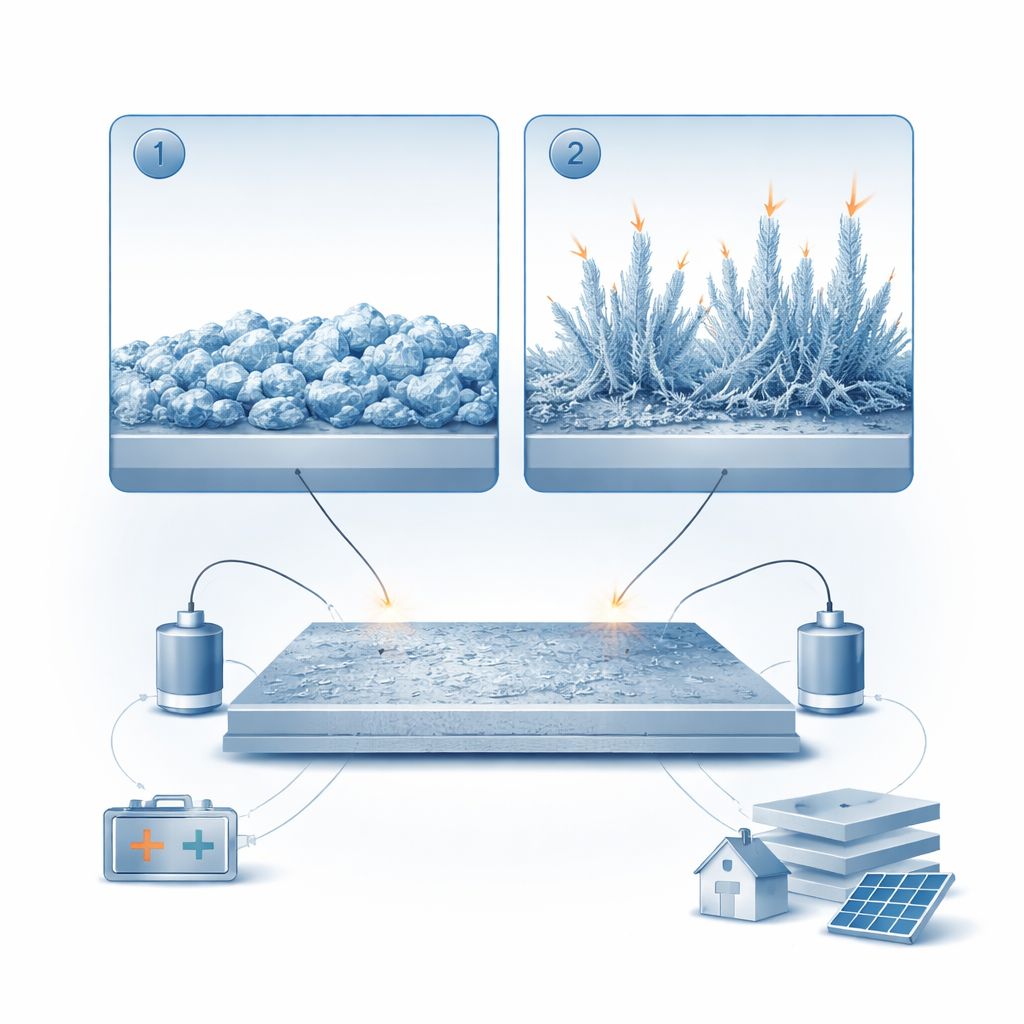
Del metal liso al “musgo” de zinc
El electrodo negativo en estas baterías está hecho de zinc metálico, que se deposita (añade zinc) y se disuelve (quita zinc) repetidamente durante la carga y descarga. Usando una celda transparente equipada con microscopio, los investigadores observaron cómo se acumula el zinc en una superficie metálica con el tiempo. Descubrieron que el zinc no crece de una sola manera sino en dos etapas distintas. Primero forma cristales relativamente densos y grumosos que crean una capa brillante y compacta. Luego, a medida que continúa el electrodepositado, surgen estructuras delgadas y filiformes desde bordes y puntas afiladas. Esta segunda etapa, de zinc “musgoso”, llena el espacio entre electrodos y acaba por conectarlos, lo que pone en riesgo cortocircuitos internos.
Cómo el zinc musgoso se vuelve zinc muerto
El equipo combinó imágenes directas, microscopía electrónica y simulaciones por ordenador para entender por qué aparece esta capa musgosa. Las protuberancias afiladas del zinc grumoso concentran el campo eléctrico—un efecto similar al de los pararrayos que concentran la descarga eléctrica. Esa concentración atrae más iones de zinc hacia las puntas, alimentando un crecimiento rápido en forma de pelos. Durante el proceso inverso, cuando el zinc se disuelve, los filamentos musgosos se disuelven primero y pueden perder contacto eléctrico con el metal subyacente. Lo que queda es zinc “muerto”: pequeños fragmentos eléctricamente aislados que ya no participan en la reacción de la batería pero que aún contienen material activo valioso, lo que provoca pérdida de capacidad y superficies rugosas e inestables.
Diseñando un electrolito más inteligente
Sabiendo que el crecimiento musgoso proviene de una acumulación local de iones en sitios salientes, los investigadores diseñaron un aditivo para el electrolito que ataca tanto la formación de zinc musgoso como el zinc muerto que genera. Usaron una sal llamada acetilcolina yoduro, que aporta un catión orgánico cargado positivamente y un anión yoduro en la misma molécula. Según medidas de masa sensibles y espectroscopía infrarroja, los cationes se adsorben de forma fuerte y selectiva en la superficie del zinc, formando una fina capa cargada positivamente que uniformiza el flujo de iones de zinc. Esto favorece un electrodepositado liso y plano en lugar del crecimiento filamentoso, manteniendo la superficie compacta y más resistente a la corrosión y a la formación de gas hidrógeno.
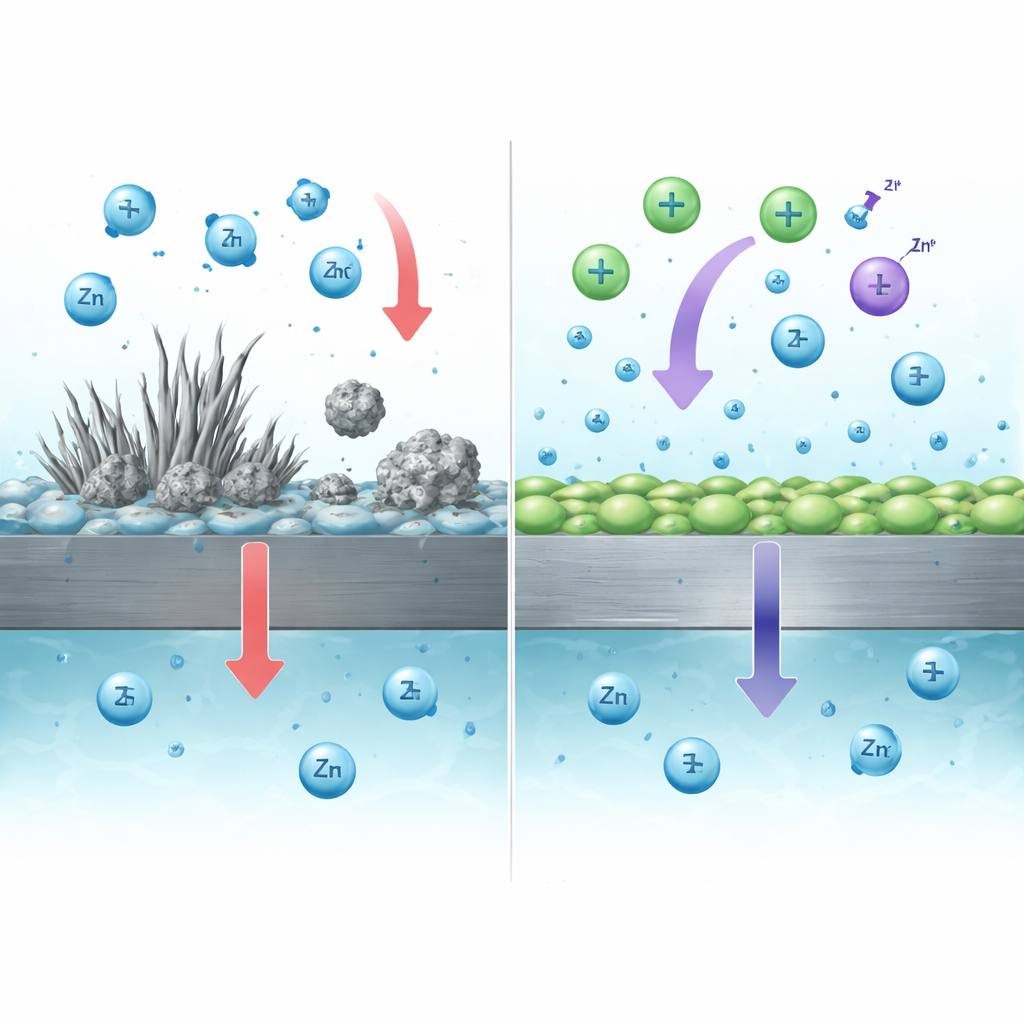
Reavivar el zinc perdido para alargar la vida útil
La porción de yoduro del aditivo desempeña un papel diferente pero complementario. Durante la carga, el yoduro se convierte parcialmente en una especie oxidante suave (I3−) que puede reaccionar con partículas de zinc muerto y con subproductos aislantes que contienen zinc que se forman en la superficie. Estas reacciones convierten el zinc eléctricamente aislado de nuevo en iones de zinc disueltos, que luego pueden volverse a depositar en el electrodo en ciclos posteriores. Los experimentos mostraron que el zinc muerto inmerso en una solución que contenía yodo se disolvió casi hasta el grado teórico esperado, y las celdas completas que usaron el aditivo de doble ión recuperaron más carga de la que sería posible con el zinc recién depositado solamente—una evidencia clara de que el zinc previamente perdido se estaba “reciclando” dentro de la batería.
Qué significa esto para las baterías reales
Al combinar cationes que suavizan el campo con un anión que recicla zinc, el nuevo electrolito permitió electrodos de zinc con una eficiencia coulómbica media de alrededor del 99,7 % y una operación estable durante más de 1.400 horas a corrientes y capacidades altas—condiciones relevantes para el almacenamiento a escala de red. Celdas simétricas de zinc y celdas prácticas tipo pouch zinc‑yodo mantuvieron bajas pérdidas de voltaje y retuvieron más del 96 % de su capacidad tras cientos a decenas de miles de ciclos, según la prueba. Para un lector no especializado, el mensaje clave es que los investigadores han identificado exactamente cómo se degradan los electrodos de zinc—mediante un crecimiento musgoso en dos etapas que produce metal muerto—y han demostrado una receta química que tanto previene esta estructura dañina como revive el material perdido. Este enfoque dual acerca mucho más las baterías de zinc seguras y a base de agua a un uso duradero y a gran escala en hogares y redes eléctricas.
Cita: Gan, H., Liu, D., Zhang, Y. et al. Negative electrode degradation induced by two-stage zinc plating and its recovery in zinc batteries. Nat Commun 17, 2067 (2026). https://doi.org/10.1038/s41467-026-68844-z
Palabras clave: baterías de metal de zinc, degradación del electrodo, zinc tipo musgo, aditivos de electrolito, almacenamiento de energía en red