Clear Sky Science · es
Respuestas cGAS-IFN-I al extraer ADN nuclear de células moribundas mediante nucleocitosis
Cómo nuestro sistema inmunitario lee el ADN de los muertos
Cuando nuestras células mueren durante infecciones, cáncer o por el desgaste cotidiano, sus restos deben limpiarse sin provocar demasiada inflamación. Este artículo revela una forma sorprendente en la que las células inmunitarias pueden literalmente perforar los núcleos de las células moribundas, extraer su ADN y usarlo como una señal de peligro. Comprender este sistema oculto de limpieza y alarma podría cambiar nuestra visión sobre fármacos antivirales, autoinmunidad, terapia contra el cáncer y efectos secundarios de medicamentos.
Una alarma de ADN oculta dentro de las células inmunitarias
Nuestras células contienen un sensor llamado cGAS que detecta ADN en el lugar equivocado: flotando en el citoplasma en lugar de estar protegido en el núcleo o las mitocondrias. Cuando cGAS encuentra ese ADN, activa un potente programa de alarma que produce interferones tipo I, proteínas clave en la defensa antiviral y la regulación inmunitaria. Los científicos sabían que los virus pueden introducir su material genético en las células para activar esta vía, y que fragmentos de nuestro propio ADN a veces pueden filtrarse y causar enfermedades autoinmunes. Pero quedaba una pregunta básica: ¿cómo llega una gran cantidad de nuestro propio ADN, sobre todo el procedente de células muertas, hasta cGAS sin ser simplemente digerida en los “estómagos” celulares llamados lisosomas?
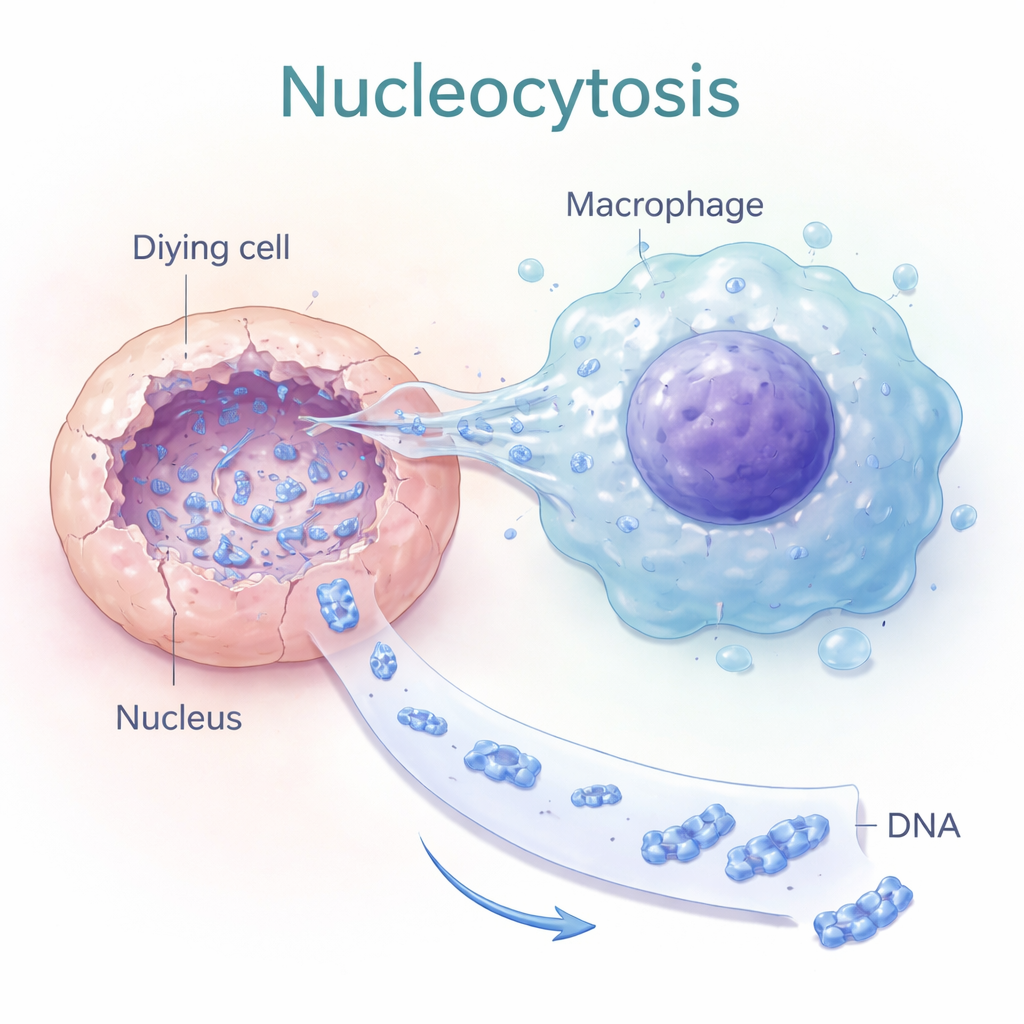
Nucleocitosis: perforando los núcleos de células muertas
Los autores descubrieron un proceso que llaman “nucleocitosis”, en el que ciertos macrófagos—células inmunitarias que normalmente engullen desechos—hacen algo mucho más dirigido. En lugar de tragarse una célula muerta entera, extienden finas protrusiones en forma de dedos directamente hacia el núcleo de la célula moribunda. Imágenes de células vivas mostraron que la intensidad del ADN disminuía dentro del núcleo de la célula muerta mientras aumentaba dentro del macrófago adherido, lo que indica una extracción activa de ADN nuclear. Esta transferencia dependía del esqueleto interno de la célula (actina) y de moléculas de señalización que controlan la forma celular, lo que sugiere que la nucleocitosis es un comportamiento mecánico intencionado, no una fuga pasiva.
Cuando los fármacos antivirales activan la alarma del ADN
Durante la pandemia de COVID-19, fármacos como la hidroxicloroquina se probaron ampliamente como antivirales, aunque sus acciones precisas en el organismo seguían siendo poco claras. Los investigadores hallaron que la hidroxicloroquina y varios fármacos relacionados, denominados “anfifílicos catiónicos”, pueden activar con fuerza la vía cGAS–STING–interferón—pero solo en una subpoblación de macrófagos. Estos compuestos alteran los lisosomas elevando su pH y bloqueando una enzima llamada PPT1, que ayuda a degradar etiquetas lipídicas en proteínas. El efecto combinado empuja a algunas células hacia una forma especial de muerte en la que una proteína llamada calreticulina se acumula en el núcleo. Los macrófagos, a su vez, tienden a extender protrusiones hacia estos núcleos ricos en calreticulina, extraen ADN mediante nucleocitosis y desencadenan una producción intensa de interferón en apenas unas pocas células—suficiente para crear una señal antiviral local fuerte sin inundar todo el organismo.
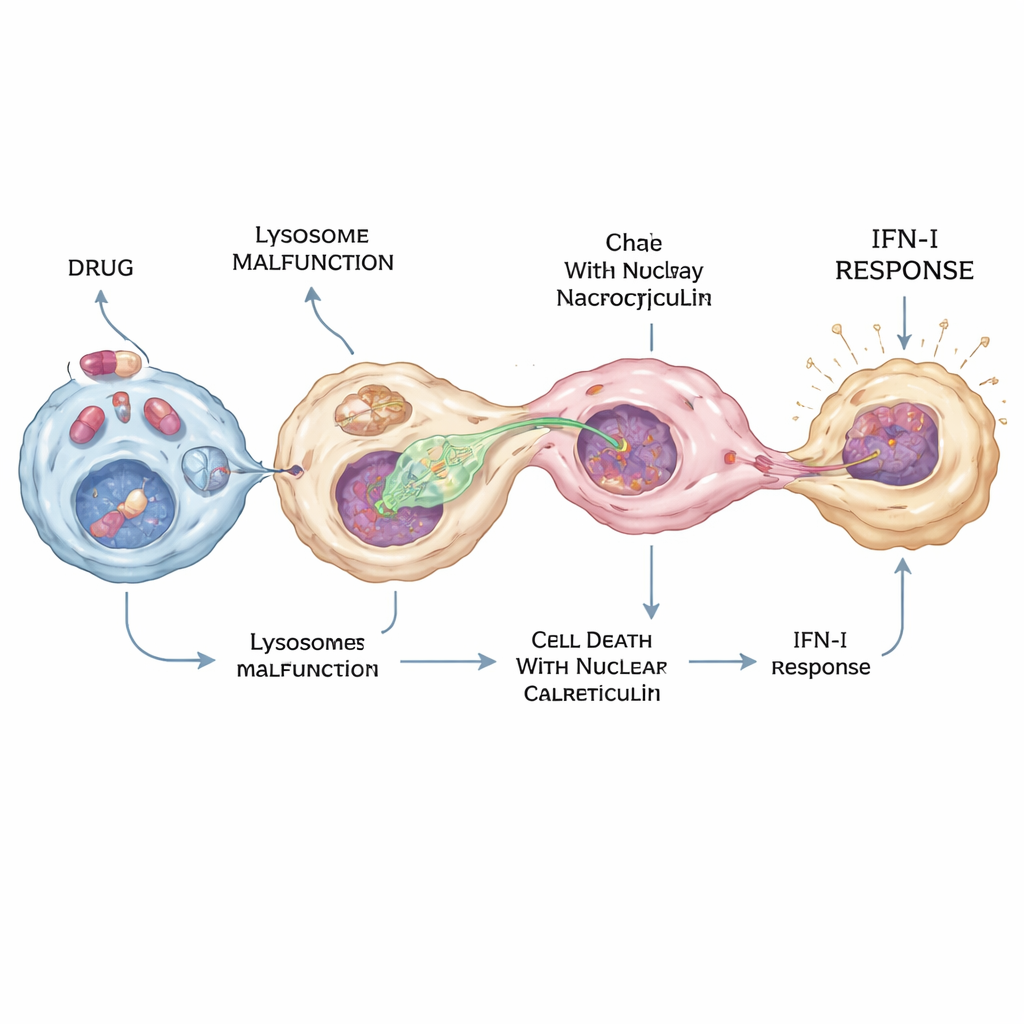
De la defensa local a la enfermedad y los efectos secundarios
Al estudiar cultivos celulares y pulmones de ratón, el equipo demostró que los macrófagos tratados con fármacos pueden desencadenar una respuesta de interferón dependiente de STING que permanece en gran medida local—por ejemplo, en el pulmón—en lugar de volverse sistémica. Esto ayuda a explicar por qué fármacos como la hidroxicloroquina podrían mostrar beneficios antivirales o antitumorales en algunos tejidos, pero también por qué pueden causar efectos secundarios específicos en órganos, como toxicidad ocular o cardíaca con uso prolongado. El mismo proceso de nucleocitosis podría contribuir plausiblemente a enfermedades autoinmunes o inflamatorias siempre que coincidan células muertas y estrés lisosomal, porque ofrece una vía directa para que el ADN propio active la alarma de cGAS.
Por qué esto importa para tratamientos futuros
Para un público no especialista, el mensaje clave es que las células inmunitarias no se limitan a engullir pasivamente las células muertas; pueden extraer activamente el ADN de sus núcleos y usarlo como señal para pedir refuerzos. Esta vía de nucleocitosis explica cómo nuestro propio ADN puede activar defensas antivirales potentes de forma focal y local, a la vez que destaca cómo fármacos que alteran los lisosomas o la PPT1 podrían activar inadvertidamente este mecanismo. Aprendiendo a regular la nucleocitosis—ya sea aumentando o disminuyendo su actividad, mediante el diseño de antivirales y tratamientos contra el cáncer más inteligentes o evitando señales de ADN propio no deseadas en la autoinmunidad—los investigadores esperan aprovechar este mecanismo recién descubierto para terapias más seguras y precisas.
Cita: Negishi, H., Wada, Y., Shirasaki, Y. et al. cGAS-IFN-I responses by extracting nuclear DNA from dying cells via nucleocytosis. Nat Commun 17, 1658 (2026). https://doi.org/10.1038/s41467-026-68839-w
Palabras clave: nucleocitosis, cGAS-STING, hidroxicloroquina, interferón tipo I, macrófagos