Clear Sky Science · es
Evolución de la fotoredox catalysis de manganeso de luz visible de alta energía a luz de baja energía
Apagar la luz, conservar la química
Los químicos suelen usar luz intensa y de alta energía —como lámparas azules o ultravioleta potentes— para impulsar reacciones que construyen moléculas complejas. Pero esta luz “dura” puede desperdiciar energía, dañar partes delicadas de las moléculas y resulta difícil de emplear en profundidad dentro de tejidos o reactores grandes. Este estudio muestra cómo sales de manganeso simples y económicas pueden ensamblarse directamente en el matraz de reacción para trabajar con luz mucho más suave, en el rojo y el infrarrojo cercano, y aun así ejecutar química de formación de enlaces potente y valiosa para el descubrimiento de fármacos y la ciencia de materiales.
Por qué importa una luz más suave
La luz de alta energía es como usar un soplete para encender una vela: hace el trabajo, pero puede chamuscar todo lo cercano. En reacciones químicas, eso puede provocar reacciones excesivas, destrucción de grupos sensibles y pobre control. La luz más suave —especialmente la roja y el infrarrojo cercano, que transportan menos energía— penetra más en líquidos e incluso en tejidos biológicos y, en general, es más compatible con moléculas complejas y frágiles. El reto es que la mayoría de los catalizadores impulsados por luz están diseñados para absorber luz de mayor energía, y rediseñarlos suele requerir síntesis largas y complejas. Los autores buscaron bajar el “presupuesto de fotones” de estas reacciones sin tener que reconstruir los catalizadores desde cero.
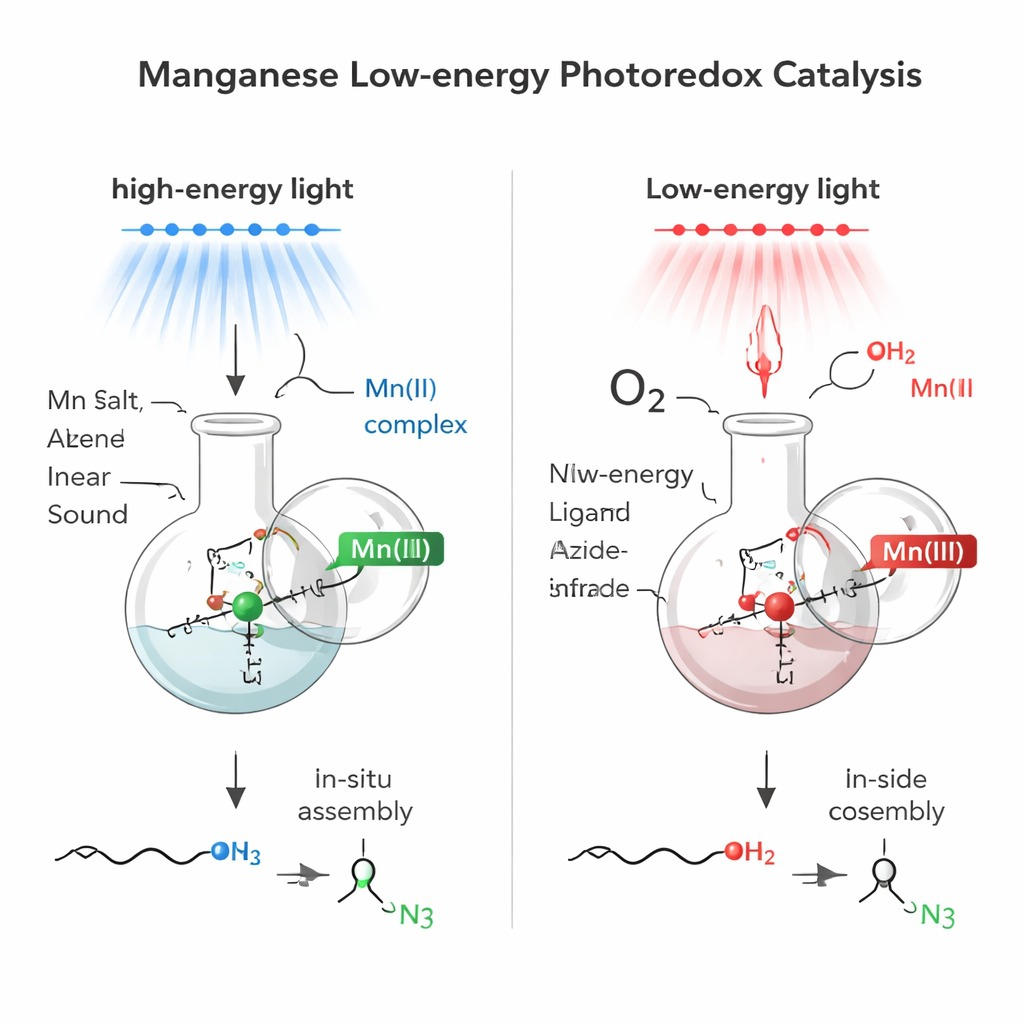
Construir el catalizador in situ
En lugar de preparar complejos metálicos elaborados por adelantado, el equipo empleó una estrategia in situ: simplemente mezclaron sales de manganeso comerciales con una pequeña molécula auxiliar (un ligando) y una fuente de azida directamente en la mezcla de reacción. Este ensamblaje espontáneo creó un sistema absorbente de luz basado en manganeso. Con una sal de manganeso(II), la mezcla absorbía intensamente luz azul y podía generar radicales “azido” de vida corta a partir de un reactivo común llamado TMSN3. Estos fragmentos reactivos se añadían luego a dobles enlaces carbono‑carbono simples (alquenos), colocando un grupo azida (N3) en el extremo menos sustituido del enlace doble —un patrón conocido como adición anti‑Markovnikov. Sorprendentemente, el agua corriente sirvió como fuente de hidrógeno, haciendo el proceso sencillo y eficiente en átomos.
Cambiando del azul al rojo intenso
Los investigadores se preguntaron si un sistema de manganeso estrechamente relacionado podría funcionar con luz de energía mucho menor, en la región del rojo intenso y el infrarrojo cercano. Al pasar de manganeso(II) a manganeso(III) y afinar el medio de reacción, crearon una nueva mezcla que absorbía luz hasta aproximadamente 850 nanómetros —bien dentro del infrarrojo cercano. Bajo esta luz suave, el complejo de manganeso(III) seguía generando radicales azido, pero ahora en presencia de aire (como fuente de oxígeno) y un alcohol simple, la reacción instaló tanto un azido como un grupo alcohol a través del alqueno en un solo paso. El resultado es un 2‑azidoalcohol, un bloque de construcción particularmente útil porque contiene dos manejos altamente versátiles —N3 y OH— en átomos de carbono contiguos.
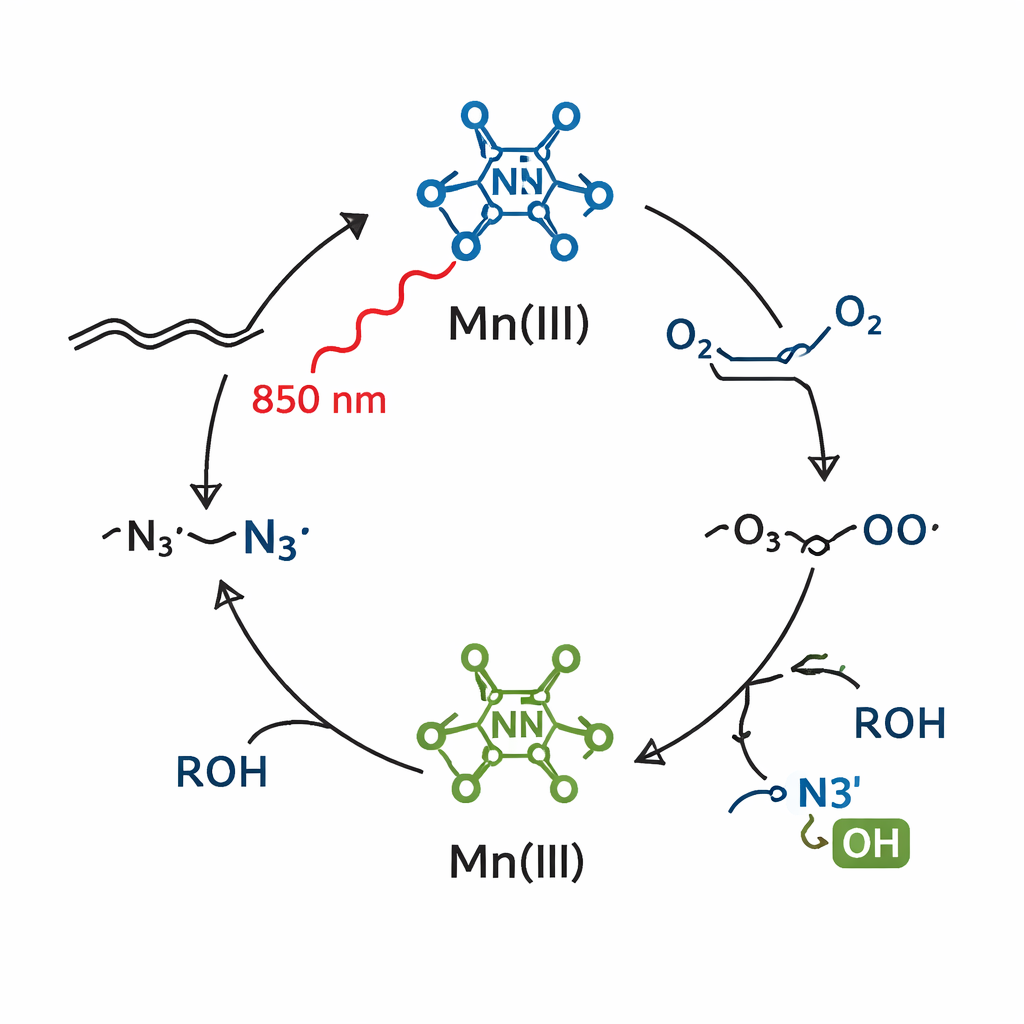
De alquenos simples a moléculas complejas tipo fármaco
Con ambos sistemas, el de luz azul y el de luz de baja energía, el equipo probó una amplia variedad de alquenos. Convirtieron muchos sustratos distintos en azidas alquílicas o 2‑azidoalcoholes con rendimientos de moderados a altos, incluso cuando las moléculas portaban grupos que típicamente interfieren con catalizadores metálicos, como aminas sin proteger, alcoholes, grupos que contienen azufre y sistemas cíclicos complejos. También demostraron “funcionalización en etapas tardías” modificando moléculas avanzadas tipo fármaco, transformando principios activos existentes en nuevos derivados con grupos azida y, en algunos casos, alcohol añadidos. Estas nuevas funciones pueden luego convertirse en otras estructuras ricas en nitrógeno o unirse selectivamente a dianas biológicas, ampliando la caja de herramientas para la química medicinal.
Química que ahorra energía con promesa práctica
El trabajo demuestra que es posible “evolucionar” una reacción de luz azul de alta energía hacia un proceso de bajo consumo en el infrarrojo cercano simplemente cambiando cómo se ensamblan en solución sal de un metal común. Los sistemas de manganeso construidos in situ evitan la síntesis laboriosa de catalizadores, usan un metal abundante y relativamente poco tóxico, y pueden incluso alimentarse con luz solar natural. Para quienes no son especialistas, el mensaje clave es que no siempre necesitamos luz más dura o metales raros y caros para realizar química exigente. Diseñando catalizadores que se formen a partir de piezas simples y que respondan a luz más suave, este enfoque apunta hacia maneras más eficientes energéticamente, escalables y compatibles con sistemas biológicos para fabricar las moléculas complejas de las que depende la medicina moderna y los materiales.
Cita: Yang, W., Song, Y., Yu, X. et al. Evolution of manganese low-energy photoredox catalysis from high-energy visible light photocatalysis. Nat Commun 17, 2062 (2026). https://doi.org/10.1038/s41467-026-68837-y
Palabras clave: catálisis fotoredox, catálisis con manganeso, luz de baja energía, funcionalización de alquenos, radicales azido