Clear Sky Science · es
Preparar frente a propagar: efectos inmunitarios distintos de radiofármacos emisores de partículas alfa frente a beta cuando se combinan con inhibición de puntos de control inmunitario en ratones
Convertir la radiación en un aliado inmunitario
Los oncólogos recurren cada vez más al sistema inmunitario para combatir los tumores, pero muchos cánceres siguen ignorando o resistiéndose a estos fármacos. Este estudio plantea una pregunta pertinente: ¿pueden distintos tipos de radiación dirigida utilizarse no solo para reducir los tumores directamente, sino para entrenar al sistema inmunitario a desempeñar mejor su función, y cambia la elección del radiofármaco la forma en que se produce ese entrenamiento?
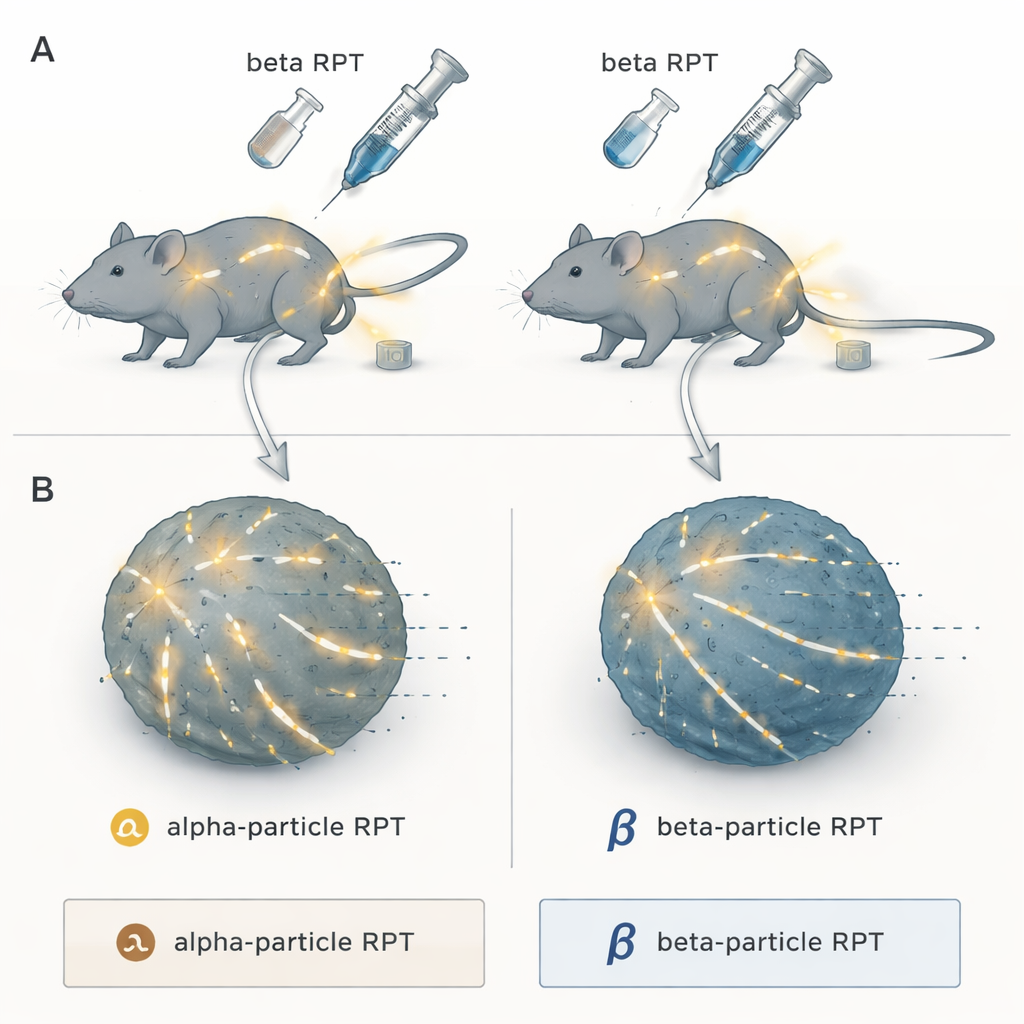
Dos variantes de radiación de precisión
Los investigadores se centraron en la terapia con radiofármacos, un enfoque de “buscar y destruir” en el que una carga radiactiva se acopla a una molécula que se dirige de forma natural a los tumores. Una vez inyectada, circula por el cuerpo y entrega radiación a nidos tumorales dondequiera que se oculten, algo que la radioterapia externa convencional no puede hacer con facilidad en enfermedad diseminada. El equipo comparó dos categorías principales: emisores de partículas alfa, que liberan ráfagas de energía extremadamente densas en una distancia muy corta, y emisores de partículas beta, que emiten radiación de menor densidad que viaja más lejos a través del tejido. Todos estaban unidos al mismo compuesto buscador de tumores, NM600, de modo que solo difería el tipo de radiación, no la diana.
Combinar radiación con bloqueadores de puntos de control inmunitario
Por sí solos, los fármacos inhibidores de puntos de control como anti‑PD‑L1 y anti‑CTLA4 pueden levantar los frenos sobre las células inmunitarias, pero funcionan mejor cuando el tumor ya es visible para el sistema inmunitario. En modelos murinos de melanoma, cáncer de próstata y cáncer colorrectal, los científicos administraron una dosis baja cuidadosamente escogida de NM600 con base alfa o beta, con o sin una combinación de inhibidores de puntos de control. También variaron cuándo se administraron los fármacos inmunitarios —antes, poco después o mucho después del tratamiento radiactivo— para ver cómo el momento afectaba resultados como el crecimiento tumoral, la supervivencia y la memoria inmunitaria a largo plazo.
Cuando la radiación beta brilla: potenciar una respuesta existente
En un modelo de cáncer colorrectal “inmuno‑caliente” que ya responde a la inmunoterapia, los mejores resultados provinieron del NM600 emisor de beta, especialmente cuando los fármacos inmunitarios se iniciaron de forma temprana o en un momento intermedio. Los tumores se redujeron más, los ratones vivieron más tiempo y los animales curados con frecuencia rechazaron el mismo cáncer cuando se reintrodujo meses después. Un perfil inmunitario detallado mostró que el tratamiento con base beta más bloqueo de puntos de control no tanto creó una nueva respuesta como amplificó la que ya existía: las células T citotóxicas tumor‑específicas preexistentes se expandieron, se activaron más y produjeron más señales de ataque. En resumen, los emisores beta fueron excelentes para propagar una respuesta inmunitaria en curso.
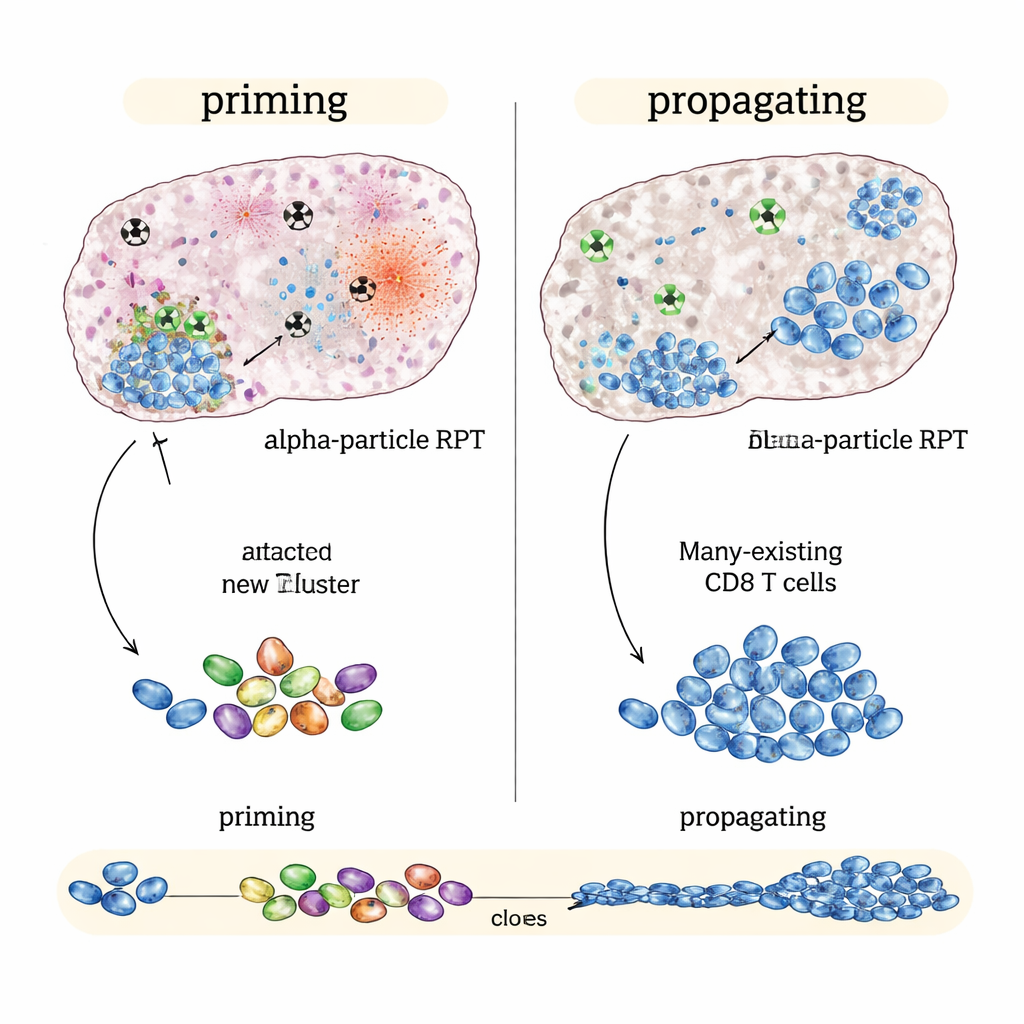
Cuando la radiación alfa brilla: provocar un nuevo ataque inmunitario
En contraste, en tumores “inmuno‑fríos” como un modelo de melanoma y uno de cáncer de próstata que apenas responden a los inhibidores de punto de control por sí solos, la versión emisora de alfa rindió mejor que los emisores beta con la misma dosis media en el tumor. La terapia basada en alfa más los fármacos inmunitarios ralentizó más el crecimiento tumoral y prolongó aún más la supervivencia. Los análisis genéticos a célula única sugirieron por qué: la radiación alfa provocó daños intensos y localizados que parecían generar señales de alarma fuertes dentro del tumor mientras respetaban estructuras inmunitarias cercanas. Este patrón se relacionó con respuestas de células T más amplias y diversas y con indicios de que se estaban formando nuevas células T citotóxicas capaces de reconocer el tumor y conectarse con células de memoria de larga duración —pruebas de primado inmunitario más que de mera amplificación.
Por qué importan el tipo y el momento de la radiación
En los distintos modelos, el inicio temprano o intermedio de los inhibidores de punto de control —aproximadamente coincidiendo con el pico de señales de peligro inducidas por la radiación— superó de forma constante al tratamiento retrasado. El trabajo sugiere una regla práctica: en cánceres ya visibles para el sistema inmunitario, los radiofármacos de baja dosis basados en beta pueden ser socios ideales para los inhibidores de punto de control porque propagan y fortalecen la inmunidad existente. En cánceres más resistentes inmunológicamente, los emisores alfa de alto impacto pueden ser más adecuados para primar respuestas nuevas de células T y convertir un tumor “frío” en “caliente”. Para los pacientes, esto significa que no todos los fármacos radiactivos son intercambiables; ajustar el isótopo y el calendario a la personalidad inmunitaria del tumor podría hacer que la radio‑inmunoterapia combinada sea a la vez más eficaz y más duradera.
Cita: Kerr, C.P., Jin, W.J., Liu, P. et al. Priming versus propagating: distinct immune effects of alpha- versus beta-particle emitting radiopharmaceuticals when combined with immune checkpoint inhibition in mice. Nat Commun 17, 2044 (2026). https://doi.org/10.1038/s41467-026-68834-1
Palabras clave: terapia con radiofármacos, radiación alfa vs beta, inhibidores de puntos de control inmunitario, inmunoterapia contra el cáncer, microambiente tumoral