Clear Sky Science · es
Seguridad y actividad biológica de un receptor de células T bispecífico dirigido al Gag del VIH en hombres que viven con VIH: un ensayo en humanos por primera vez
Por qué importa este nuevo estudio sobre el VIH
Hoy en día, las personas que viven con VIH pueden esperar una esperanza de vida casi normal gracias a los cócteles de fármacos modernos. Pero estos fármacos, denominados terapia antirretroviral (TAR), no eliminan el virus; simplemente lo mantienen controlado. Quedan reservorios ocultos de VIH en el cuerpo que pueden reiniciar la infección si se interrumpe el tratamiento. Este estudio prueba un nuevo tipo de terapia inmune de precisión —construida a partir de un receptor de células T diseñado en laboratorio— que pretende entrenar al sistema inmunitario para localizar de forma segura esos escondites en personas que ya tienen el virus bien controlado con TAR.
El virus oculto que no desaparece
Aun cuando las pruebas de sangre muestran un virus “indetectable”, el VIH persiste como material genético alojado dentro de células de larga vida, principalmente un tipo de glóbulo blanco llamado células T CD4. Estas células reservorio contienen virus silencioso pero intacto que puede reactivarse, obligando a las personas a tomar pastillas diarias de por vida. Borrar por completo cada célula infectada es extremadamente difícil y solo se ha conseguido en un puñado de personas que se sometieron a trasplantes de médula ósea arriesgados por cáncer. Muchos investigadores, en cambio, aspiran a una “curación funcional”: reducir el reservorio lo suficiente para que las defensas propias del cuerpo puedan mantener el VIH controlado sin medicación continua.
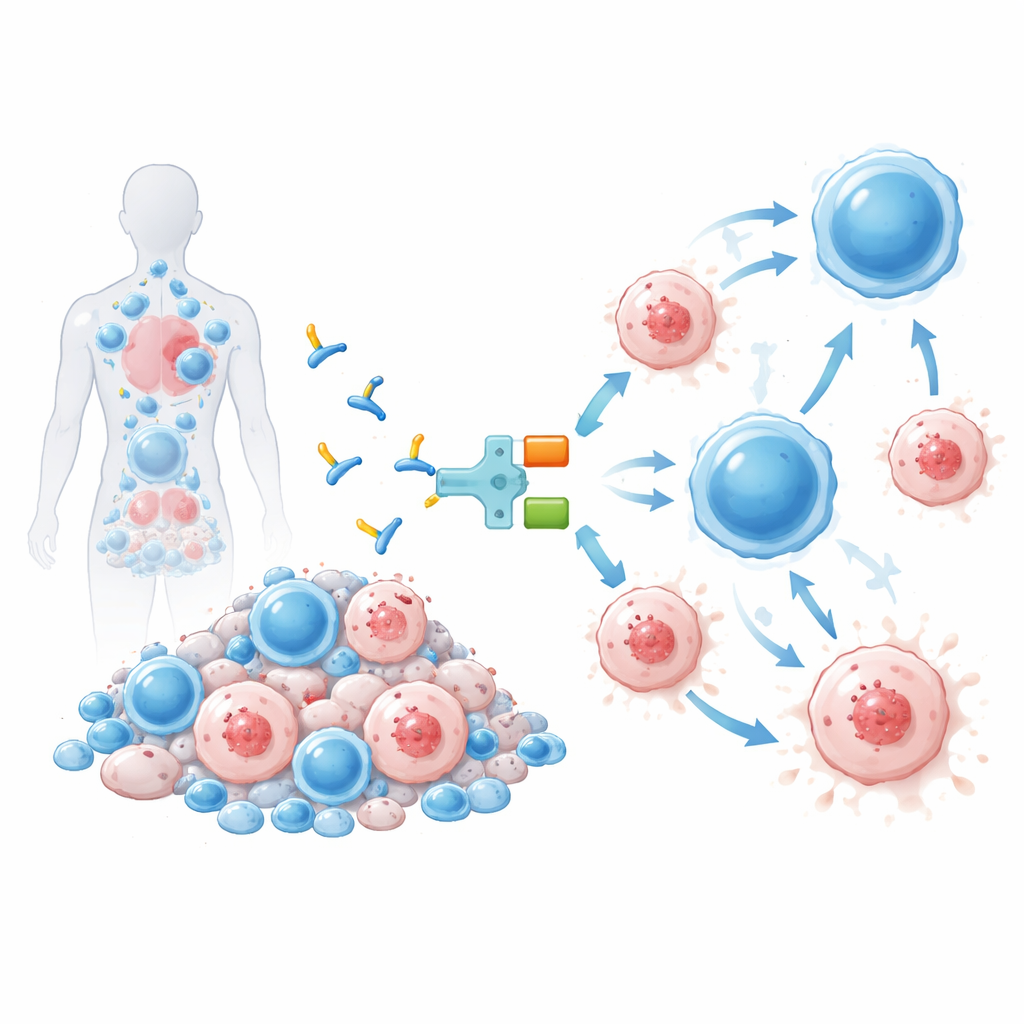
Una molécula diseñada para redirigir las células T
La terapia probada aquí, llamada IMC‑M113V, es una proteína pequeña que actúa como un adaptador molecular entre las células infectadas y el sistema inmune. Un extremo de IMC‑M113V es un receptor de células T diseñado que reconoce un pequeño fragmento del VIH procedente de la proteína Gag, mostrado en la superficie de las células infectadas en el contexto de un marcador inmunitario común (HLA‑A*02:01). El otro extremo se une a CD3, una estructura presente en todas las células T. Cuando IMC‑M113V se une a ambos lados a la vez, aproxima células T ordinarias a una célula infectada por el VIH y las activa para que la destruyan. En pruebas de laboratorio, esta molécula fue extremadamente sensible, detectando solo unas pocas copias del fragmento viral en la superficie de una célula y eliminando de forma eficaz células infectadas con varias variantes comunes del VIH, sin mostrar una activación significativa frente a un panel de células humanas sanas.
Primera prueba en personas que viven con VIH
Para evaluar si este enfoque es seguro en humanos, los investigadores realizaron un ensayo en fase temprana con doce hombres adultos que viven con VIH en el Reino Unido, Bélgica y España. Todos los participantes tenían la infección bien controlada con TAR, recuentos elevados de CD4 y poseían el tipo de HLA requerido. Cada persona recibió una dosis intravenosa única de IMC‑M113V en uno de tres niveles de dosis bajos y fue monitorizada de cerca durante un mes. El objetivo principal en esta fase fue la seguridad: vigilar efectos secundarios como fiebre, inflamación severa o problemas neurológicos, que pueden ocurrir con otros potentes fármacos que reclutan células T usados en el tratamiento del cáncer.
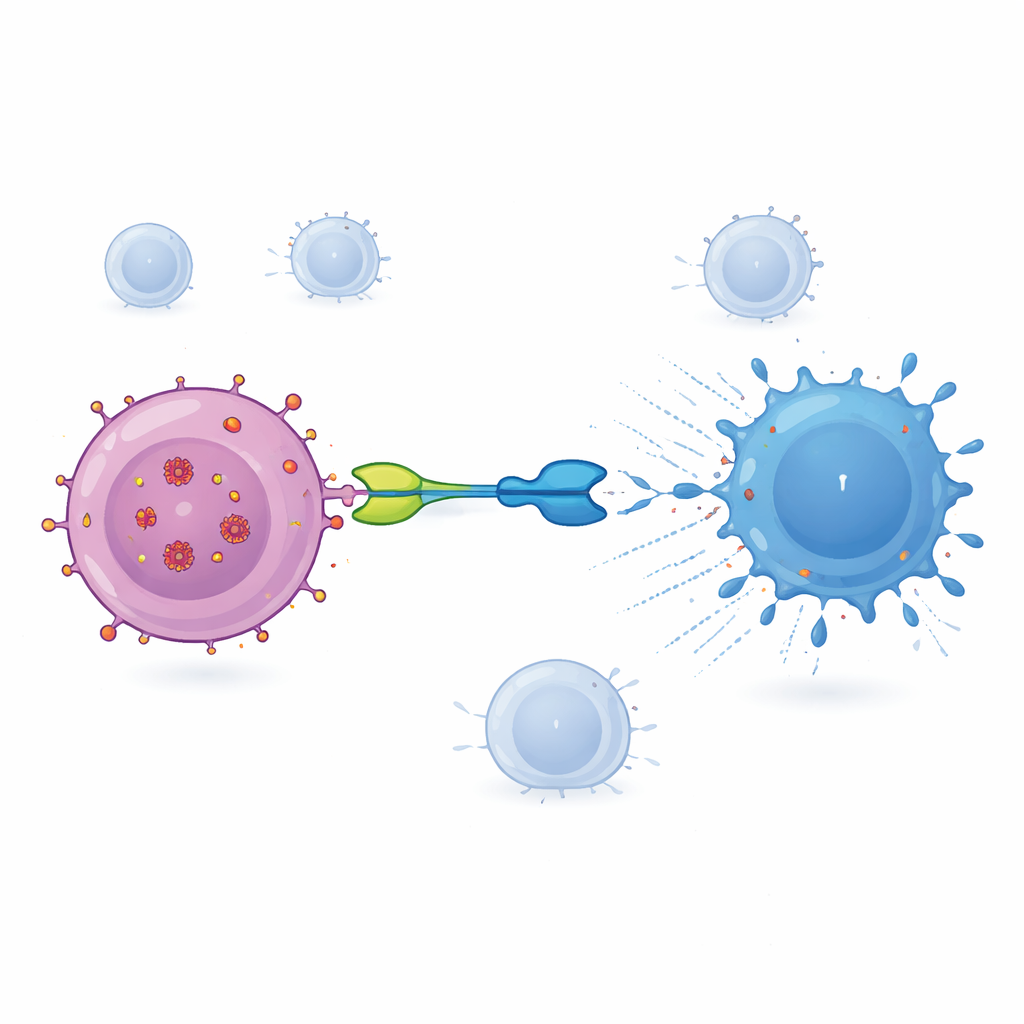
Lo que observaron los investigadores en la clínica
En todos los niveles de dosis, IMC‑M113V fue generalmente bien tolerado. La mitad de los participantes comunicó algunos efectos secundarios, en su mayoría problemas leves como fatiga o irritación cutánea, y nadie desarrolló complicaciones graves como síndrome de liberación de citocinas o neurotoxicidad. Los análisis de sangre mostraron que los niveles del fármaco aumentaban y decrecían en aproximadamente un día, con una vida media de alrededor de 15–22 horas. En la dosis más alta (15 microgramos), varios participantes mostraron aumentos temporales en moléculas inflamatorias, especialmente interleucina‑6, y signos de que sus células T se habían activado y eran más capaces de producir proteínas citotóxicas. Estos cambios inmunitarios fueron más fuertes en voluntarios cuyos virus portaban variantes de Gag que IMC‑M113V puede unirse con particular afinidad, lo que sugiere que el fármaco estaba interactuando con sus dianas previstas en el organismo. Sin embargo, tras una única dosis no se observó una reducción medible en el tamaño del reservorio del VIH en sangre, según el ARN viral y el ADN viral intacto dentro de las células CD4.
Qué significa esto para el futuro del tratamiento del VIH
Para un lector no especializado, el mensaje principal es que este estudio aporta una importante prueba de concepto inicial: una molécula inmune altamente dirigida que actúa como “puente” puede administrarse de forma segura a personas con VIH bien controlado y puede activar sus células T para reconocer células que albergan el virus. No curó el VIH ni permitió que las personas interrumpieran la TAR, pero ese no era el objetivo de este ensayo en humanos inicial. Los hallazgos respaldan probar dosis mayores y repetidas, posiblemente combinadas con fármacos que inducen a más células infectadas a revelarse, y ampliar el enfoque para abarcar otros tipos inmunitarios más allá de HLA‑A*02:01. Si estudios futuros confirman que esta estrategia puede reducir de forma fiable los reservorios virales sin efectos secundarios peligrosos, podría convertirse en una parte clave de tratamientos combinados orientados al control a largo plazo del VIH sin fármacos.
Cita: Vandekerckhove, L., Fox, J., Mora-Peris, B. et al. Safety and biologic activity of a bispecific T cell receptor targeting HIV Gag in males living with HIV: a first-in-human trial. Nat Commun 17, 2207 (2026). https://doi.org/10.1038/s41467-026-68833-2
Palabras clave: Curación del VIH, Terapia con células T, Reservorio viral, Receptor bispecífico, Ensayo clínico