Clear Sky Science · es
Perspectivas mecanísticas sobre el desdoblamiento dirigido por PCBP1 de i-motif de ADN selectos en el control del punto de paso G1/S
Plegamientos de ADN que actúan como semáforos
Dentro de nuestras células, el código genético es más que una simple escalera recta de ADN. Parte de él puede plegarse en formas inusuales que actúan como pequeños interruptores, ayudando a controlar cuándo las células copian su ADN y se dividen. Este estudio se centra en una de esas formas, llamada i-motif, y en una proteína denominada PCBP1 que puede reconocer y desplegar estas estructuras justo cuando la célula se prepara para replicar su ADN. Comprender esta interacción arroja luz sobre cómo las células mantienen la estabilidad de su genoma y qué puede fallar en el cáncer.
Misteriosos nudos de ADN en regiones vinculadas al cáncer
La mayoría aprende que el ADN forma la famosa doble hélice, pero ciertos tramos ricos en la letra C (citosina) pueden plegarse en un nudo de cuatro hebras conocido como i-motif. Estas estructuras tienden a aparecer en regiones reguladoras de genes que impulsan el crecimiento celular, como cMYC y BCL2. Durante años, los científicos debatieron si los i-motifs realmente se forman en células vivas, porque son más fáciles de detectar en condiciones ácidas de tubo de ensayo que en las condiciones casi neutras del interior del organismo. Usando anticuerpos especializados que reconocen i-motifs, trabajos recientes, incluido el presente estudio, han confirmado que aparecen en los núcleos celulares—y con frecuencia se agrupan cerca de genes clave de crecimiento y cáncer.
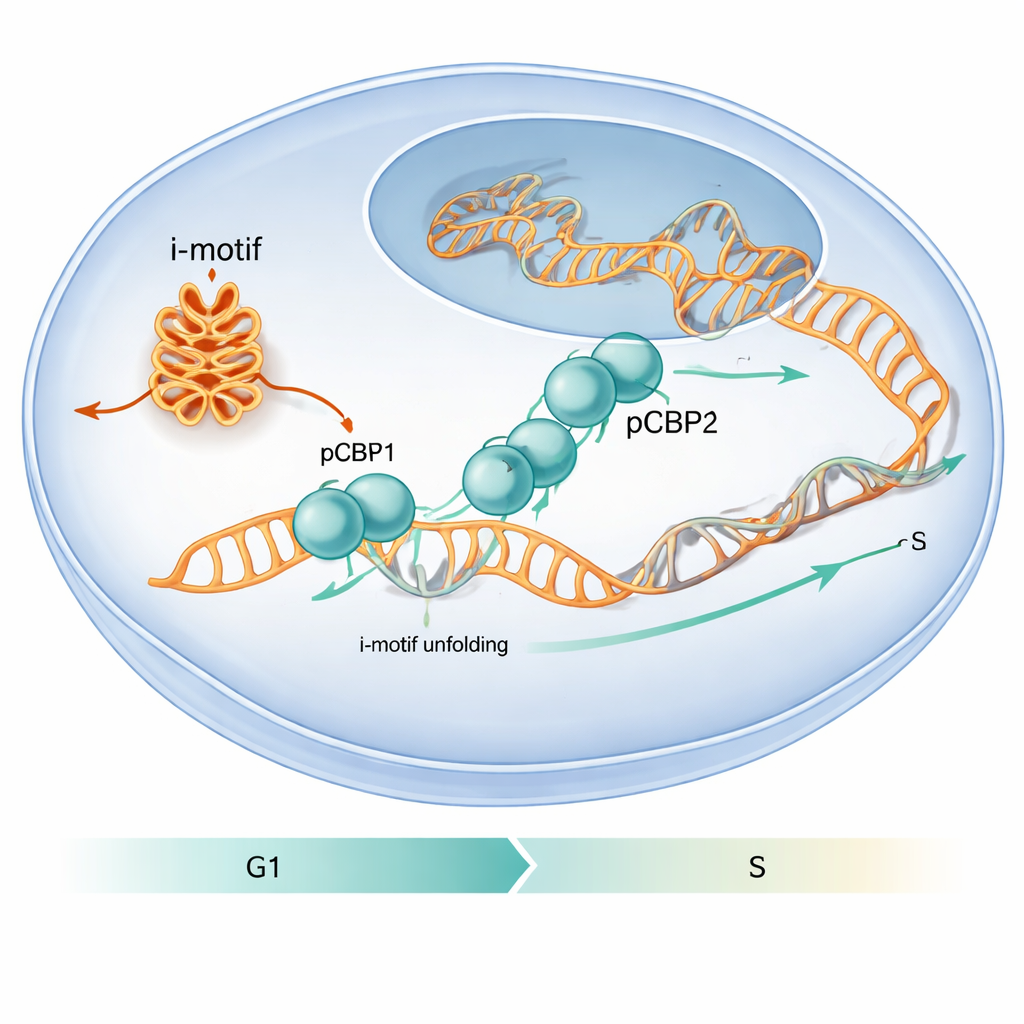
Una proteína que distingue pliegues especiales del ADN
Los autores se propusieron descubrir cómo las proteínas en la célula tratan estos pliegues inusuales del ADN. Se centraron en PCBP1, una proteína ya conocida por unirse a tramos ricos en C de ADN y ARN y por influir en el ciclo celular. Al analizar mapas de unión a escala genómica existentes y realizar experimentos dirigidos, hallaron que PCBP1 frecuentemente se localiza en regiones ricas en C que pueden formar i-motifs, especialmente alrededor de los sitios de inicio de los genes. En experimentos celulares con líneas de cáncer humanas, regiones de los promotores de cMYC, BCL2 y la secuencia ILPR vinculada a la insulina mostraron tanto señales fuertes de i-motif como una marcada ocupación por PCBP1, lo que sugiere que PCBP1 actúa como un guardián dedicado de estas estructuras.
Cómo PCBP1 atrapa y desenreda el nudo
En ensayos de tubo de ensayo, los investigadores compararon la afinidad de PCBP1 por i-motifs plegados frente a la misma secuencia de ADN en forma desplegada. Ajustaron la acidez para que el ADN permaneciera plegado o se relajara, manteniendo estable la proteína. PCBP1 mostró siempre preferencia por el i-motif plegado, uniéndose a él aproximadamente el doble de fuerte que a la misma secuencia cuando estaba desplegada, y solo débilmente a formas de ADN no relacionadas. Una vez unido, PCBP1 podía promover activamente el desdoblamiento, permitiendo que la hebra del i-motif se emparejara con su complementaria. Sin embargo, no todos los i-motifs se comportaron igual: algunos, como la estructura en el promotor de cMYC, se desplegaron rápidamente, mientras que otros, como los de BCL2, ofrecieron resistencia y se desplegaron solo lentamente. Características adicionales como horquillas en las hebras del ADN y el grado de protonación de las citosinas (tener carga positiva adicional) podían facilitar o dificultar la actividad desenredadora de PCBP1.
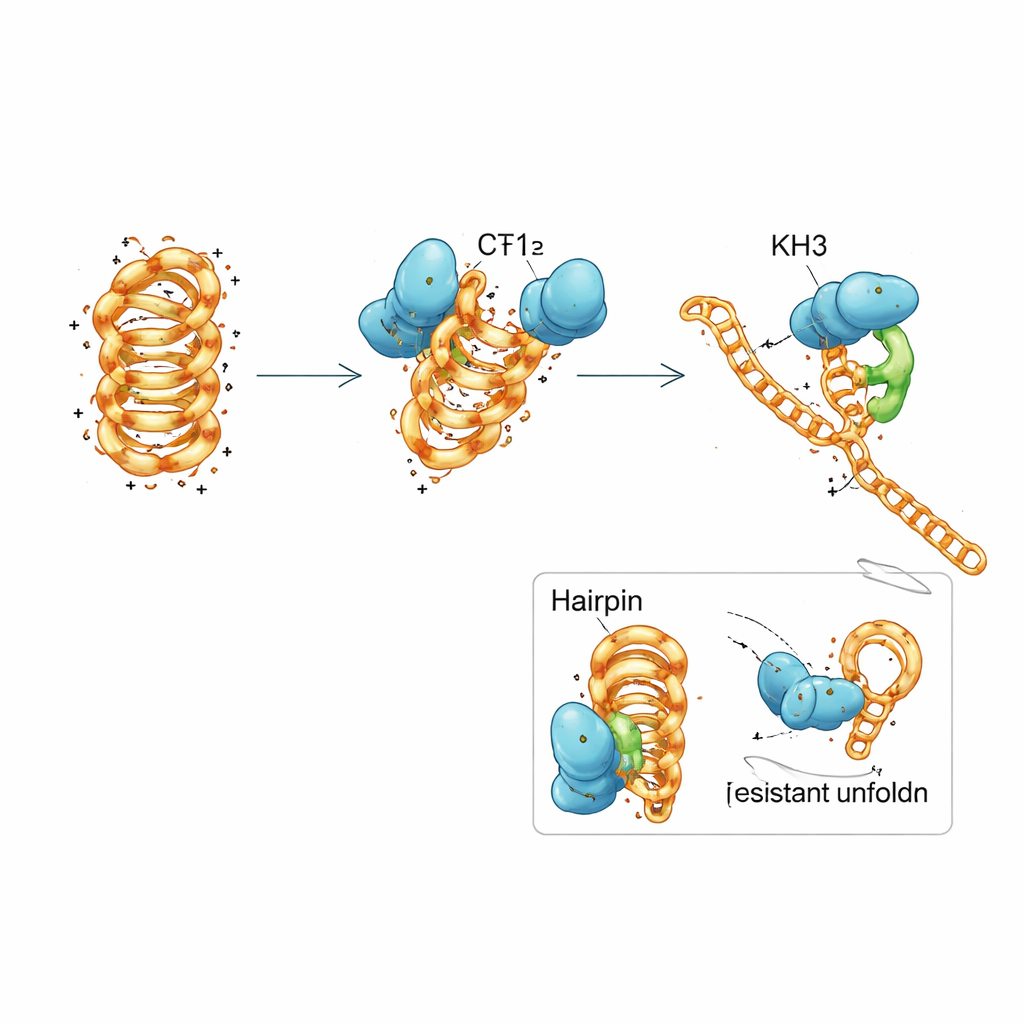
Un esfuerzo en equipo dentro de una sola proteína
PCBP1 está formado por tres módulos repetidos denominados dominios KH, motivos comunes que captan tramos cortos de ácidos nucleicos. El equipo disecó PCBP1 en piezas y descubrió que ningún dominio KH por sí solo podía reproducir completamente el comportamiento de la proteína intacta. Los dos primeros dominios juntos podían adherirse tanto al ADN plegado como al desplegado y empujar al i-motif hacia una forma menos estable, pero solo promovían lentamente el desdoblamiento total. El tercer dominio por sí solo apenas se unía. Cuando los tres dominios estaban presentes y podían cooperar, la proteína recuperaba su fuerte preferencia por los i-motifs plegados y su capacidad eficiente para desplegarlos. Mediciones biofísicas detalladas y simulaciones por ordenador sugirieron un mecanismo escalonado: KH1 y KH2 primero se acoplan a regiones flexibles de los bucles del i-motif y alteran parcialmente pares de bases seleccionados, lo que permite luego que KH3 se implique y conduzca la estructura a un estado abierto, listo para la replicación.
Mantener el ciclo celular en horario
El trabajo también demuestra que esta danza molecular importa para el comportamiento celular. Cuando los investigadores redujeron los niveles de PCBP1 en células humanas, aparecieron más estructuras i-motif en promotores génicos específicos, aumentaron los marcadores de daño en el ADN y las células se detuvieron en el crítico punto de control G1/S—el momento justo antes de que comience la replicación del ADN. En condiciones normales, la presencia de PCBP1 en regiones susceptibles de formar i-motifs alcanza su máximo alrededor de este punto de control y luego disminuye al iniciarse la fase S, cuando los i-motifs se resuelven. Esta sincronía sugiere que PCBP1 actúa como un cuidador: se une y despliega i-motifs concretos en el momento oportuno para que la replicación del ADN pueda proceder sin problemas y el genoma permanezca intacto. Para un lector no especializado, el mensaje es que los pliegues inusuales del ADN pueden funcionar como obstáculos temporales en la vía, y PCBP1 es una de las herramientas especializadas que la célula emplea para retirarlos, ayudando a prevenir errores que de otro modo podrían contribuir al cáncer.
Cita: Sengupta, P., Gillet, N., Obi, I. et al. Mechanistic insights into PCBP1-driven unfolding of selected i-motif DNA at G1/S checkpoint. Nat Commun 17, 1149 (2026). https://doi.org/10.1038/s41467-026-68822-5
Palabras clave: ADN i-motif, proteína PCBP1, punto de control del ciclo celular, estabilidad genómica, estructura secundaria del ADN