Clear Sky Science · es
La transcriptómica unicelular guiada por química revela la remodelación del andamiaje mediada por sulfotransferasas en la biosíntesis de securinina
Por qué importa la química de un arbusto
Los alcaloides de securinega son moléculas potentes que se encuentran en un pequeño arbusto ornamental, Flueggea suffruticosa, largamente estudiado por su potencial en tratamientos contra el cáncer y enfermedades neurológicas. Sin embargo, hasta ahora nadie sabía realmente cómo construye esta planta esos compuestos tan complejos. Este estudio combina la lectura génica unicelular moderna con ingeniosos experimentos químicos para revelar, paso a paso, cómo la planta monta y remodela estas moléculas —y revela un trabajo inesperado para un tipo común de enzima en el proceso. 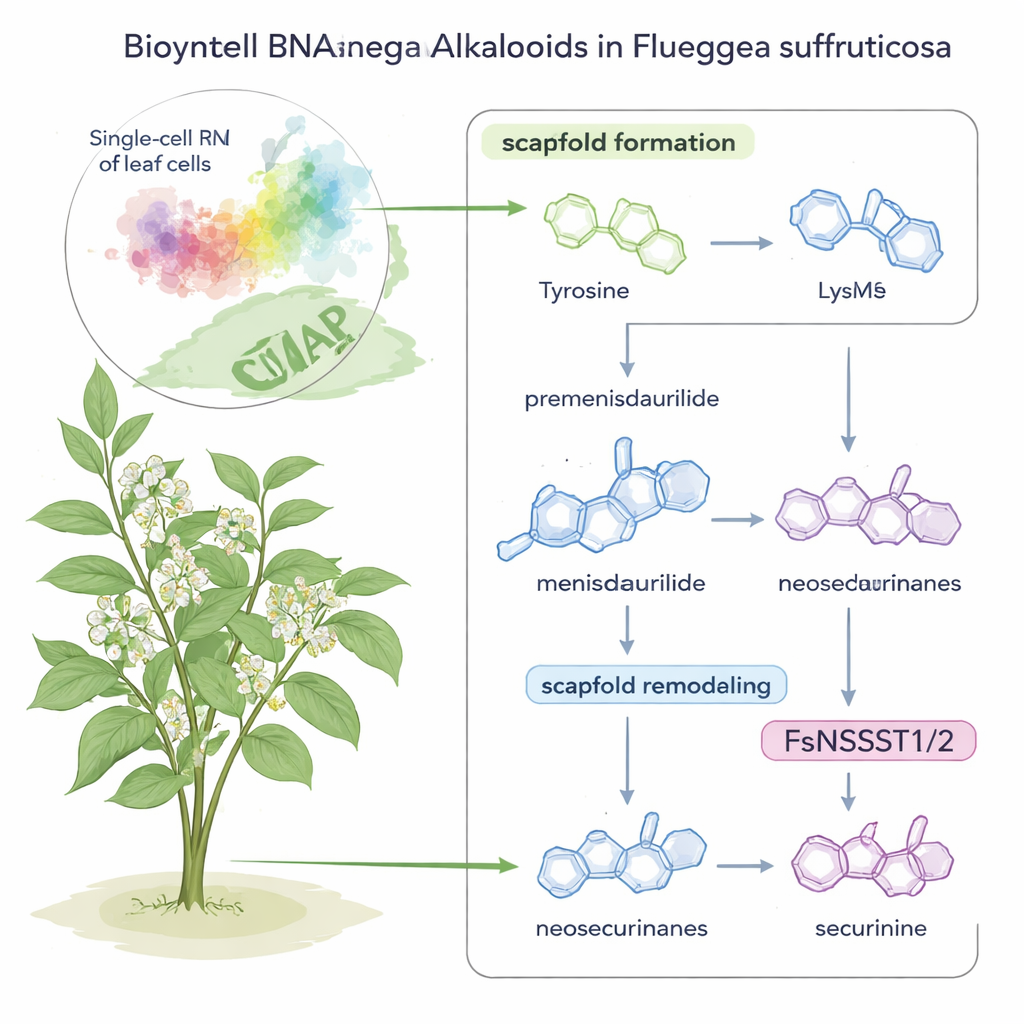
Ladrillos constructores a partir de aminoácidos cotidianos
La historia comienza con dos nutrientes familiares: los aminoácidos tirosina y lisina. En F. suffruticosa, la tirosina se transforma en una inusual molécula cíclica llamada premenisdaurilida, que luego se reduce a menisdaurilida por una enzima recién descubierta que los autores denominan FsMS (por “menisdaurilide synthase”). En paralelo, la lisina se convierte en un pequeño anillo con nitrógeno llamado 1-piperideína por otra enzima, FsPS, identificada en trabajos anteriores. Cuando la menisdaurilida y la 1-piperideína se encuentran en condiciones ligeramente básicas, acuosas, se fusionan espontáneamente para formar alcaloides “neosecurinanos”, estructuras intermedias en el camino hacia los compuestos medicinales finales.
Ver la química en tiempo real
Para demostrar que estos pasos propuestos no son solo teóricos, el equipo sintetizó versiones de los intermediarios sospechados marcadas con átomos de carbono pesados. Alimentar estos compuestos etiquetados a extractos de la planta permitió a los científicos trazar exactamente dónde acababan los átomos. Observaron la conversión de menisdaurilida marcada en neosecurinanos marcados, y de estos en los alcaloides conocidos allosecurinina y securinina, confirmando que estos intermedios forman realmente parte de la vía natural. Es importante destacar que algunas de las reacciones clave de formación de anillos ocurrieron incluso en extractos hervidos, lo que muestra que partes de la ruta pueden avanzar sin enzimas, impulsadas simplemente por la química intrínseca de las moléculas.
Acercándose a las células correctas
Saber qué moléculas aparecen dónde es solo la mitad del rompecabezas; identificar los genes que controlan cada paso requiere saber qué células realizan el trabajo. Los investigadores secuenciaron ARN de miles de células individuales tomadas de hojas de F. suffruticosa, agrupándolas en tipos celulares distintos según los patrones de actividad génica. Un grupo, asociado a las venas de la hoja, destacó: expresaba con fuerza los genes conocidos de la vía y muchas enzimas vinculadas al metabolismo de tirosina, lisina y azufre. Al examinar qué genes variaban al unísono con las enzimas de la vía dentro de este grupo, el equipo identificó a FsMS y a dos sulfotransferasas, FsNSST1 y FsNSST2, como candidatas principales para los pasos faltantes. 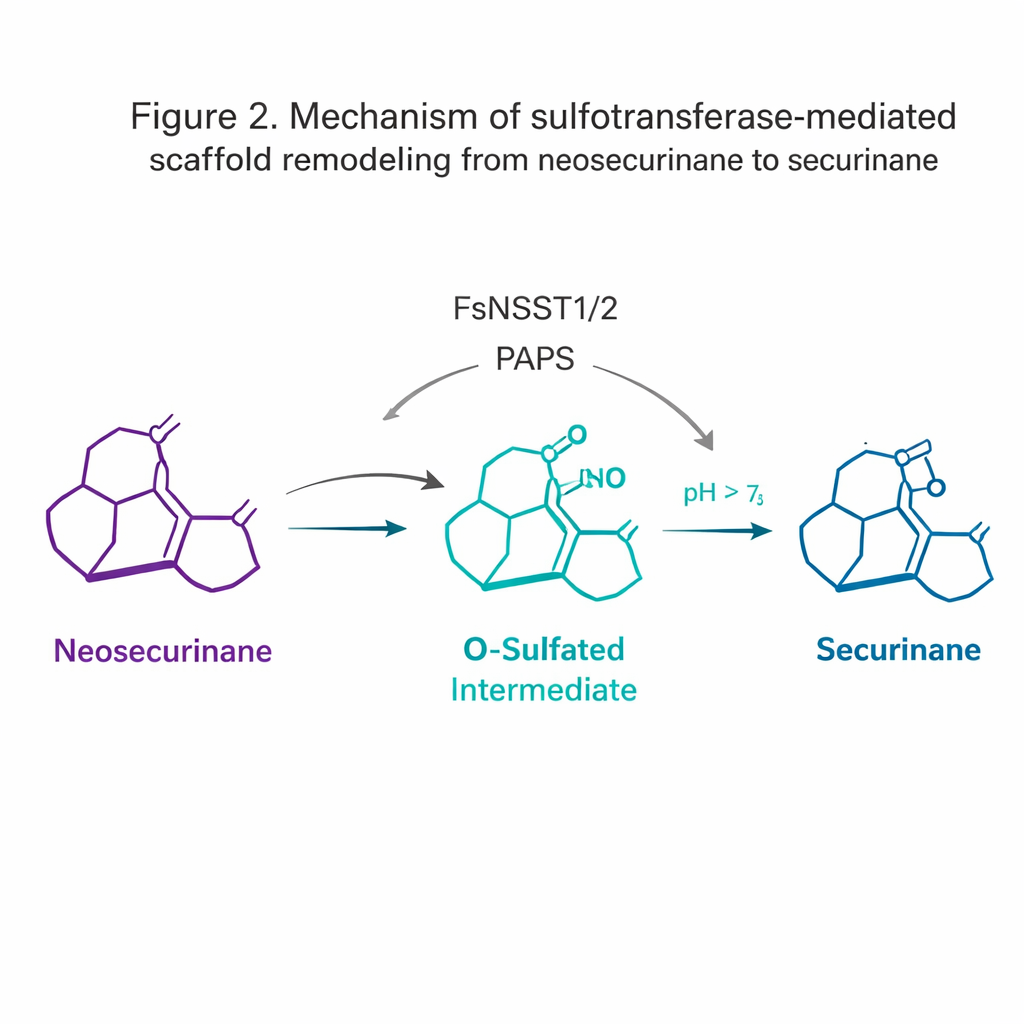
Una enzima que remodela el andamiaje molecular
El hallazgo más sorprendente provino de las sulfotransferasas. Normalmente, las sulfotransferasas añaden un grupo sulfato a las moléculas para mejorar su solubilidad o marcarlas para su degradación. Aquí, FsNSST1 y FsNSST2 actúan en cambio como interruptores: añaden sulfato al andamiaje neosecurinano, transformándolo temporalmente en un intermediario “O-sulfatado” de alta energía. Esta forma activada sufre luego un desplazamiento espontáneo 1,2-amina —un pequeño reordenamiento en el que un átomo de nitrógeno migra— convirtiendo el armazón bicíclico [2.2.2] del “neosecurinano” en el armazón [3.2.1] del “securinano”. Este sutil paso de remodelación es lo que origina el núcleo tetracíclico distintivo de los alcaloides con actividad biológica.
Por qué importa esta vía
Para un público no especialista, el mensaje clave es que la planta ensambla los alcaloides de securinega en dos fases principales: primero construye un sistema de anillos preliminar a partir de aminoácidos comunes; luego remodela químicamente ese andamiaje en una forma más compleja usando un “disparador” sulfato. Al combinar el perfilado génico célula por célula con química isotópica marcada, los autores cartografían esta ruta en detalle y revelan que las sulfotransferasas —enzimas presentes en todas las formas de vida— pueden hacer más que decorar moléculas; pueden iniciar reordenamientos completos de su estructura. Entender esta vía no solo aclara cómo se fabrican en la naturaleza una prometedora clase de moléculas semejantes a fármacos, sino que también abre la puerta a la ingeniería de cultivos o microbios para producir nuevos medicamentos inspirados en securinega.
Cita: Choung, S., Kang, G., Kim, T. et al. Chemically guided single-cell transcriptomics reveals sulfotransferase-mediated scaffold remodeling in securinine biosynthesis. Nat Commun 17, 1954 (2026). https://doi.org/10.1038/s41467-026-68816-3
Palabras clave: alcaloides vegetales, biosíntesis, transcriptómica unicelular, sulfotransferasa, química de productos naturales