Clear Sky Science · es
Trayectorias celulares y transcripcionales de la especificación del destino neuronal en anémonas de mar revelan dos modos de neurogénesis adulta
Cómo una criatura marina sencilla sigue formando nuevas células cerebrales
La mayoría de los animales, incluidos los humanos, generan la mayoría de sus neuronas al principio de la vida y luego detienen en gran medida esa producción. Sin embargo, algunos animales aparentemente simples, como las anémonas de mar, continúan incorporando nuevas neuronas a lo largo de la edad adulta. Este estudio explora cómo la anémona estrella (Nematostella vectensis) renueva y remodela de forma constante su sistema nervioso difuso, revelando estrategias que podrían evocar soluciones antiguas para el crecimiento y la reparación de cerebros.
Un cuerpo en crecimiento necesita una red nerviosa que crezca
Las anémonas de mar no tienen cerebro; en su lugar poseen una red nerviosa enmarañada distribuida por la pared corporal. A medida que estos animales crecen o se encogen según la disponibilidad de alimento, su red nerviosa debe ampliarse o reducirse para adaptarse. Usando una proteína fluorescente sensible a la luz como sello temporal, los autores marcaron neuronas existentes en adultos juveniles y luego observaron las células recién nacidas que aparecieron durante la semana siguiente. Encontraron abundantes neuronas nuevas repartidas a lo largo del eje corporal, no confinadas a una zona de crecimiento especial. Estas células nuevas surgieron tanto en el extremo orientado hacia la boca como en el extremo opuesto del animal, mostrando que la neurogénesis adulta es espacialmente amplia y continua.
Rastreando el origen de las nuevas células nerviosas
Para descubrir de dónde proceden estas nuevas neuronas, los investigadores combinaron imágenes en vivo con secuenciación de ARN de célula única, una técnica que lee qué genes están activos en miles de células individuales. Se centraron en células que portaban “reporteros” fluorescentes controlados por tres genes clave: FoxL2, SoxC y Elav. FoxL2 marca un amplio reservorio de células progenitoras multipotentes en división; SoxC se activa de forma breve cuando las células comienzan a especializarse; y Elav está fuertemente activo en neuronas peptidérgicas, que se comunican principalmente mediante pequeños péptidos señalizadores. El equipo mostró que una población de progenitores FoxL2-positivos y Piwi1-positivos se comporta como células madre: se autorrenuevan mientras generan continuamente descendientes diversos, incluidas neuronas, células urticantes llamadas cnidocitos y células secretoras. SoxC y Elav, en cambio, se iluminan solo cuando las células abandonan este reservorio progenitor y se comprometen con destinos neuronales particulares.
Dos caminos distintos hacia las neuronas adultas
Alineando los tiempos de los reporteros con la firma de expresión génica de cada célula, el estudio descubrió dos rutas distintas hacia células neuronales maduras. Las neuronas peptidérgicas siguen una vía directa: provienen de progenitores que ya presentan un perfil molecular «comprometido con lo peptidérgico» y luego se diferencian rápidamente en una variedad de subtipos neuronales. Los nuevos miembros de cada subtipo aparecen en proporción a la frecuencia con la que ese subtipo ya existe, lo que sugiere que el sistema mantiene una mezcla equilibrada de tipos neuronales en lugar de favorecer algunos en particular. En esta línea, no hay una serie clara de estaciones intermedias; en lugar de ello, subtipos neuronales estrechamente relacionados surgen en paralelo a partir de progenitores similarmente predispuestos. 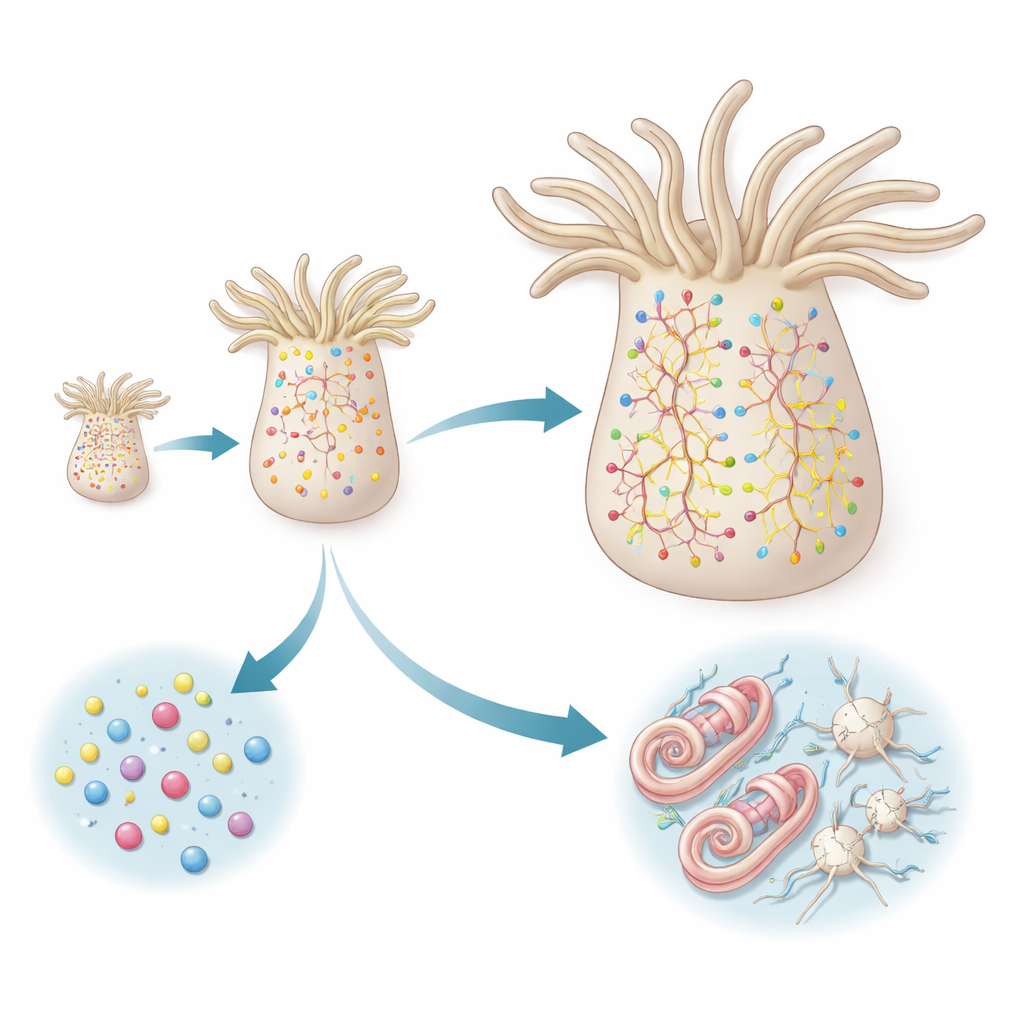
El caso especial de las células urticantes
Los cnidocitos, las células urticantes únicas de los cnidarios, siguen una ruta más escalonada. Primero atraviesan una fase de «construcción de cápsula», durante la cual fabrican sus característicos orgánulos presurizados que pueden disparar un arpón microscópico. Esta etapa depende de un conjunto específico de genes regulatorios y proteínas estructurales que están mayormente ausentes en otros tipos celulares. Solo después de completarse este programa intermedio los cnidocitos activan un segundo programa más convencional de tipo neuronal, incorporando canales iónicos y otros componentes necesarios para la señalización eléctrica. Los datos genéticos de mutantes que se estancan en la etapa temprana refuerzan este modelo de dos fases: bloquear la transición impide la aparición de las características neuronales posteriores. 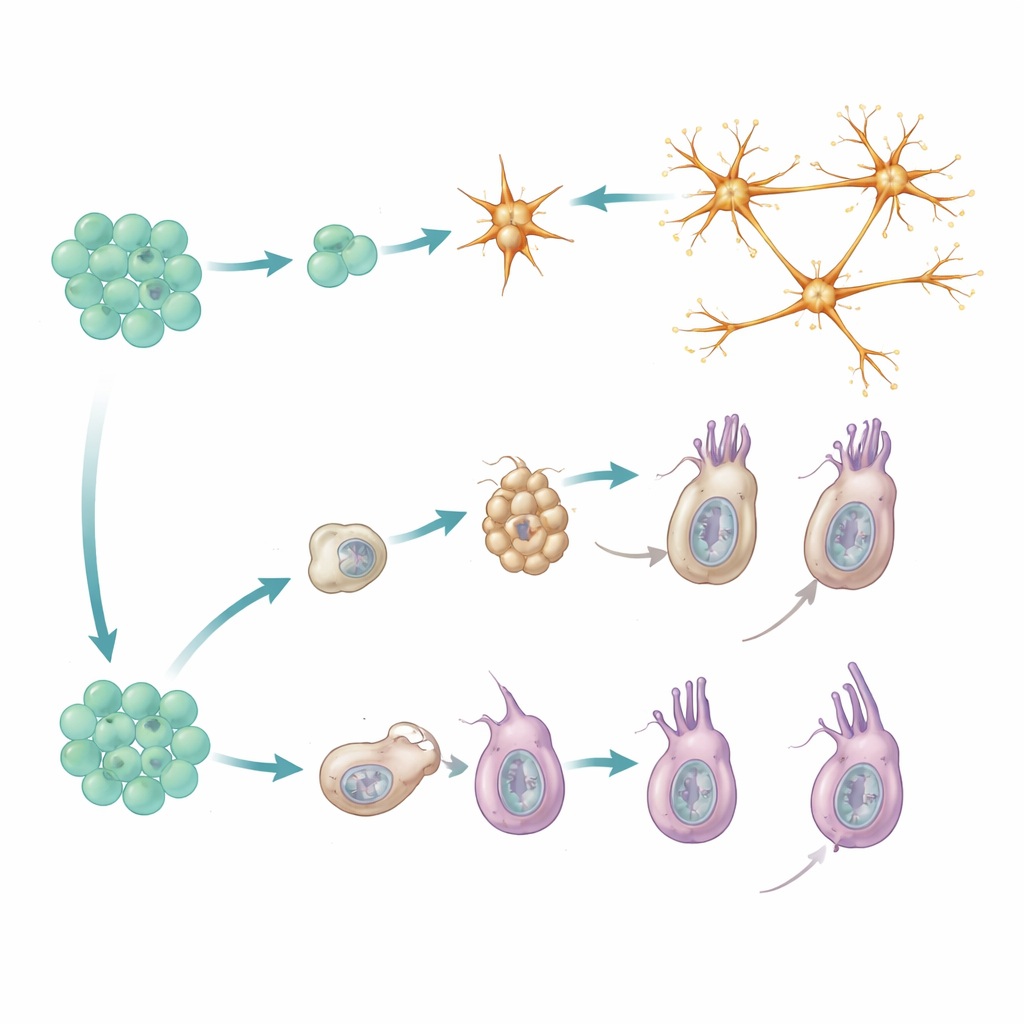
Reglas compartidas y raíces antiguas
A pesar de sus rutas diferentes, las neuronas peptidérgicas y los cnidocitos dependen de familias de genes regulatorios superpuestas para afianzar sus identidades. Rasgos neuronales generales se asocian con factores de transcripción bHLH y bZIP, mientras que la identidad fina de cada subtipo neuronal la especifican combinaciones únicas de genes de dominio homeobox y dedos de zinc: un «código» que recuerda a cómo se definen los tipos neuronales en animales más complejos, incluidos gusanos y vertebrados. Los autores sostienen que estas estrategias modulares —progenitores tipo célula madre, actividad transitoria de SoxC durante el compromiso y códigos homeodominio que definen subtipos— pueden representar principios profundamente conservados de la neurogénesis. En las anémonas, sostienen la renovación y el escalado de la red nerviosa durante toda la vida; en otros animales, mecanismos relacionados podrían subyacer tanto a la neurogénesis adulta limitada como a las notables habilidades regenerativas observadas en algunas líneas evolutivas.
Cita: Plessier, F., Marlow, H. Cellular and transcriptional trajectories of neural fate specification in sea anemone uncover two modes of adult neurogenesis. Nat Commun 17, 2611 (2026). https://doi.org/10.1038/s41467-026-68802-9
Palabras clave: neurogénesis adulta, anémona de mar, células progenitoras neurales, cnidocitos, transcriptómica de célula única