Clear Sky Science · es
Entrega de coacervados peptídicos para formar centros de interacción estables en células
Construyendo nuevos “puestos de trabajo” dentro de las células
Nuestras células están llenas de pequeños espacios de trabajo donde tienen lugar tareas importantes —como la producción de energía o las respuestas al estrés—. Con el tiempo, o en enfermedad, estos puestos naturales pueden fallar. Este estudio explora una forma de añadir nuevos “centros de interacción” a células vivas usando gotas sencillas hechas en el laboratorio a partir de péptidos cortos. Estos centros sintéticos pueden capturar proteínas específicas, concentrarlas e incluso ayudar a degradarlas, lo que sugiere nuevas estrategias para futuras terapias e ingeniería celular.
Por qué las células necesitan espacios de trabajo a medida
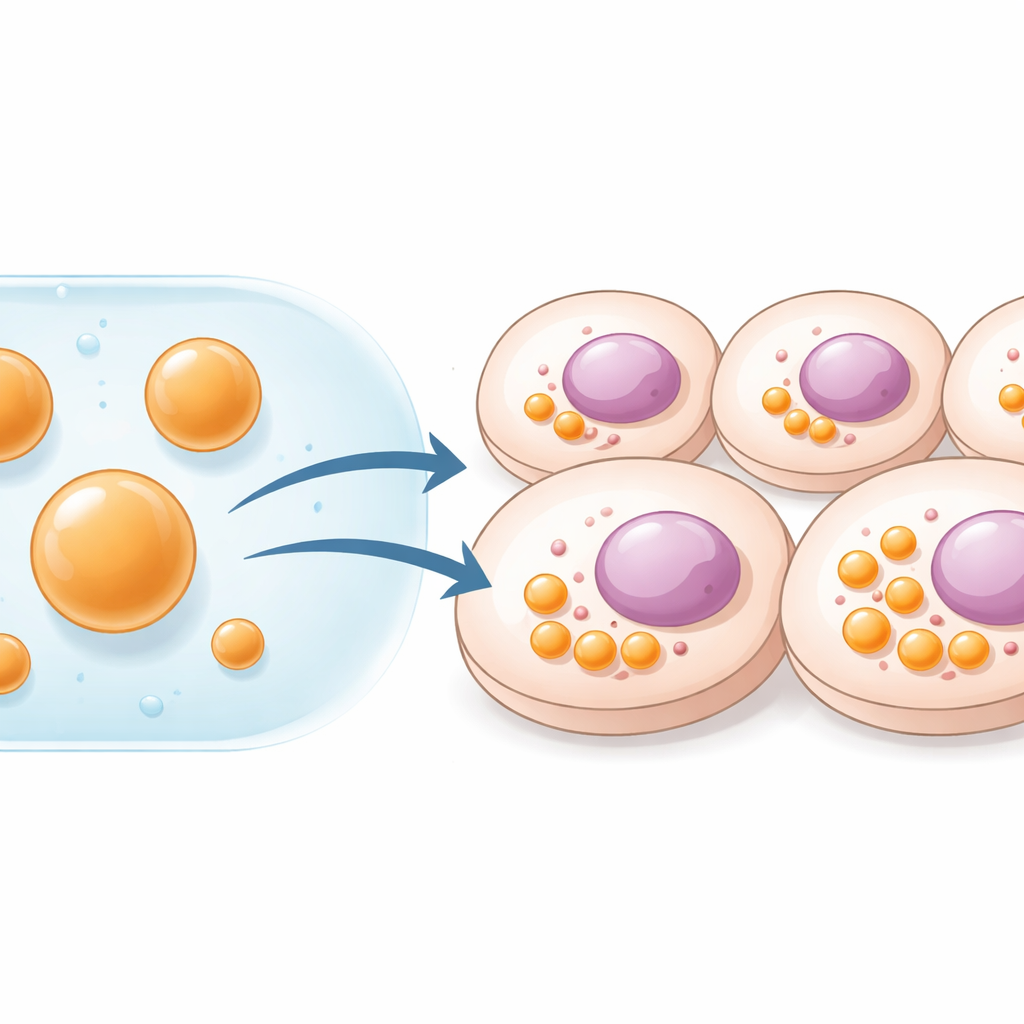
Las células mantienen el orden separando diferentes tareas en compartimentos distintos. Algunos están rodeados por membranas, como las mitocondrias; otros son estructuras más suaves, similares a gotas, que se forman cuando ciertas proteínas y ARN se agrupan. Estas gotas fluidas, o condensados, actúan como centros de reacción que aceleran o detienen vías bioquímicas particulares. Investigadores han diseñado previamente tales compartimentos haciendo que las células fabriquen proteínas andamiaje especiales mediante genes insertados. Aunque potente, ese método requiere la entrega de ADN y limita la cantidad de material que la célula puede producir. Los autores de este trabajo propusieron eludir por completo el ADN y, en su lugar, fabricar compartimentos ya formados fuera de la célula para entregarlos directamente como gotas estables de tamaño micrométrico.
Gotas peptídicas que forman centros estables
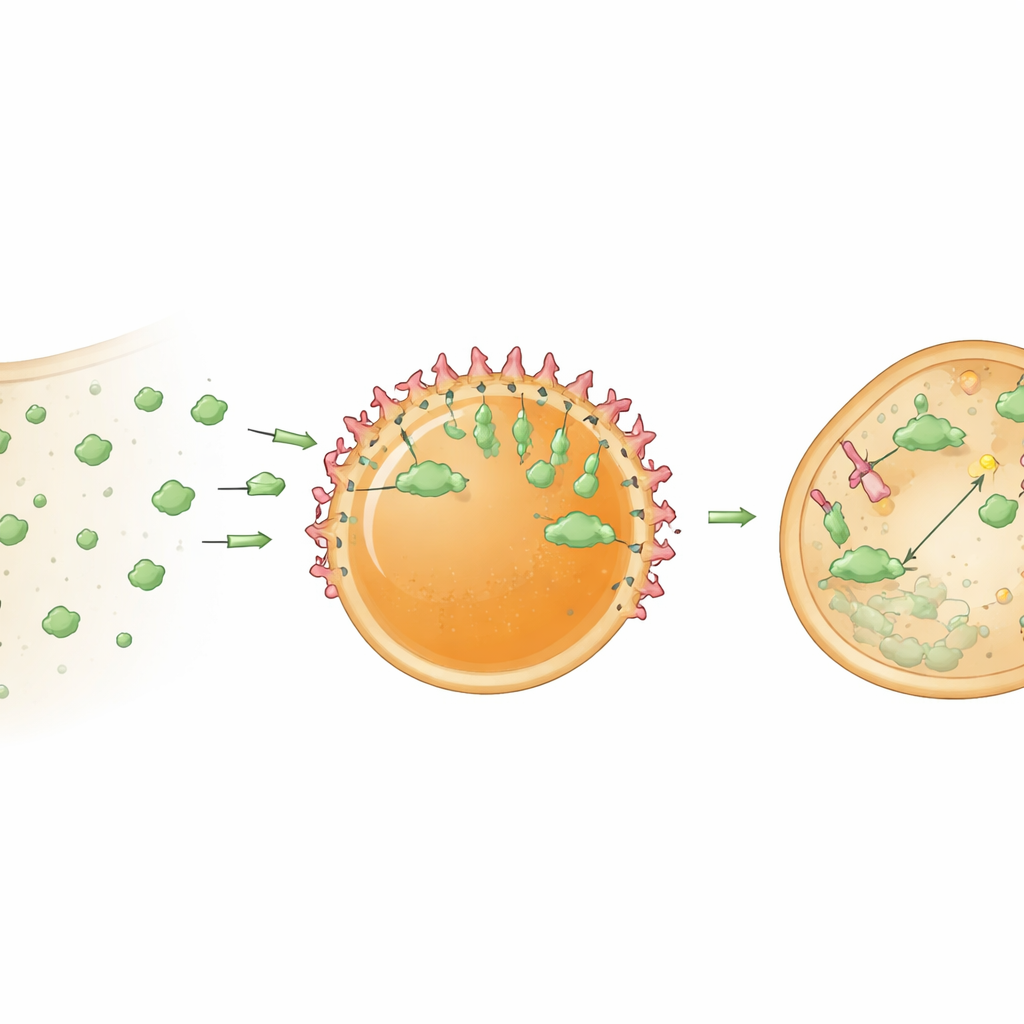
El equipo trabajó con péptidos cortos y desordenados conocidos como HBpep y una variante sensible al estado redox, HBpep‑SA. En condiciones ligeramente ácidas estos péptidos permanecen disueltos, pero cuando el pH se desplaza a niveles cercanos a los fisiológicos —o cuando la temperatura baja— se separan en fase formando gotas blandas, tipo gel, de unos 1–5 micrómetros de diámetro. Al ajustar la concentración de péptidos, los investigadores pudieron controlar tanto el tamaño como el número de gotas. Usando técnicas de fluorescencia, demostraron que las moléculas peptídicas dentro de estas gotas se mueven despacio, lo que indica un estado gelatinoso lo suficientemente resistente para sobrevivir a la dilución y manipulación. Al añadirse a cultivos de células humanas cancerosas, células de melanoma de ratón y células inmunitarias humanas primarias, las gotas se internalizaron eficientemente y se acumularon en el citoplasma. Las gotas más grandes, en particular, permanecieron intactas durante al menos cinco días, actuando efectivamente como orgánulos sintéticos de larga duración dentro de células vivas.
Cargando y dirigiendo los centros
Para que estos centros sean útiles, deben retener y organizar proteínas cargadas. Los investigadores mejoraron primero la carga añadiendo una etiqueta corta derivada de HBpep a una proteína modelo, GFP. Esta etiqueta incentivó que la GFP se repartiera fuertemente hacia las gotas y, de manera interesante, se concentrara cerca de sus superficies, creando una organización núcleo‑corteza. A continuación, incorporaron nanocuerpos —proteínas compactas similares a anticuerpos que se unen fuertemente a objetivos elegidos— dentro de las gotas. Un nanocuerpo que se une a GFP permitió que los centros capturaran selectivamente GFP tanto en tubos de ensayo como dentro de células. Dado que el gel peptídico es relativamente denso, inicialmente la mayor parte de la GFP capturada se acumuló en la superficie de la gota. Pero cuando la estructura interna se aflojó parcialmente, ya fuese cambiando las condiciones redox o favoreciendo la salida de las gotas de las membranas endosómicas que las rodeaban, la GFP también comenzó a penetrar en el interior. En células, coadyuvantes químicos que promueven la salida endosómica aumentaron mucho la fracción de centros que reclutaron con éxito sus objetivos.
Convertir centros en trituradoras de proteínas
Los autores luego mejoraron estos centros, pasando de trampas pasivas a centros de procesamiento activos. Cargaron las gotas con un bioPROTAC —una proteína de fusión que combina un nanocuerpo que liga al objetivo con parte de un adaptador enzimático que marca proteínas para su destrucción por la maquinaria de eliminación celular—. Cuando estas gotas “degradasoma” se introdujeron en células que expresan GFP de forma estable, los niveles de GFP citosólica disminuyeron en alrededor de un 78 por ciento en un día. Centros de control que contenían solo el nanocuerpo secuestraron GFP pero no redujeron apreciablemente su nivel total, confirmando que la fuerte disminución procedía de la degradación dirigida y no de la mera captura. Los resultados sugieren que agrupar bioPROTACs dentro de un microentorno concentrado los hace mucho más potentes que cuando están dispersos libremente en el citoplasma.
Qué podría significar esto para futuras terapias
En términos sencillos, este trabajo muestra que los científicos pueden fabricar gotas basadas en péptidos en un tubo de ensayo, cargarlas con herramientas proteicas a medida y luego entregarlas a células vivas donde actúan como nuevos orgánulos duraderos. Estos centros sintéticos pueden atraer selectivamente proteínas naturales y, cuando se equipan con maquinaria de degradación, pueden eliminar activamente objetivos elegidos de la célula. Debido a que esta plataforma evita alterar los genes de la célula y es modular en lo que puede transportar, abre un camino hacia terapias que restauren o reescriban el comportamiento celular —como eliminar proteínas dañinas o reconectar señales defectuosas— simplemente instalando nuevos “puestos de trabajo” programables en nuestras células.
Cita: Tu, W., Theisen, R.Q., Jin, P. et al. Delivery of peptide coacervates to form stable interaction hubs in cells. Nat Commun 17, 2250 (2026). https://doi.org/10.1038/s41467-026-68793-7
Palabras clave: orgánulos sintéticos, coacervados peptídicos, entrega intracelular, degradación de proteínas, ingeniería celular