Clear Sky Science · es
Un sistema de defensa bacteriano que apunta a la citosina modificada del ADN genómico de fagos
Cómo las bacterias superan a los virus invasores
Los virus que infectan bacterias, llamados fagos, están inmersos en una carrera armamentista constante con sus hospedadores microbianos. Muchos de estos fagos reescriben las letras químicas de su ADN para eludir las defensas bacterianas. Este estudio descubre una contramovida bacteriana hasta ahora oculta: un sistema proteico denominado CMoRE que puede reconocer y destruir el ADN fagénico que porta estas modificaciones químicas. Además de revelar un giro nuevo en la guerra microbio–virus, CMoRE podría convertirse en una herramienta precisa para detectar marcas sutiles del ADN relacionadas con enfermedades humanas.
Una etiqueta oculta en las letras del ADN
Tanto los fagos como los animales alteran a veces la letra básica del ADN, la citosina, añadiéndole pequeños grupos químicos. En muchos fagos del grupo T-even, incluido el clásico T4 que infecta a E. coli, la citosina se reemplaza por una versión modificada llamada 5-hidroximetilcitosina (5hmC), que puede ser además decorada para formar 5-glucósil-hidroximetilcitosina (5ghmC). Estos cambios ayudan a los fagos a eludir defensas bacterianas comunes que normalmente cortan el ADN “extranjero” no modificado, mientras respetan el genoma de la propia bacteria. En mamíferos, una marca relacionada, la 5hmC, se considera ahora una señal epigenética clave implicada en el control génico, la función cerebral y el cáncer, pero es muy rara y difícil de medir con precisión.
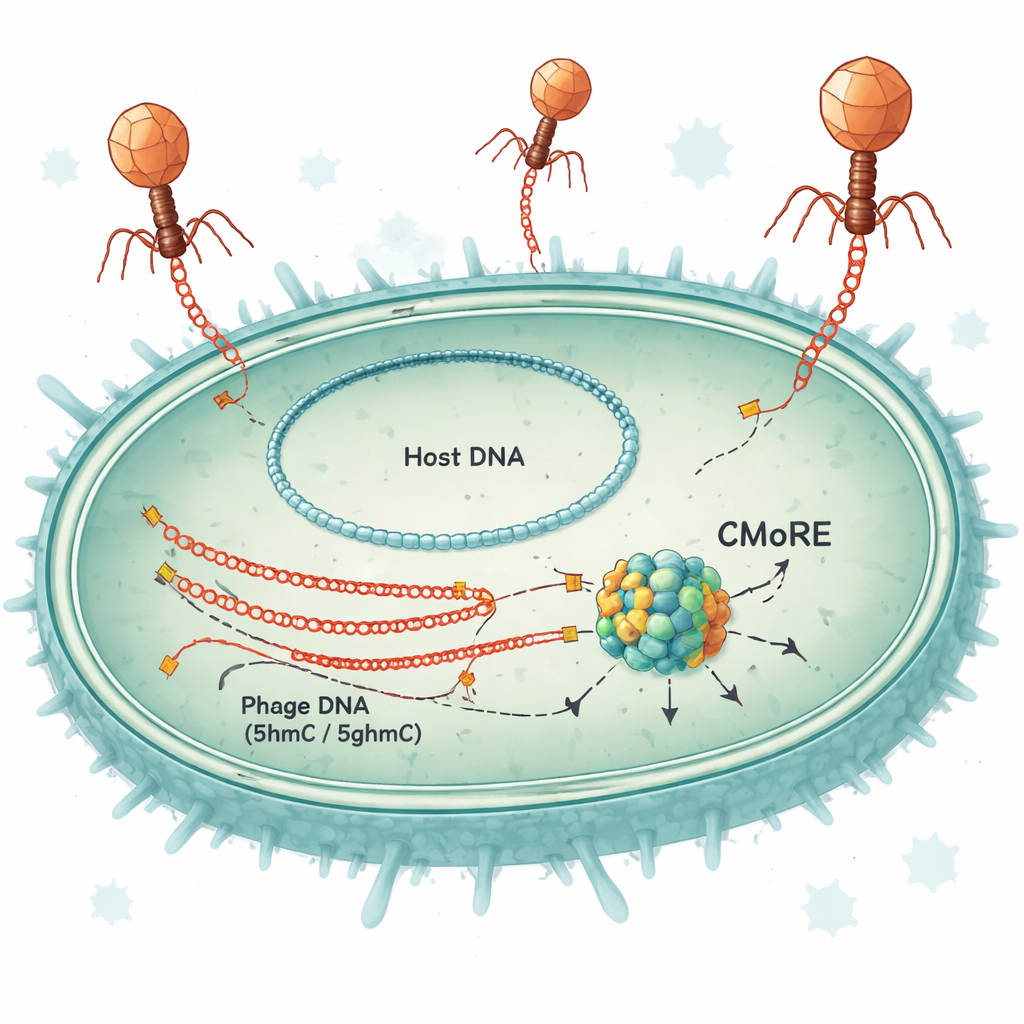
Un sistema de seguridad de una sola proteína
Los investigadores estudiaron un gen de defensa hallado originalmente en ciertas cepas de E. coli y bacterias emparentadas. Cuando introdujeron este gen —ahora renombrado CMoRE— en cepas de laboratorio que normalmente no lo poseen, las bacterias se volvieron casi completamente resistentes a varios fagos T-even, incluidos T2, T4 y T6. Bajo un intenso ataque viral, las células portadoras de CMoRE continuaron creciendo, lo que muestra que el sistema protege sin sacrificar al hospedador mediante una respuesta tipo “suicidio”. Pruebas en cultivo líquido y en placas sólidas demostraron que la infección por fagos cayó hasta aproximadamente cien mil veces, mientras que las bacterias sin CMoRE seguían siendo vulnerables.
Direccionamiento preciso del ADN viral modificado
Para ver qué corta exactamente CMoRE, el equipo purificó la proteína y la expuso a ADN de distintos fagos y de bacterias. CMoRE troceó selectivamente el ADN de fagos T-even pero dejó prácticamente intacto el ADN bacteriano. Cuando hicieron fragmentos de ADN de prueba construidos con distintas versiones de citosina, CMoRE ignoró la citosina normal y una forma metilada común (5mC), pero degradó eficientemente el ADN que contenía 5hmC o 5ghmC. Un fago T4 mutante cuyo genoma usaba citosina no modificada se volvió completamente resistente a la defensa, lo que confirma que es la modificación química —no una secuencia concreta— lo que reconoce CMoRE. El secuenciado de los fragmentos de ADN tras el corte mostró que CMoRE actúa como una enzima de restricción: une dos citosinas modificadas con un espaciado característico y realiza cortes limpios que producen salientes cortos en los extremos del ADN.
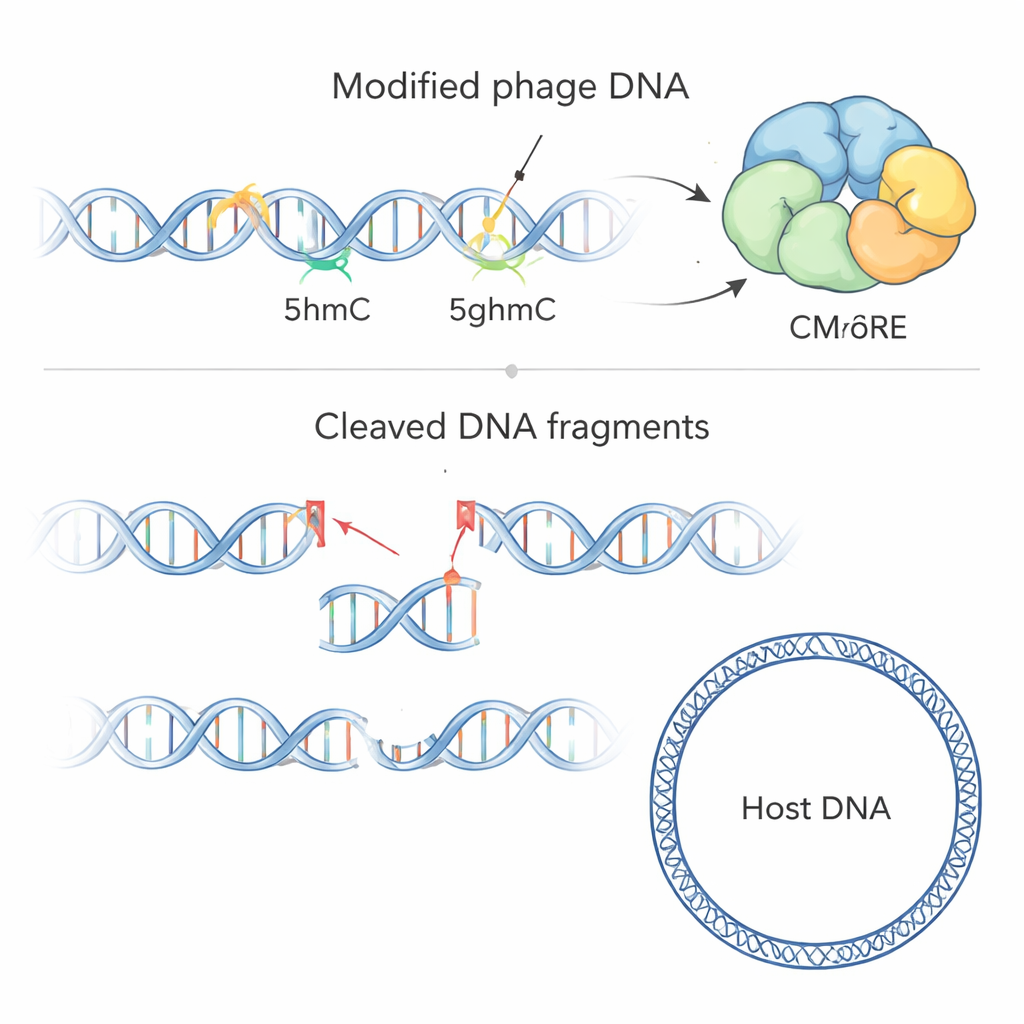
La forma y el interruptor de seguridad de CMoRE
Mediante cristalografía de rayos X, los autores resolvieron estructuras de alta resolución de CMoRE de dos especies bacterianas. La proteína está compuesta por dos partes enlazadas: una “cuchilla” N-terminal que realiza el corte del ADN, perteneciente a la familia de nucleasas GIY-YIG, y un “sensor” C-terminal que agarra la citosina modificada. Cuatro copias de CMoRE se ensamblan en un tetrámero compacto, y alterar este ensamblaje elimina en gran medida la actividad antiviral. El dominio cortador porta un motivo distintivo “GIYxY–YIG” y un bucle inusual rico en carga negativa que se proyecta sobre el sitio activo como una tapa. Cuando los investigadores neutralizaron este bucle, CMoRE se volvió hiperactivo, comenzó a atacar el ADN bacteriano normal y ralentizó el crecimiento celular: evidencia de que el bucle actúa como un freno de seguridad integrado, ayudando a la proteína a discriminar fuertemente a favor del ADN fagénico marcado con 5hmC o 5ghmC.
De la guerra microbiana a las herramientas médicas
Al explorar miles de genomas microbianos, el equipo encontró cientos de sistemas CMoRE relacionados distribuidos entre muchos grupos bacterianos, todos compartiendo las mismas características clave: la tirosina extra en el motivo catalítico y el bucle de seguridad cargado negativamente. Esto sugiere que CMoRE es una estrategia ampliamente utilizada en la lucha bacteriana contra fagos químicamente disfrazados. Debido a que CMoRE puede distinguir con claridad 5hmC y 5ghmC de la casi idéntica 5mC, y porque la proteína es estable y fácil de manejar en el laboratorio, también puede servir como un “bisturí molecular” altamente selectivo para cartografiar 5hmC en genomas de mamíferos. Eso podría mejorar las herramientas para detectar cambios epigenéticos relacionados con enfermedades, ofreciendo un rendimiento práctico derivado de entender cómo las bacterias sobreviven a sus enemigos microscópicos.
Cita: Liu, R., Tang, D., Niu, M. et al. A bacterial defense system targeting modified cytosine of phage genomic DNA. Nat Commun 17, 1920 (2026). https://doi.org/10.1038/s41467-026-68792-8
Palabras clave: defensa frente a bacteriófagos, modificación del ADN, 5-hidroximetilcitosina, enzima de restricción, epigenética