Clear Sky Science · es
La trans-corte de CRISPR-Cas9 se ve obstaculizada por un R-loop flanqueado, un espaciador alargado y un dominio HNH inactivo
Por qué importan los pequeños cortes en el ADN
CRISPR-Cas9 es famoso como un bisturí molecular capaz de cortar el ADN en puntos elegidos, pero esta herramienta tiene un segundo comportamiento menos apreciado: una vez activada, también puede mordisquear otros fragmentos de material genético en las cercanías. Comprender cuándo se activa o desactiva este corte “colateral” es crucial para crear terapias de edición genética más seguras y pruebas diagnósticas más sensibles. Este estudio diseca las características físicas del complejo Cas9–ADN–ARN que determinan si Cas9 realiza silenciosamente su corte previsto o si además empieza a degradar hebras simples de ADN sueltas.
Cómo se ponen en marcha las tijeras CRISPR
Para actuar, Cas9 se une a un fragmento corto de ARN guía que lo dirige a una secuencia de ADN coincidente en un genoma. Cuando Cas9 encuentra su diana, el ARN guía se aparea con una hebra de ADN, separando las dos hebras y creando una región híbrida ADN–ARN llamada R-loop. En su papel clásico, Cas9 corta entonces ambas hebras de ADN en ese punto. Pero trabajos recientes mostraron que, una vez activado de esta manera, el dominio catalítico RuvC de Cas9 puede también trocear ADN de hebra simple no relacionado, como tramos de poli(T), en otras partes de la solución. Los autores se propusieron preguntar: ¿qué características geométricas y estructurales precisas del ADN diana y del ARN guía hacen que esta actividad colateral sea fuerte, débil o inexistente?
Blancos cortos frente a largos: dar espacio para que Cas9 se mueva
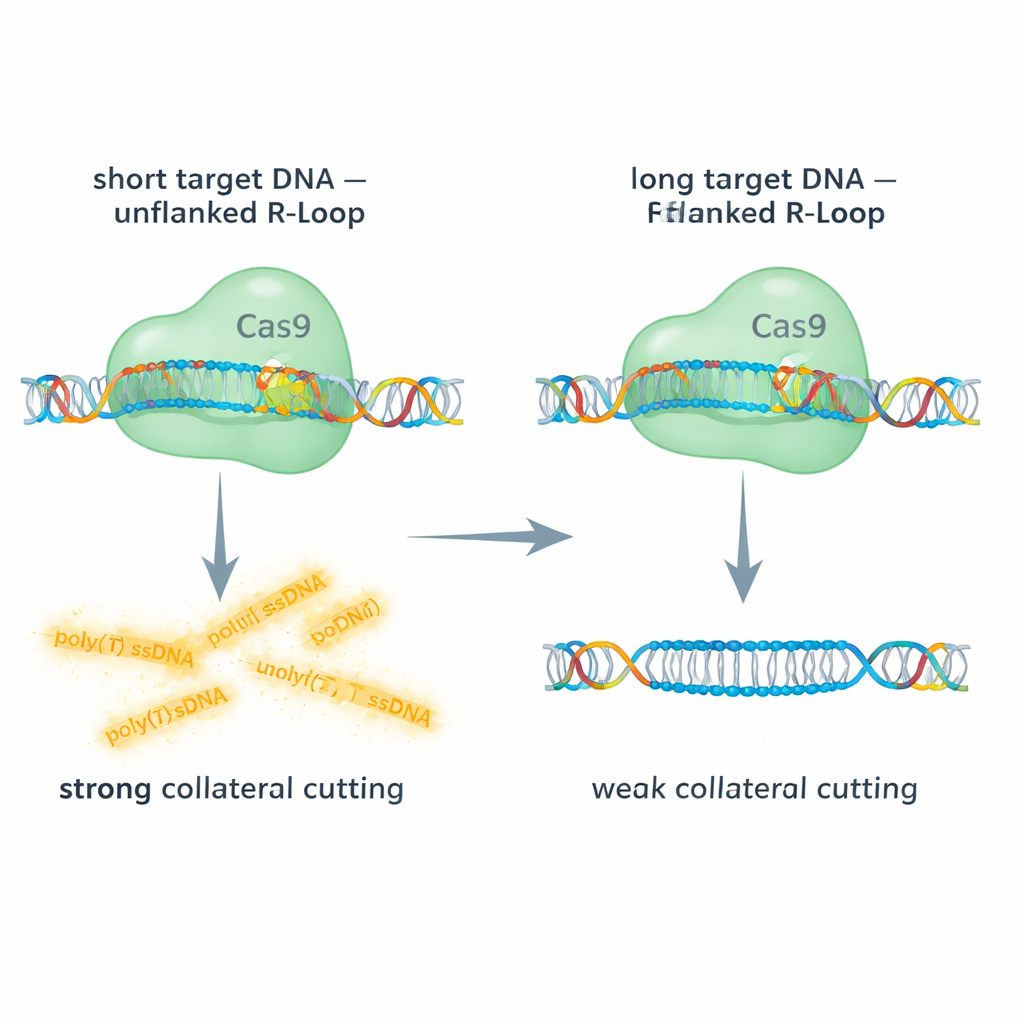
El equipo comparó la acción de Cas9 sobre dianas de ADN bicatenario cortas y largas, usando lecturas fluorescentes para seguir tanto el corte en diana como el corte colateral de una sonda de ADN de hebra simple. Con dianas cortas, el R-loop en el extremo 5′ del ARN guía está “sin flanquear”: no hay ADN doble hebra adicional más allá de la región híbrida. En estas condiciones, Cas9 mostró una robusta actividad colateral sobre ADN de hebra simple. En contraste, cuando usaron segmentos de ADN más largos que dejaban ADN bicatenario adicional flanqueando el R-loop, el corte colateral se redujo drásticamente, a veces en torno al 90%, aunque el corte principal en diana aún se produjera. Apuntar a ADN de hebra simple largo, que elimina por completo el R-loop, restauró en gran medida la actividad colateral. Estas comparaciones revelan que una “tapa” de ADN doble hebra adyacente al R-loop rigidiza el complejo y obstaculiza físicamente el acceso o la flexibilidad necesarios para que el dominio RuvC de Cas9 corte otras hebras.
Ajustes finos con la longitud del guía y los desajustes
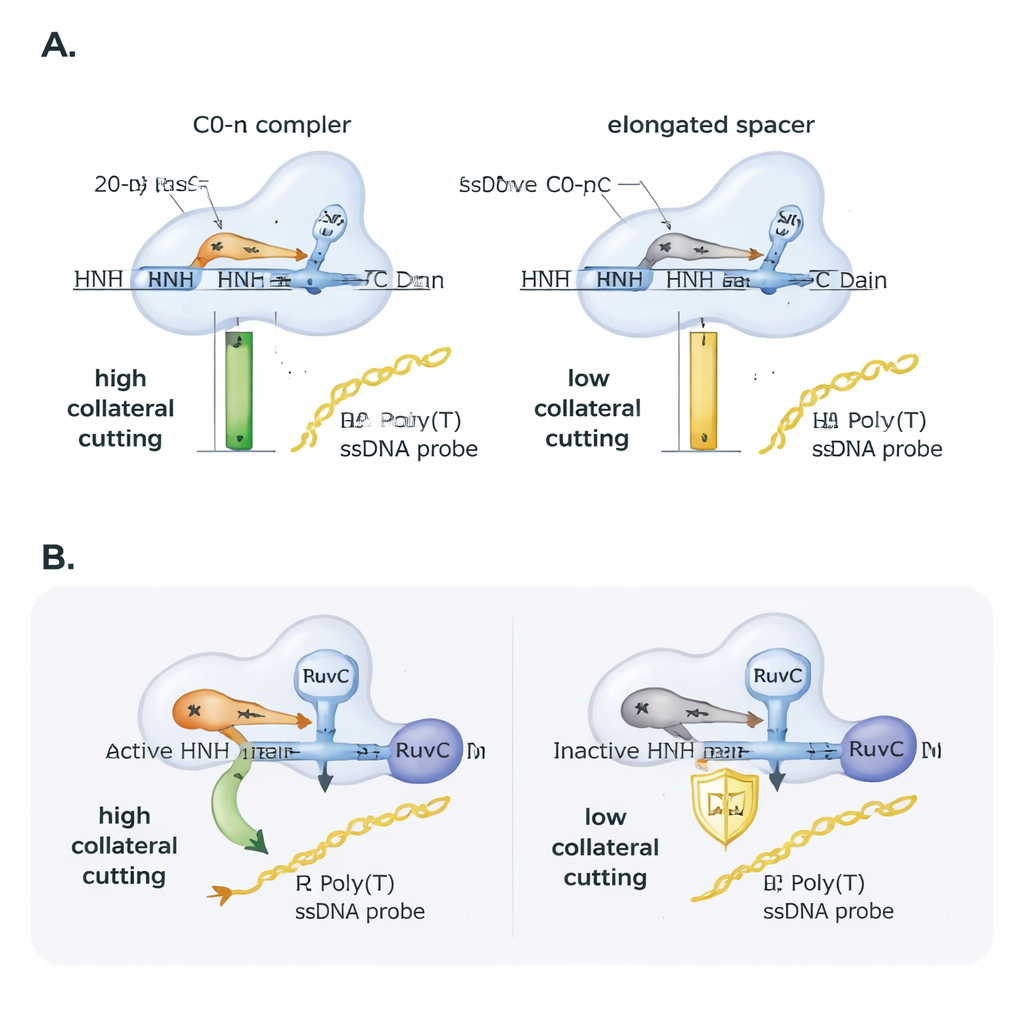
Los investigadores investigaron luego cómo el propio ARN guía modula este comportamiento. Introdujeron pequeños desajustes entre el guía y el ADN diana y midieron hasta qué punto Cas9 seguía cortando. El corte principal en diana toleró muchos desajustes de una sola base, pero el corte colateral fue más frágil y dependió decisivamente de la posición exacta del desajuste, subrayando su sensibilidad. A continuación, alargaron sistemáticamente el espaciador del ARN guía más allá de los habituales 20 nucleótidos. Aunque Cas9 todavía podía unirse y cortar el ADN diana, la actividad colateral disminuyó casi linealmente conforme aumentaba la longitud del espaciador: añadir solo dos bases extra redujo aproximadamente a la mitad la actividad colateral, y cuatro bases adicionales la disminuyeron aún más. En pruebas prácticas con material genético de SARS-CoV-2, solo los amplicones de ADN diseñados para producir un R-loop sin flanquear con un guía de longitud estándar dieron una señal colateral fuerte, lo que destaca cómo el diseño de cebadores y guías puede potenciar o arruinar los ensayos de detección basados en CRISPR.
Un dominio auxiliar esencial entre bastidores
Cas9 tiene dos dominios de corte, RuvC y HNH. Trabajos previos vincularon el corte colateral directamente a RuvC, pero este estudio muestra que HNH también importa. Cuando los autores usaron una variante de Cas9 con el dominio HNH inactivo, la actividad colateral se desplomó, aunque la unión a la diana y el comportamiento de nicking se mantuvieran. Curiosamente, si proporcionaban a Cas9 una diana de ADN que ya estaba nickeada en una hebra, la versión con HNH inactivo recuperó la actividad colateral similar a la de la enzima normal. Esto sugiere que el papel de HNH es en parte mecánico: al cortar o aflojar la hebra dirigida, ayuda a que la proteína adopte una conformación que exponga RuvC a ADN de hebra simple cercano. Los análisis estructurales de modelos 3D existentes apoyaron esta visión, mostrando que los R-loops sin flanquear y los guías de longitud estándar permiten que el extremo 5′ del ARN se “apoye” contra Cas9 y posicionen las regiones catalíticas de forma favorable, mientras que los R-loops flanqueados y los guías alargados compactan la proteína más ajustadamente y probablemente protegen el sitio RuvC de hebras sueltas.
Qué significa esto para herramientas futuras
Para no especialistas, el mensaje principal es que el comportamiento de Cas9 no es todo o nada: pequeños detalles geométricos—hasta dónde se extiende el ADN, cuánto mide el guía y si un dominio auxiliar puede completar su corte—deciden si la enzima se ciñe a su tarea principal o también destroza hebras simples próximas. Dianas cortas que dejan el R-loop sin flanquear, guías estándar de 20 bases y un dominio HNH activo promueven conjuntamente un corte colateral fuerte; ADN flanqueante largo, guías alargados o un dominio HNH inactivo lo suprimen. Estos hallazgos ofrecen a los investigadores un control más preciso para modular a Cas9, ayudándoles a diseñar sistemas de edición genética más seguros que eviten daños colaterales no deseados, o ensayos diagnósticos más potentes que aprovechen deliberadamente esta actividad colateral para detectar cantidades ínfimas de material viral o genético.
Cita: Montagud-Martínez, R., Ruiz, R., Baldanta, S. et al. CRISPR-Cas9 trans-cleavage is hindered by a flanked R-loop, an elongated spacer, and an inactive HNH domain. Nat Commun 17, 1998 (2026). https://doi.org/10.1038/s41467-026-68789-3
Palabras clave: CRISPR-Cas9, corte colateral, R-loop, espaciador de ARN guía, diagnósticos de ácidos nucleicos