Clear Sky Science · es
La adhesina que se une al colágeno restringe la infección cutánea por Staphylococcus aureus
Por qué importa el “Velcro” de un microbio de la piel
Staphylococcus aureus es la principal causa de furúnculos y abscesos cutáneos dolorosos, y las cepas resistentes a fármacos como MRSA dificultan el tratamiento de estas infecciones. Este estudio examina un giro inesperado: una proteína de la superficie bacteriana llamada Cna que actúa como Velcro para el colágeno, la principal proteína estructural del cuerpo en la piel y las heridas. En lugar de agravar la infección, los autores encuentran que esta proteína que se aferra al colágeno en realidad modera la enfermedad cutánea en ratones al condicionar cómo las células inmunitarias atacan a la bacteria.
Una proteína adhesiva con un trabajo sorprendente
El colágeno es la proteína más abundante en nuestros cuerpos y es esencial para mantener la integridad de la piel y la cicatrización. Algunas cepas de S. aureus portan Cna, una proteína que se ancla en la pared celular bacteriana y se une fuertemente al colágeno y a una cola similar al colágeno de una proteína sanguínea llamada C1q. C1q normalmente ayuda a marcar microbios para su destrucción por el sistema inmune. Trabajos anteriores asociaron Cna con infecciones graves en articulaciones y ojos, pero su papel en la enfermedad cutánea no estaba claro. Los investigadores usaron un modelo de absceso cutáneo en ratones y bacterias genéticamente modificadas que producían Cna, carecían de ella o la tenían restaurada desde un plásmido, para preguntar cómo este único adhesino cambia el curso de la infección.
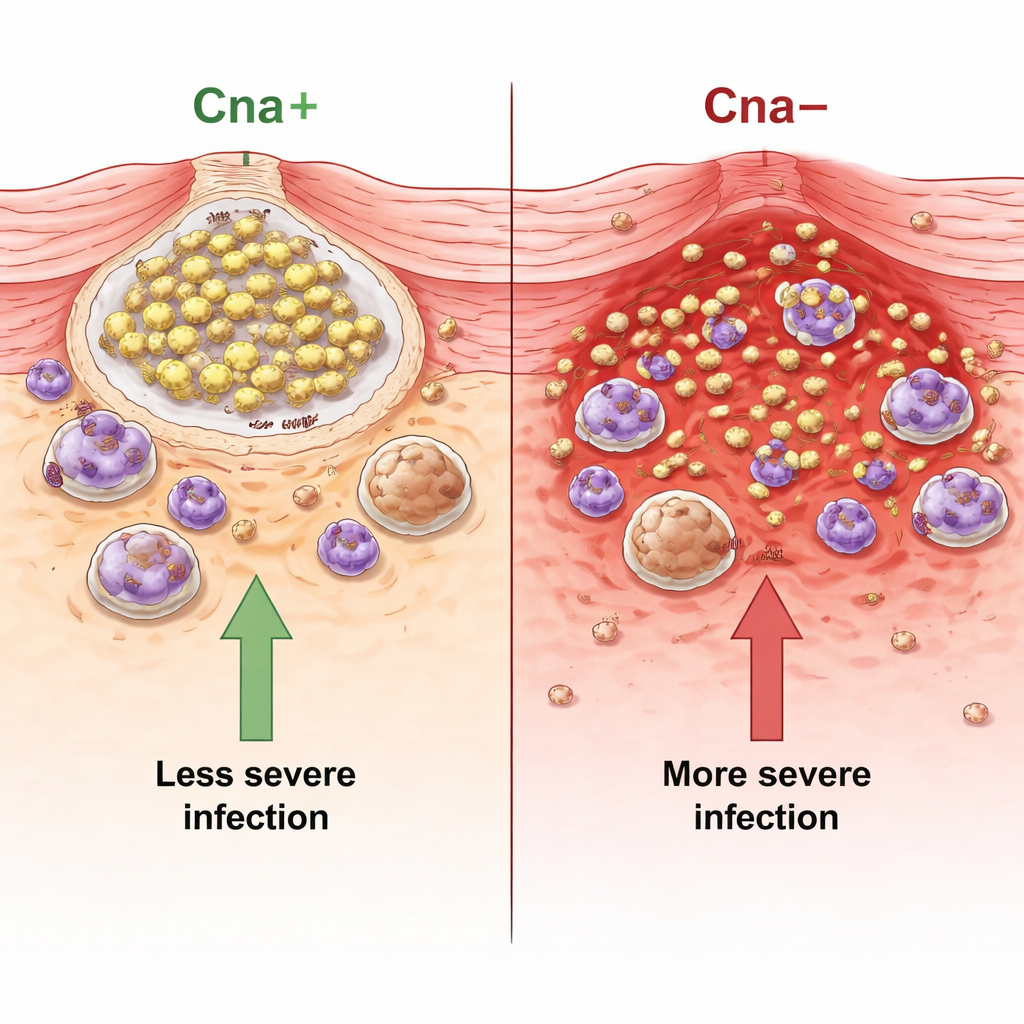
Cuando las bacterias no pueden agarrar el colágeno, las infecciones empeoran
En ratones inyectados con S. aureus positivo para Cna, las lesiones cutáneas permanecieron más pequeñas, los animales perdieron menos peso y se recuperaron muchas menos bacterias de los abscesos que en ratones infectados con mutantes negativos para Cna. La restauración de Cna revirtió estos efectos, mostrando que la propia proteína era responsable. El equipo también probó USA300, una cepa común de MRSA que carece naturalmente de Cna y es notoria en infecciones cutáneas humanas. Para esta cepa también, añadir Cna redujo el tamaño de las lesiones y el recuento bacteriano. Encuestas de aislamientos de pacientes con infecciones cutáneas, portadores nasales y neumonía revelaron que la mayoría de las cepas circulantes de S. aureus no portan el gen cna, lo que sugiere que perder esta proteína puede favorecer una enfermedad más agresiva y de mayor diseminación.
Cómo el colágeno protege a la bacteria y calma la inflamación
Las secciones de tejido de los abscesos de ratón contaron una historia clara. Las infecciones con bacterias positivas para Cna mostraron cúmulos bacterianos compactos envueltos en colágeno, con células inmunitarias como neutrófilos y macrófagos concentradas en los bordes. En contraste, las infecciones negativas para Cna eran irregulares e infiltradas, repletas de células inmunitarias muertas y con inflamación intensa. El análisis químico del tejido mostró que las infecciones sin Cna desencadenaron niveles más altos de señales inflamatorias como IL‑6, TNF‑α e IL‑1β, y de enzimas llamadas metaloproteinasas de matriz (MMP‑9 y MMP‑12) y del mediador lipídico leucotrieno B4, todos los cuales amplifican la afluencia de células inmunitarias y el daño tisular. La citometría de flujo y las imágenes confirmaron que los neutrófilos en abscesos sin Cna tenían muchas más probabilidades de estar muertos o en proceso de muerte, mientras que las células inmunitarias vivas eran relativamente escasas.
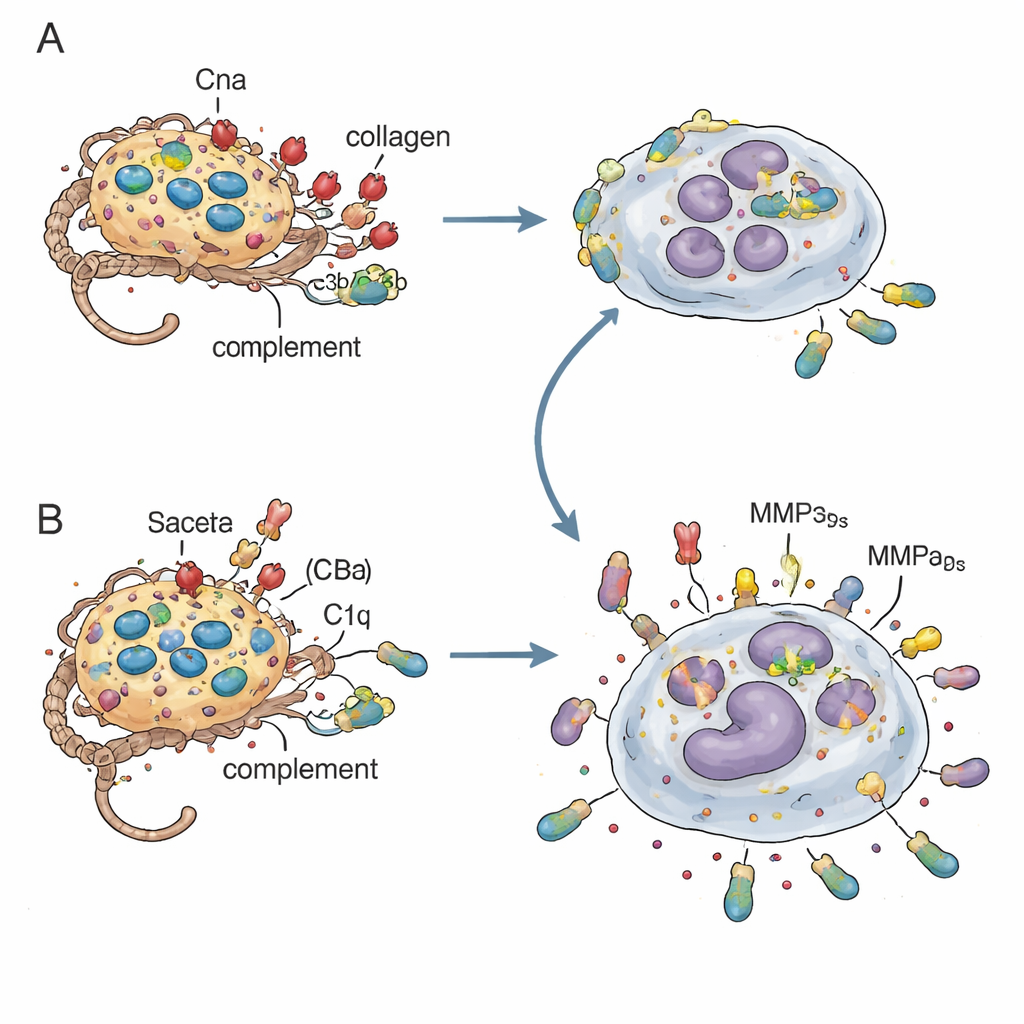
Secuestrar el complemento para evitar un abrazo letal
El vínculo mecanístico clave fue C1q, una molécula iniciadora del sistema del complemento que recubre las bacterias para que los neutrófilos puedan fagocitarlas. En experimentos in vitro, las bacterias que carecían de Cna acumularon más componentes del complemento (C4b y C3b) en su superficie y fueron captadas con mayor avidez por neutrófilos humanos. Pero esta captación excesiva resultó contraproducente: los neutrófilos cargados con bacterias sin Cna tendían a lisarse, liberando bacterias vivas y moléculas inflamatorias de vuelta al tejido. Cuando los investigadores usaron suero depletedo de C1q, o ratones genéticamente carentes de C1q, las diferencias entre infecciones positivas y negativas para Cna disminuyeron, mostrando que la unión de Cna a la cola similar al colágeno de C1q atenúa el etiquetado por complemento y modera la sobrerreacción neutrofílica. Al mismo tiempo, el colágeno que rodea a las bacterias Cna‑positivas parece crear una barrera física, ralentizando el contacto directo con los neutrófilos y permitiendo una eliminación más controlada.
Equilibrar defensa y daño en las infecciones cutáneas
Para un público no especializado, el mensaje principal es que no toda “pegajosidad” bacteriana empeora las infecciones. En este caso, las cepas de S. aureus que pueden adherirse al colágeno y a C1q provocan una respuesta inmune más mesurada: menos neutrófilos mueren de forma explosiva, la inflamación es menor y el daño cutáneo se reduce, aunque las bacterias siguen presentes. Las cepas que carecen de Cna, incluidas muchas clones importantes de MRSA, son más fácilmente señalizadas por el complemento, desencadenan una tormenta de actividad neutrofílica y acaban causando abscesos más grandes y destructivos. Comprender este fino equilibrio entre el ocultamiento bacteriano y la sobrerreacción inmune podría orientar nuevas estrategias para tratar las infecciones cutáneas: bien atacando cómo las bacterias interactúan con el colágeno y C1q, o modulando las enzimas inflamatorias y los lípidos que convierten un absceso contenido en una lesión dañina.
Cita: Bhattacharya, M., Spencer, B.L., Kwiecinski, J.M. et al. Collagen binding adhesin restricts Staphylococcus aureus skin infection. Nat Commun 17, 1980 (2026). https://doi.org/10.1038/s41467-026-68788-4
Palabras clave: Staphylococcus aureus, absceso cutáneo, colágeno, neutrófilos, sistema del complemento