Clear Sky Science · es
NatA participa en complejos multifactoriales en la salida del túnel polipeptídico ribosomal
Cómo las células afinan las proteínas recién nacidas
Cada segundo, tus células fabrican miles de proteínas nuevas en pequeñas máquinas llamadas ribosomas. A medida que emerge cada cadena proteica, debe ser recortada, etiquetada y plegada correctamente; si no, puede comportarse mal y contribuir a enfermedades. Este estudio examina uno de los sistemas de etiquetado clave, una modificación llamada acetilación N-terminal, y muestra cómo un complejo enzimático central, NatA, trabaja junto con varios socios justo donde las proteínas nuevas salen del ribosoma. Entender esta coreografía ayuda a explicar cómo las células mantienen en buen funcionamiento sus fábricas de proteínas.
La pequeña etiqueta química que importa
La mayoría de las proteínas comienzan su vida con el mismo primer bloque, el aminoácido metionina. A menudo, esta metionina inicial se elimina y se reemplaza por una pequeña etiqueta química llamada grupo acetilo. Esta etiqueta, añadida a la punta de la proteína (su N-terminal), puede influir en cuánto tiempo dura la proteína, a qué lugar de la célula se dirige y cómo funciona. Dos tipos principales de enzimas se sitúan en la salida del túnel del ribosoma para gestionar este primer arreglo: las metionina aminopeptidasas (MAPs), que cortan la metionina inicial, y las N-acetiltransferasas (NATs), que añaden la etiqueta de acetilo. Entre las NATs, NatA es la más activa en células humanas, potencialmente modificando casi el 40% de todas las proteínas. Dado que muchas proteínas se producen a la vez, la célula debe organizar estas enzimas para que el recorte y el etiquetado ocurran con rapidez y en el orden correcto.
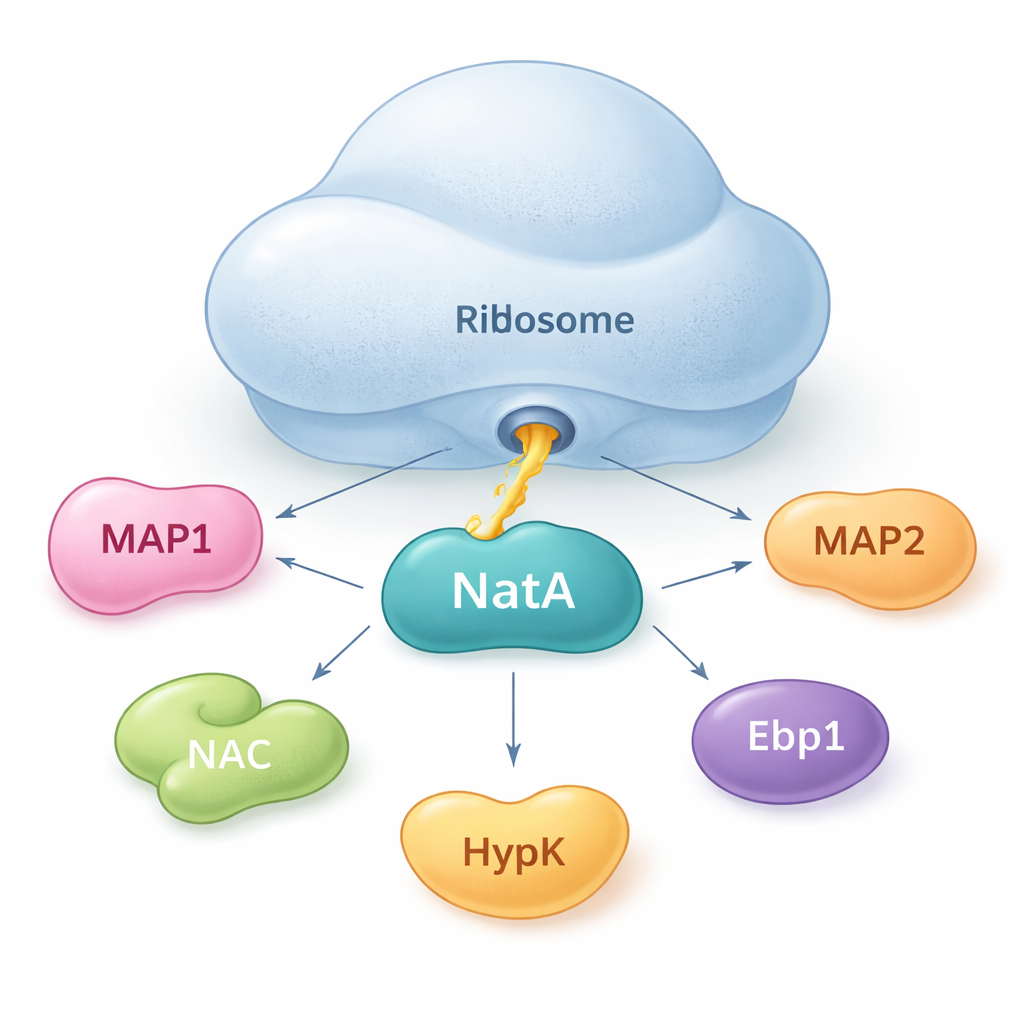
NatA como punto de encuentro para ayudantes proteicos
Los autores muestran que NatA no actúa sola. En cambio, se comporta como un centro que reúne múltiples proteínas auxiliares, tanto sobre el ribosoma como fuera de él. Utilizando mediciones de unión sensibles en solución, encontraron que NatA puede formar complejos estrechos con MAP1, el complejo asociado a polipéptidos nacientes (NAC), la proteína reguladora HypK y otra enzima, Naa50, incluso sin la presencia del ribosoma. NAC puede conectar a NatA con MAP1, permitiendo que los pasos de corte y etiquetado estén vinculados dentro de una sola ensambladura. Sin embargo, HypK, que normalmente atenúa la actividad de NatA, puede bloquear la unión de NAC. Esto sugiere que las células pueden alternar a NatA entre un estado más activo, ligado a NAC, y un estado contenido, ligado a HypK, según sus necesidades.
Un segundo punto de anclaje justo en la salida del túnel
Mediante criomicroscopía electrónica, una técnica que imagina moléculas grandes con detalle casi atómico, los investigadores descubrieron que NatA puede unirse al ribosoma en dos posiciones distintas. Un sitio, conocido previamente, se sitúa algo retirado de la salida del túnel. El sitio recién descubierto, “próximo”, coloca el núcleo catalítico de NatA muy cerca de donde emerge la cadena proteica en crecimiento, acortando la distancia que la cadena debe recorrer para ser modificada. De forma intrigante, ambas posiciones pueden estar ocupadas simultáneamente, lo que significa que dos complejos NatA pueden sentarse en el mismo ribosoma. La copia más distante actúa como andamiaje y anclaje, mientras que la copia próxima está en la posición óptima para etiquetar las proteínas nuevas. Las dos moléculas de NatA también se tocan entre sí, lo que indica que NatA puede coordinar sus propias réplicas en equipos multi-enzimáticos.
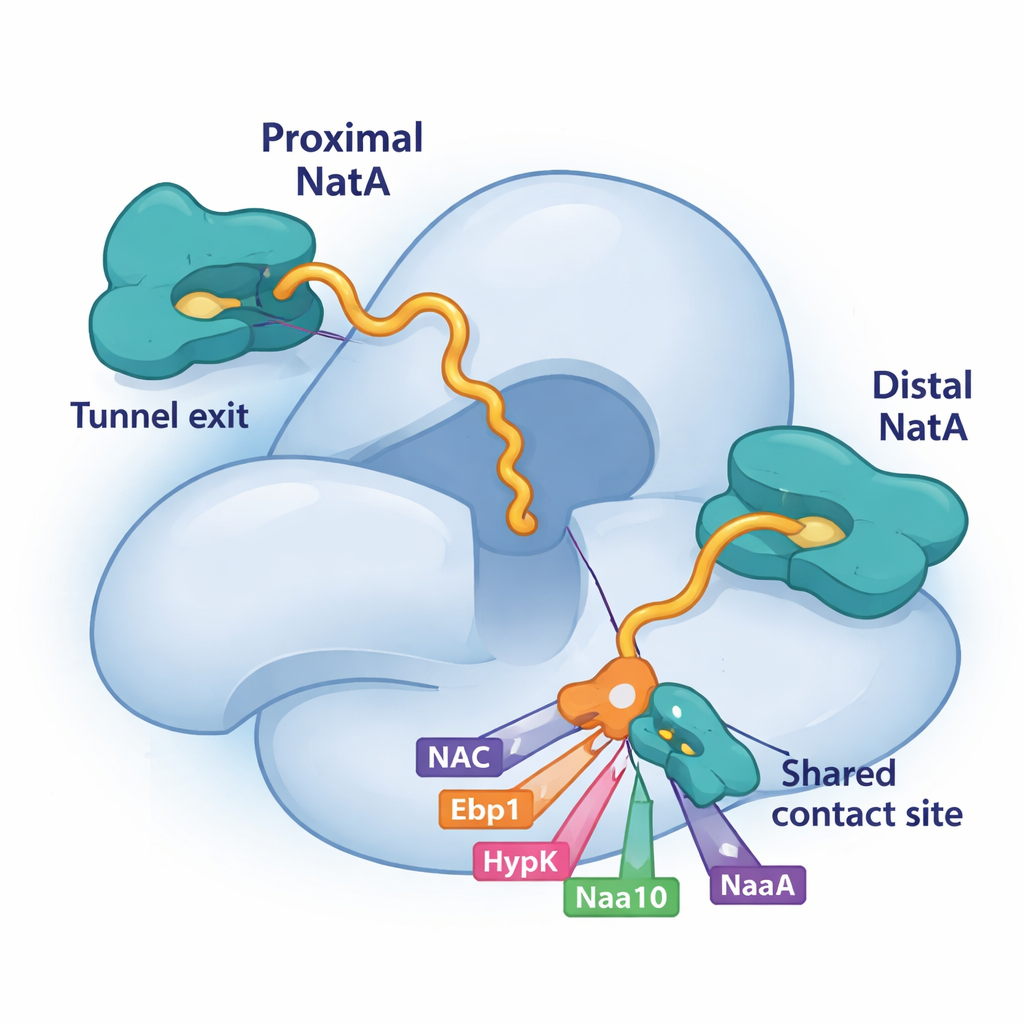
Competencia por una misma plataforma de aterrizaje en NatA
Una pieza clave de este rompecabezas es una pequeña ranura en la subunidad grande de NatA, Naa15. El estudio muestra que cuatro factores asociados al ribosoma—NAC, HypK, Ebp1 e incluso un segmento terminal de la propia subunidad catalítica de NatA, Naa10—utilizan hélices cortas para engancharse exactamente al mismo parche en Naa15. Porque todos dependen de esta plataforma compartida, deben competir por el acceso. Cuando HypK ocupa el sitio, no solo silencia la actividad de NatA sino que también impide que NatA se empareje con NAC o forme dímeros NatA–NatA. Cuando NAC, la pseudoenzima Ebp1 o Naa10 proximal se unen allí en su lugar, pueden remodelar la posición o las conexiones de NatA en el ribosoma. Esta unión competitiva ofrece a la célula una forma flexible de elegir qué socios se ensamblan alrededor de NatA en cada momento.
Una pseudoenzima como controladora del tráfico
La proteína Ebp1 resulta especialmente intrigante. Se parece a una de las enzimas que eliminan la metionina pero carece de actividad catalítica; es una “pseudoenzima”. Trabajos anteriores mostraron que Ebp1 puede situarse en el ribosoma cerca de la salida del túnel y sujetar un tramo largo de ARN. En este estudio, los autores encuentran que cuando NatA se une al ribosoma, Ebp1 cambia de posición, suelta el ARN y, en su lugar, utiliza su propia hélice para ocupar el mismo sitio de unión en Naa15 que usan NAC y HypK. Este reordenamiento sugiere que Ebp1 puede actuar como un marcador temporal u organizador: puede moldear el entorno local del ARN y luego ceder el control a enzimas activas como las MAPs y NatA, sin realizar química directamente.
Por qué importa este control molecular de la aglomeración
Para un no especialista, los detalles de hélices y sitios de unión pueden sonar abstractos, pero el mensaje es simple: las células ejecutan un sistema de control de calidad multi-step, altamente coreografiado, justo donde nacen las proteínas. NatA se sitúa en el centro de este sistema, capaz de reclutar o liberar distintos socios según qué factores ganen acceso a un parche de acoplamiento crucial y qué sitio ribosomal ocupe NatA. Esta red flexible ayuda a asegurar que el recorte y la acetilación ocurran con el tiempo y el orden adecuados para miles de proteínas distintas. Dado que los errores en el procesamiento N-terminal se asocian con trastornos del desarrollo, neurodegeneración y cáncer, mapear cómo NatA y sus socios se ensamblan ofrece a los investigadores un plan más claro de cómo se controla el procesamiento temprano de proteínas y cómo podría dirigirse cuando falla.
Cita: Klein, M., Wild, K., McTiernan, N. et al. NatA engages in multi-factor complexes at the ribosomal polypeptide tunnel exit. Nat Commun 17, 884 (2026). https://doi.org/10.1038/s41467-026-68787-5
Palabras clave: control de calidad de las proteínas, acetilación N-terminal, salida del túnel ribosomal, complejo NatA, modificación cotraduccional