Clear Sky Science · es
La fucosiltransferasa vegetal FUT11 deforma el aceptor de azúcar para catalizar mediante un intermedio oxocarbenio transitorio
Cómo las plantas ajustan finamente los azúcares de sus proteínas
Las proteínas en nuestras células, y en las plantas, suelen estar adornadas con cadenas complejas de azúcares que actúan como códigos, orientando cómo se pliegan esas proteínas, cuánto duran y con qué parejas pueden interaccionar. Este estudio se centra en una enzima vegetal llamada FUT11 que añade un azúcar pequeño, la fucosa, a estas cadenas. Al desvelar exactamente cómo funciona FUT11 a nivel atómico, los autores revelan un truco sorprendente: la enzima dobla brevemente su partner azucarado fuera de forma para impulsar un paso químico difícil. Entender este proceso importa no solo para la biología básica, sino también para diseñar medicamentos producidos en plantas que eviten desencadenar reacciones inmunitarias indeseadas en humanos.
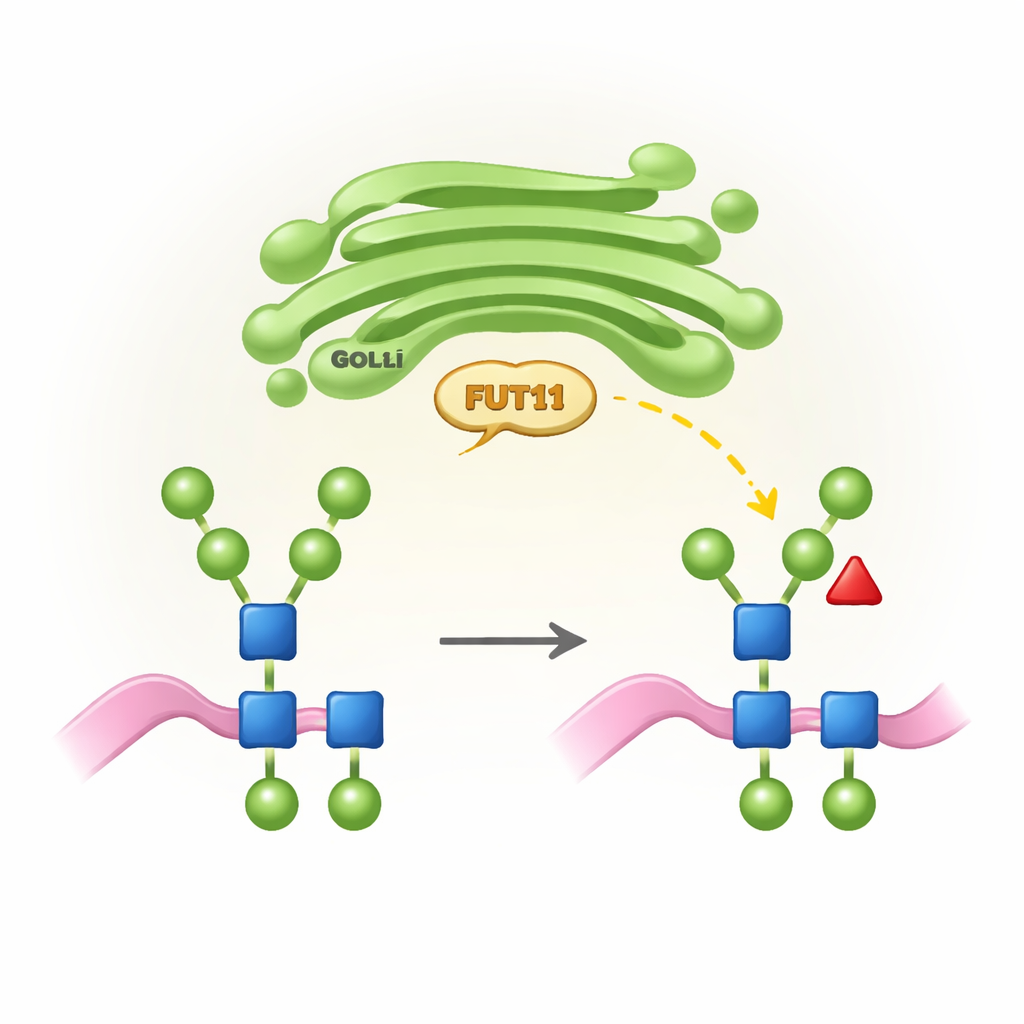
Etiquetas azucaradas específicas de las plantas y por qué importan
Todos los organismos superiores usan un proceso llamado N-glicosilación para unir cadenas de azúcares (N-glicanos) a puntos concretos de las proteínas. En animales, estas cadenas se remodelan en el aparato de Golgi en estructuras elaboradas que a menudo terminan en ácidos siálicos y llevan una fucosa central en una posición específica. Las plantas, sin embargo, siguen una “regla de diseño” distinta: sus N-glicanos suelen carecer de ácido siálico pero llevan una fucosa central en otra posición (denominada b1,3) además de una xilosa adicional. Estas características propias de las plantas son esenciales para el crecimiento y la fertilidad normales, pero pueden ser percibidas como extrañas por el sistema inmunitario humano. FUT11 es una de las enzimas vegetales clave que instala esta fucosa central, y su actividad modela tanto el desarrollo vegetal como la manera en que las proteínas terapéuticas producidas en plantas serán percibidas por nuestro organismo.
Mapeo de dónde puede actuar FUT11 en ramas complejas de azúcares
Para entender qué reconoce FUT11, los investigadores probaron la enzima en un microarray con 144 estructuras diferentes de N-glicanos. Encontraron que FUT11 es bastante selectiva respecto a una rama del árbol de azúcares —el denominado brazo b1,3— que debe portar un bloque constructivo particular (una N-acetilglucosamina terminal, o GlcNAc) para que la reacción progrese. Al mismo tiempo, FUT11 tolera otras decoraciones: sigue funcionando cuando la manosa central lleva una xilosa exclusiva de plantas, e incluso cuando ya se ha añadido otra fucosa en la posición típica de mamíferos en el núcleo. La rama opuesta (b1,6) queda mayormente expuesta al solvente y establece solo contactos débiles con la enzima, lo que explica por qué FUT11 puede aceptar una amplia variedad de modificaciones allí. Estas preferencias de unión ayudan a explicar por qué las plantas producen un conjunto característico de estructuras de N-glicanos y muestran cómo FUT11 podría usarse o evitarse al diseñar células vegetales para biotecnología.
Un diseño estructural único para agarrar y posicionar azúcares
Mediante cristalografía de rayos X, el equipo resolvió la estructura tridimensional de FUT11 ligada a su donante de azúcar (GDP-fucosa) y a un aceptor N-glicano. La enzima presenta una arquitectura “GT-B” de dos lóbulos: un lóbulo acuna la GDP-fucosa, mientras que un lóbulo aceptador inusualmente elaborado, que incluye un subdominio N-terminal específico de plantas, envuelve el N-glicano. Este subdominio extra, unido al resto de la enzima por puentes disulfuro, ancla la parte central del glicano y ayuda a presentar la unidad reactiva GlcNAc hacia el donante. Mutar aminoácidos clave confirmó sus roles: cambiar un solo glutamato (Glu158) eliminó la actividad, mientras que alterar dos residuos cercanos debilitó considerablemente la fucosilación en células humanas modificadas. Estos resultados conectan las instantáneas estructurales con la función celular real, mostrando exactamente qué partes de la proteína son indispensables para la unión y la catálisis.
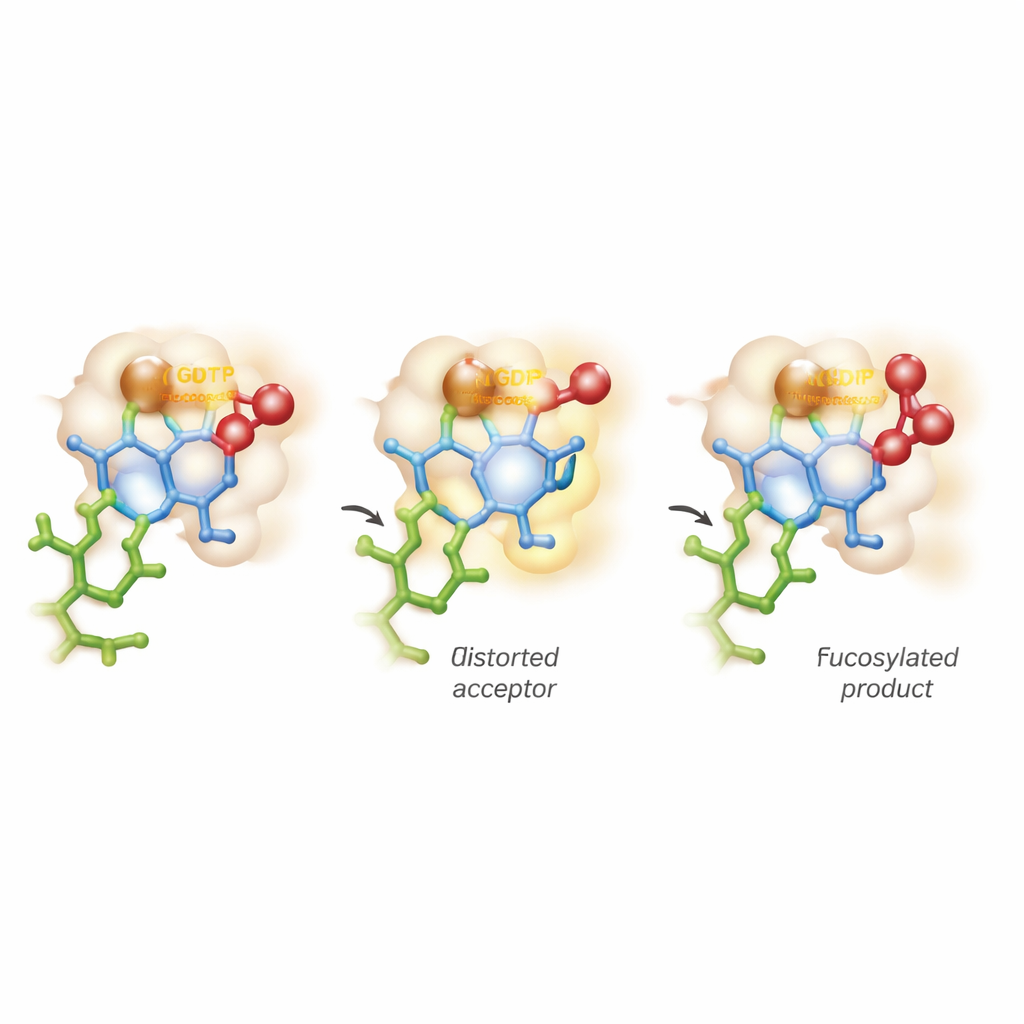
Deformar el azúcar y caminar la línea entre dos vías reactivas
La percepción más llamativa proviene de simulaciones informáticas avanzadas que combinan mecánica cuántica y dinámica molecular. Las visiones tradicionales asumen que el azúcar aceptor mantiene su forma estable, tipo silla, mientras la enzima simplemente activa el donante. Aquí, FUT11 actúa con mayor agresividad: interacciones mediadas por Glu158 distorsionan temporalmente el anillo interior de GlcNAc hacia una conformación más forzada y poco cómoda. En esta postura tensa, el grupo hidroxilo crítico queda perfectamente alineado para atacar al donante de fucosa. Los cálculos revelan que, a medida que el enlace químico con el GDP se rompe, aparece un estado de corta vida y carga positiva semejante a un oxocarbenio sobre el azúcar, antes de que el nuevo enlace al aceptor se complete. Esto significa que la reacción no encaja limpiamente en las categorías SN1 o SN2 de libro, sino que progresa a lo largo de un continuo, de forma asincrónica y casi por pasos.
Flexibilidad oculta y ecos evolutivos
Al comparar FUT11 con una enzima humana relacionada, FUT9, los autores hallaron que la enzima vegetal puede también, aunque débilmente, modificar otro tipo de motivo azucarado (LacNAc) para formar una estructura conocida como Lewis X. Esta actividad secundaria probablemente no es biológicamente relevante en plantas, donde Lewis X no suele aparecer, pero destaca cómo andamiajes proteicos similares pueden reutilizarse a lo largo de la evolución para actuar sobre contextos azucarados distintos. El estudio sugiere que FUT11 y sus parientes comparten un marco modular para reconocer N-glicanos, con ajustes sutiles que desplazan la especificidad entre núcleos vegetales y antenas animales.
Por qué este truco de deformación importa para la ciencia y la medicina
En conjunto, el trabajo muestra que FUT11 hace más que acercar dos socios azucarados: deforma activamente el azúcar aceptor hasta una pose reactiva y canaliza la química a través de un intermedio cargado y fugaz. Para un lector general, esto significa que el azúcar en la proteína no es un punto de anclaje rígido, sino un participante flexible que la enzima moldea según sus necesidades. Esta nueva visión de la “catálisis conformacional” ayuda a entender cómo las enzimas alcanzan velocidad y selectividad, y ofrece un plano para rediseñar vías de glicosilación. En términos prácticos, conocer exactamente cómo FUT11 reconoce y modifica los N-glicanos vegetales puede orientar la ingeniería de cultivos y de sistemas de producción basados en plantas para minimizar patrones azucarados que desencadenan respuestas inmunitarias en terapias humanas, o para crear glicoproteínas de diseño con propiedades biológicas a medida.
Cita: Taleb, V., Sanz-Martínez, I., Serna, S. et al. Plant fucosyltransferase FUT11 distorts the sugar acceptor to catalyze via a transient oxocarbenium intermediate mechanism. Nat Commun 17, 1960 (2026). https://doi.org/10.1038/s41467-026-68786-6
Palabras clave: glicosilación vegetal, fucosiltransferasa FUT11, N-glicanos, mecanismo enzimático, glicoingeniería