Clear Sky Science · es
Base estructural e implicaciones patológicas del complejo básico ERAD dimerico OS9-SEL1L-HRD1
El equipo de limpieza celular bajo el microscopio
Dentro de cada una de nuestras células, una fábrica muy activa convierte las instrucciones genéticas en proteínas funcionales. Como en cualquier fábrica, ocurren errores. Cuando las proteínas se pliegan de forma incorrecta, pueden atascar el sistema y contribuir a la enfermedad. Este estudio se centra en una de las principales máquinas de control de calidad celular: el complejo SEL1L‑HRD1, para revelar su estructura tridimensional detallada y mostrar cómo pequeños cambios genéticos pueden romper esta maquinaria y, potencialmente, conducir a enfermedades humanas.
Una cinta transportadora oculta en la célula
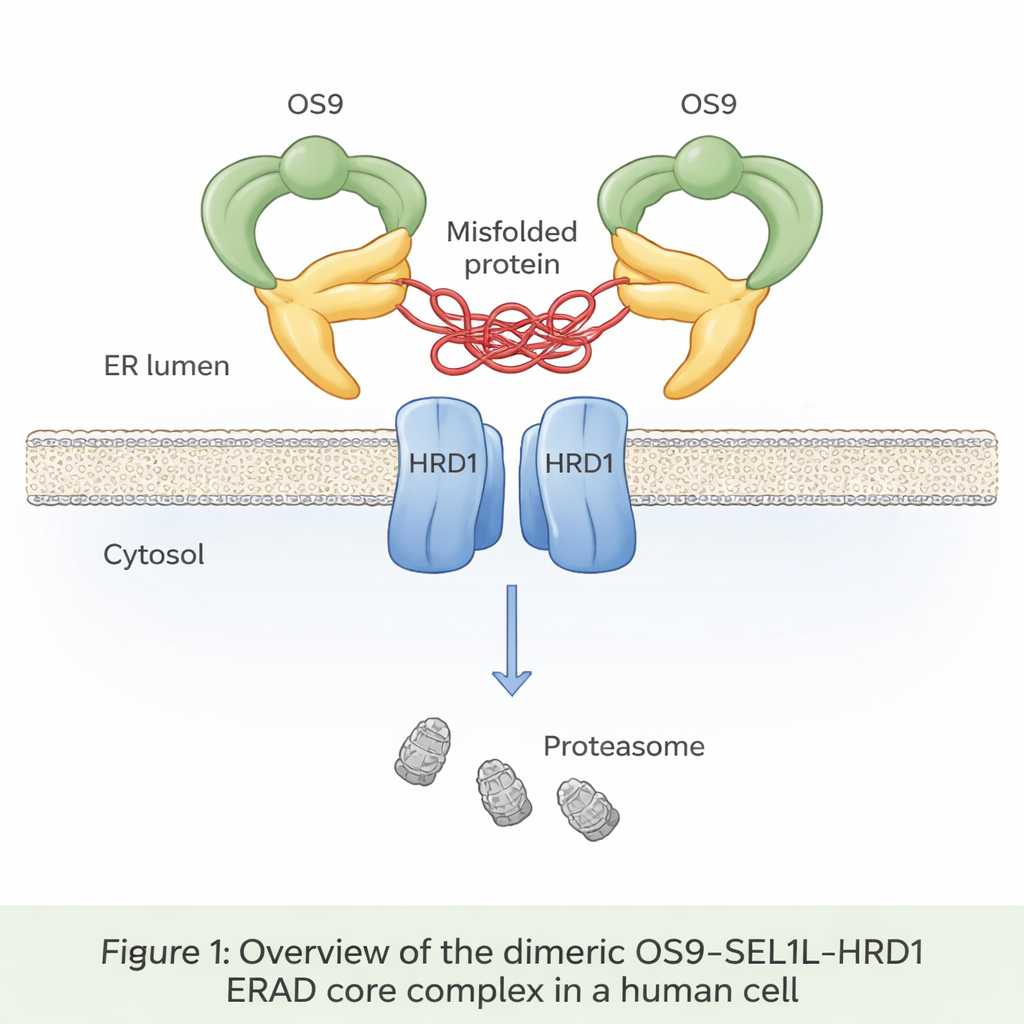
Hasta un tercio de todas las proteínas recién sintetizadas entran en un compartimento llamado retículo endoplásmico, o RE, donde se pliegan y se comprueban. Las proteínas mal plegadas suelen ser reconocidas, retrotraídas fuera del RE y destruidas en un proceso conocido como degradación asociada al RE (ER‑associated degradation, ERAD). En el centro de una vía principal de ERAD se encuentra un trío de proteínas: OS9, SEL1L y HRD1. OS9 actúa como sensor de proteínas defectuosas con etiquetas de azúcar; SEL1L sirve de andamiaje; y HRD1 marca las proteínas condenadas con pequeñas banderas de ubiquitina que las señalan para su destrucción por las unidades de eliminación celular, los proteasomas. Hasta ahora, sin embargo, nadie había observado con detalle atómico cómo encajan estas tres piezas en las células humanas.
Revelando la forma de la máquina central
Los autores emplearon crio‑microscopía electrónica, una técnica que imagen moléculas congeladas al instante a resolución casi atómica, para visualizar el complejo OS9‑SEL1L‑HRD1 purificado de células humanas. Descubrieron que forma un dímero: esencialmente dos copias idénticas unidas, en lugar de permanecer como unidades simples. En el lado luminal del RE (el interior del RE), dos moléculas de OS9 y dos de SEL1L se ensamblan en un anillo con forma de pinza de cangrejo con una abertura central que parece diseñada para agarrar proteínas mal plegadas. Dentro de la membrana, dos moléculas de HRD1 se emparejan para formar un canal compartido. Esta disposición sitúa la «pinza» directamente sobre la puerta formada por HRD1, creando un camino continuo para que las proteínas mal plegadas se desplacen desde la luz del RE, a través de la membrana, y hacia la degradación en el citosol.
Cómo pequeños cambios rompen un gran sistema
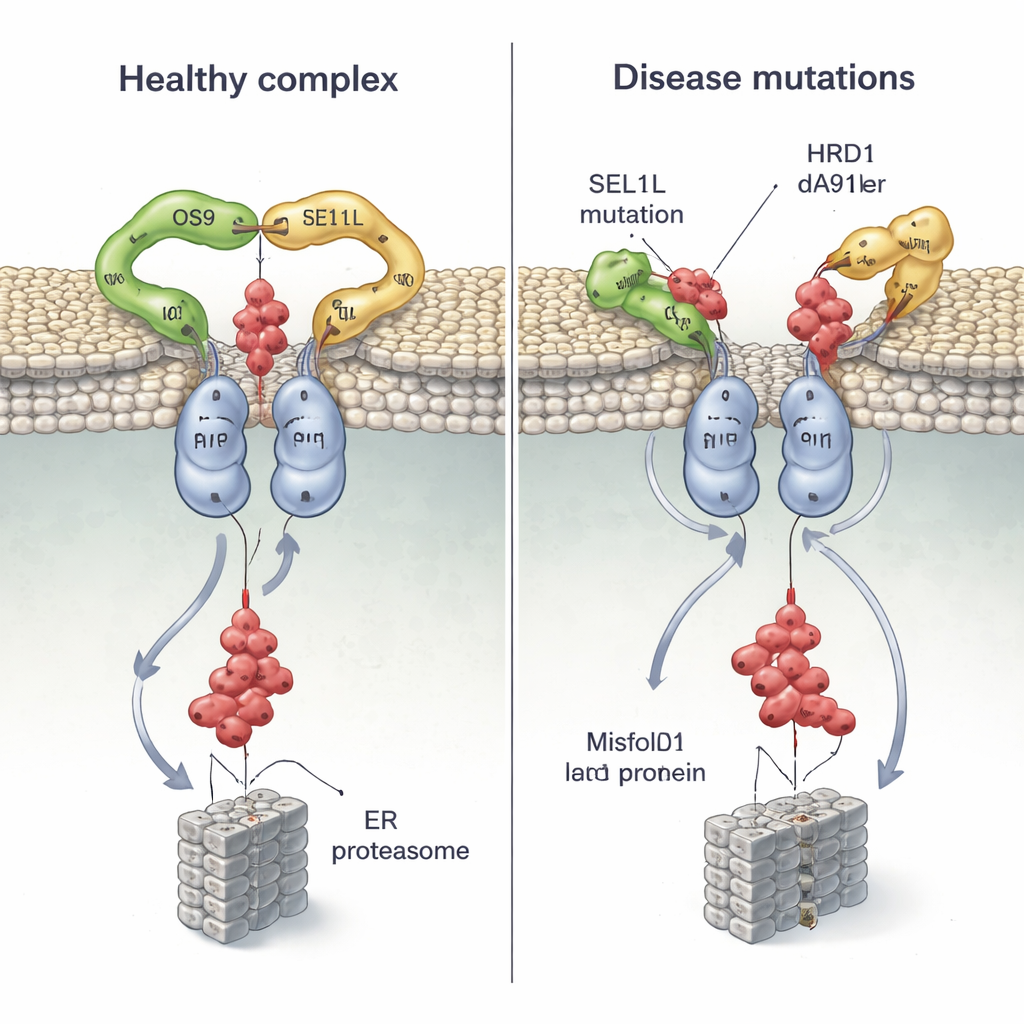
Dado que se han encontrado mutaciones en SEL1L y HRD1 en pacientes con trastornos neurodesarrollativos graves y otras enfermedades, el equipo mapeó varias variantes relacionadas con la enfermedad sobre su estructura y probó cómo se comportan en células. Dos mutaciones de SEL1L, G585D y S658P, se ubican justo en los puntos de contacto con OS9 y HRD1, respectivamente. En experimentos celulares, G585D casi abolió la capacidad de SEL1L para unirse a OS9, mientras que S658P debilitó considerablemente su unión a HRD1; la combinación de ambas mutaciones esencialmente rompió el complejo central, aunque dejó intactos a otros asociados. Como resultado, las células tuvieron dificultades para marcar y eliminar el precursor hormonal mal plegado, permitiendo que las proteínas defectuosas persistieran.
Una mutación patológica en el canal de la membrana
La estructura también muestra que el segmento transmembrana 3 de HRD1 es la interfaz clave donde dos moléculas de HRD1 se encuentran para formar el canal. Los investigadores introdujeron «asas» de cisteína en posiciones específicas y usaron reticulación química para confirmar que estas regiones entran en contacto cercano en células vivas, demostrando que HRD1 realmente dimeriza in vivo. Cuando perturbaron un único residuo altamente conservado (T93) en esta interfaz, el dímero se deshizo y la actividad de ERAD colapsó, a pesar de que el complejo seguía ensamblándose con OS9 y SEL1L. Luego examinaron una variante recién descrita en un paciente, HRD1 A91D, encontrada en un niño con problemas cardiacos y pulmonares. Este cambio, también en la interfaz de dímero, redujo la dimerización de HRD1 aproximadamente a la mitad e impidió gravemente la eliminación de proteínas mal plegadas, de nuevo sin alterar la unión global de los asociados.
Una nueva visión del control de calidad de proteínas y la enfermedad
Al combinar biología estructural con ensayos celulares, este trabajo muestra que el complejo OS9‑SEL1L‑HRD1 opera como una máquina emparejada y dimérica: un captor con forma de pinza vinculado a un canal compartido que transporta proteínas defectuosas fuera del RE. Las mutaciones que aflojan el agarre de la pinza o desestabilizan el par HRD1 no solo ajustan la eficiencia: pueden atascar el sistema, permitiendo que las proteínas dañadas se acumulen y contribuyan a la enfermedad humana. Para el público no especializado, el mensaje clave es que incluso cambios de una sola letra en nuestro ADN pueden deformar sutilmente la forma de máquinas celulares esenciales, con consecuencias de gran alcance para el desarrollo cerebral, la inmunidad y la función de los órganos.
Cita: Lin, L.L., Maldosevic, E., Zhou, L.E. et al. Structural basis and pathological implications of the dimeric OS9-SEL1L-HRD1 ERAD Core Complex. Nat Commun 17, 2064 (2026). https://doi.org/10.1038/s41467-026-68777-7
Palabras clave: control de calidad de proteínas, retículo endoplásmico, ERAD, complejo SEL1L-HRD1, desplegamiento de proteínas