Clear Sky Science · es
Perfiles de eliminación de exones a nivel unicelular revelan eventos de splicing que moldean la expresión génica y la dinámica del estado celular
Cómo pequeños cambios en el ARN pueden alterar el comportamiento celular
Nuestras células leen y empalman continuamente las instrucciones de ARN para decidir qué proteínas producir y cómo responder al estrés, crecer o dividirse. Este estudio muestra que cambiar piezas muy pequeñas de esos mensajes de ARN —segmentos individuales llamados exones— puede remodelar fuertemente la actividad génica e incluso desplazar la manera en que las células avanzan por el ciclo celular. El trabajo presenta una herramienta potente que permite a los científicos explorar muchas de estas pequeñas decisiones de ARN a la vez, célula por célula, abriendo nuevas vías para entender enfermedades y descubrir dianas farmacológicas.
Recortando palabras seleccionadas del guion genético
Los genes están escritos como largas secuencias de ADN, pero las células no los leen de forma lineal. En su lugar, recortan y pegan bloques más pequeños, llamados exones, para construir un mensaje de ARN. Al elegir qué exones conservar, las células pueden generar varias versiones proteicas a partir de un mismo gen, de forma similar a producir distintos montajes de una película a partir del mismo metraje. Muchas enfermedades, incluido el cáncer y el autismo, están asociadas a errores en este proceso; sin embargo, para la mayoría de las elecciones de exones todavía desconocemos su función real. Los autores se propusieron resolver esto construyendo un sistema a gran escala que puede eliminar exones específicos de muchos genes y luego observar, en miles de células individuales a la vez, cómo esos recortes afectan la red interna de la célula.
Un "motor de búsqueda" unicelular para la función de exones
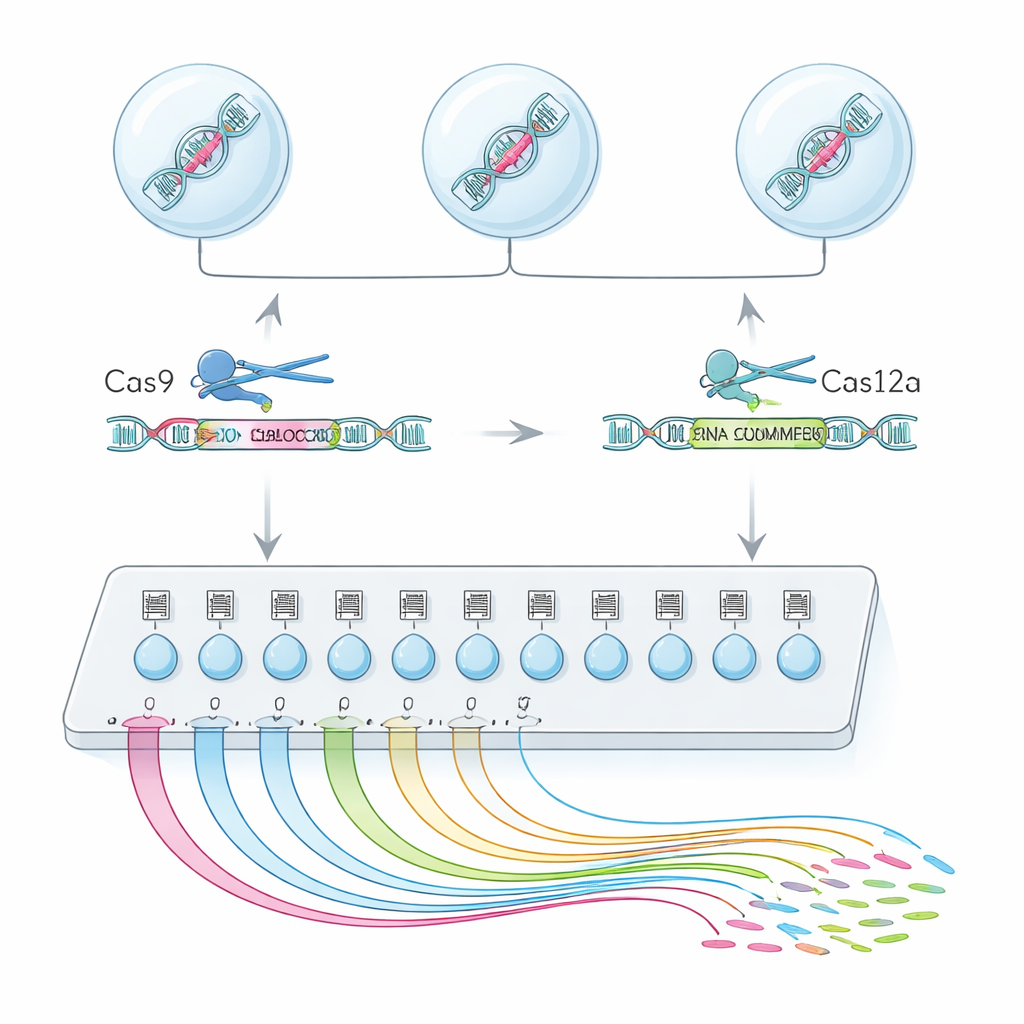
Para lograrlo, el equipo combinó dos enzimas de edición del genoma, Cas9 y Cas12a, en una plataforma híbrida llamada CHyMErA. Cada enzima es guiada hacia el ADN por cortas "direcciones" de ARN. Al dirigir las dos enzimas para cortar justo antes y justo después de un exón elegido, pueden eliminar limpiamente ese segmento dejando intacto el resto del gen. El nuevo método, scCHyMErA-Seq, vincula este corte preciso con la tecnología de secuenciación de ARN unicelular. El ARN de cada célula se captura en una gota junto con un código de barras y las guías de ARN que especifican qué exón fue eliminado. La secuenciación revela entonces, para decenas de miles de células, tanto la edición que recibió cada célula como el patrón detallado de genes que activó o silenció.
Ingeniería de la herramienta para ver ambas hojas de las tijeras
Un desafío clave fue detectar de manera fiable las guías de Cas12a junto a las de Cas9 en el mismo experimento unicelular. Los diseños iniciales o bien no capturaban las guías de Cas12a o perjudicaban la eficiencia de edición. Los investigadores solucionaron esto rediseñando cuidadosamente la secuencia del mango de Cas12a para eliminar tramos que detenían prematuramente la transcripción, y añadiendo un pequeño elemento estabilizador de ARN y un paso de amplificación dirigido. Estos ajustes aumentaron la capacidad de detectar ambas guías en cerca del 90 por ciento de las células, al tiempo que preservaban una fuerte eliminación de exones. Con esta configuración optimizada, los autores cribaron 224 exones alternativos en 161 genes humanos, perfilando más de 200.000 células individuales de alta calidad.
Descubriendo exones que controlan programas génicos y ciclos celulares
Al comparar la actividad génica de las células editadas con controles, casi la mitad de los exones evaluados provocaron cambios sustanciales en cientos de otros genes. Los exones de genes implicados en el procesamiento de ARN y la transcripción tendieron a agruparse, produciendo huellas de expresión similares y revelando vías biológicas compartidas, como la biogénesis de ribosomas o la degradación de ARN. En algunos casos, eliminar un solo exón tuvo un efecto claro e interpretable: suprimir un exón en los genes TAF5 o LSM11 perturbó el procesamiento correcto de los ARN histónicos, conduciendo a una acumulación inusual de mensajes histónicos poliadenilados. El conjunto de datos también señaló docenas de exones cuya pérdida alteró el número de células en diferentes etapas del ciclo celular, vinculando eventos de splicing concretos con decisiones sobre cuándo una célula se detiene, copia su ADN o se prepara para dividirse.
Un estudio de caso: un exón que ajusta a un regulador maestro
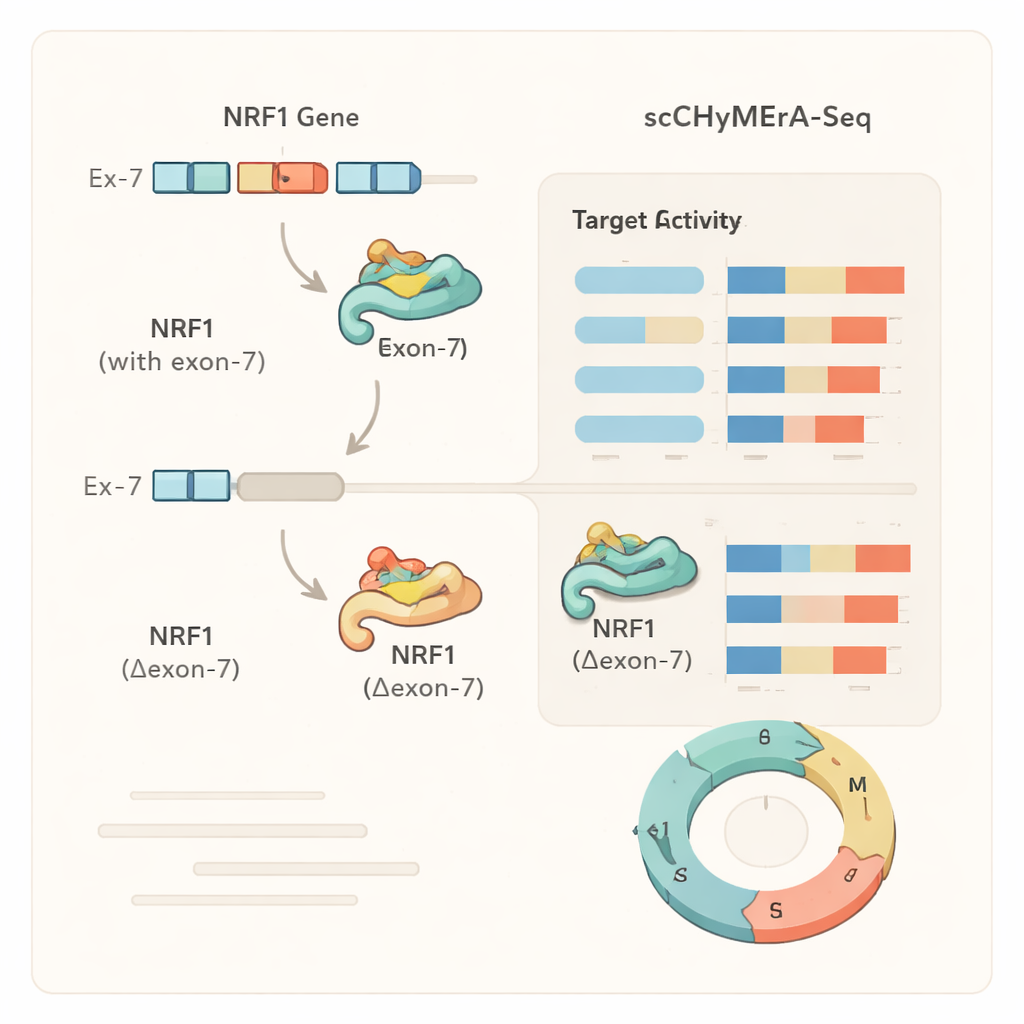
Un ejemplo destacado fue el exón 7 del gen NRF1, un factor de transcripción que controla muchos genes implicados en la producción de energía celular. Este exón se solapa parcialmente con la región de unión al ADN de NRF1. Cuando se eliminó el exón 7, cientos de genes regulados por NRF1 cambiaron su actividad, y experimentos detallados mostraron que la proteína NRF1 acortada tenía mucha menos capacidad para unirse a sus promotores objetivo en el genoma. Los autores también identificaron un regulador del splicing específico, SRSF3, que favorece la inclusión de este exón, revelando una cadena desde un factor de splicing, pasando por la elección de un exón en NRF1, hasta amplios cambios en los programas génicos y el metabolismo celular. Análisis similares mostraron que, para algunos genes, la eliminación de un exón imitaba la pérdida completa del gen, mientras que para otros producía un cambio más fino y dependiente del estado, lo que sugiere que los exones alternativos pueden modular sutilmente el comportamiento de las proteínas en lugar de simplemente activarlas o desactivarlas.
Por qué esto importa para la salud y las terapias futuras
Para un público no especializado, el mensaje clave es que las células dependen de la inclusión o el salto de segmentos de ARN muy cortos para ajustar cómo funcionan los genes, y que estos finos ajustes pueden alterar rasgos importantes como la división celular o la respuesta al estrés. La plataforma scCHyMErA-Seq actúa como una prueba de laboratorio de alto rendimiento para estas decisiones de splicing, señalando qué exones tienen impacto funcional real y cómo remodelan los estados celulares. Dado que muchos cánceres y trastornos neurológicos implican exones mal empalmados o factores de transcripción alterados, este enfoque podría ayudar a priorizar qué variantes de splicing atacar con futuros fármacos o terapias de ARN, y proporcionar una hoja de ruta para entender cómo pequeños recortes en el guion genético se traducen en grandes cambios en el comportamiento celular.
Cita: Kumari, B., Damodaran, A.P., Guiblet, W.M. et al. Single-cell exon deletion profiling reveals splicing events that shape gene expression and cell state dynamics. Nat Commun 17, 1218 (2026). https://doi.org/10.1038/s41467-026-68774-w
Palabras clave: splicing alternativo, secuenciación de ARN unicelular, cribado con CRISPR, regulación génica, ciclo celular