Clear Sky Science · es
Nanozima mimética de granzyme B para aplicaciones anticancerígenas dirigidas mediante nanovesículas
Reinventando a los asesinos corporales contra el cáncer
Nuestro sistema inmunitario dispone de células especializadas capaces de localizar y eliminar el cáncer, pero en muchos tumores sólidos tienen dificultades para penetrar, se fatigan con rapidez o atacan objetivos equivocados. Este estudio describe un sistema totalmente artificial a escala nanométrica que imita una de las armas más potentes del sistema inmune y la entrega directamente dentro de las células tumorales. El trabajo es importante porque apunta a tratamientos contra el cáncer que actúan como células inmunitarias vivas, pero están hechos de materiales estables y controlables en lugar de células humanas frágiles.
Convertir a un asesino natural en un plano de diseño
Las células T citotóxicas, un tipo de glóbulo blanco, eliminan células peligrosas usando una enzima llamada granzyme B. Una vez que reconocen un objetivo, perforan la membrana y liberan granzyme B, que activa programas de suicidio dentro de la célula. Esta estrategia sustenta terapias modernas como las células CAR-T, que pueden curar algunos cánceres de la sangre. Sin embargo, en tumores sólidos las células CAR-T a menudo fallan porque no alcanzan todas las regiones tumorales, se agotan o atacan tejidos sanos por error. Los autores se preguntaron si podían construir un dispositivo no vivo y a escala nanométrica que reprodujera la función clave de la granzyme B —activar la maquinaria de autodestrucción celular— sin depender de células T vivas.
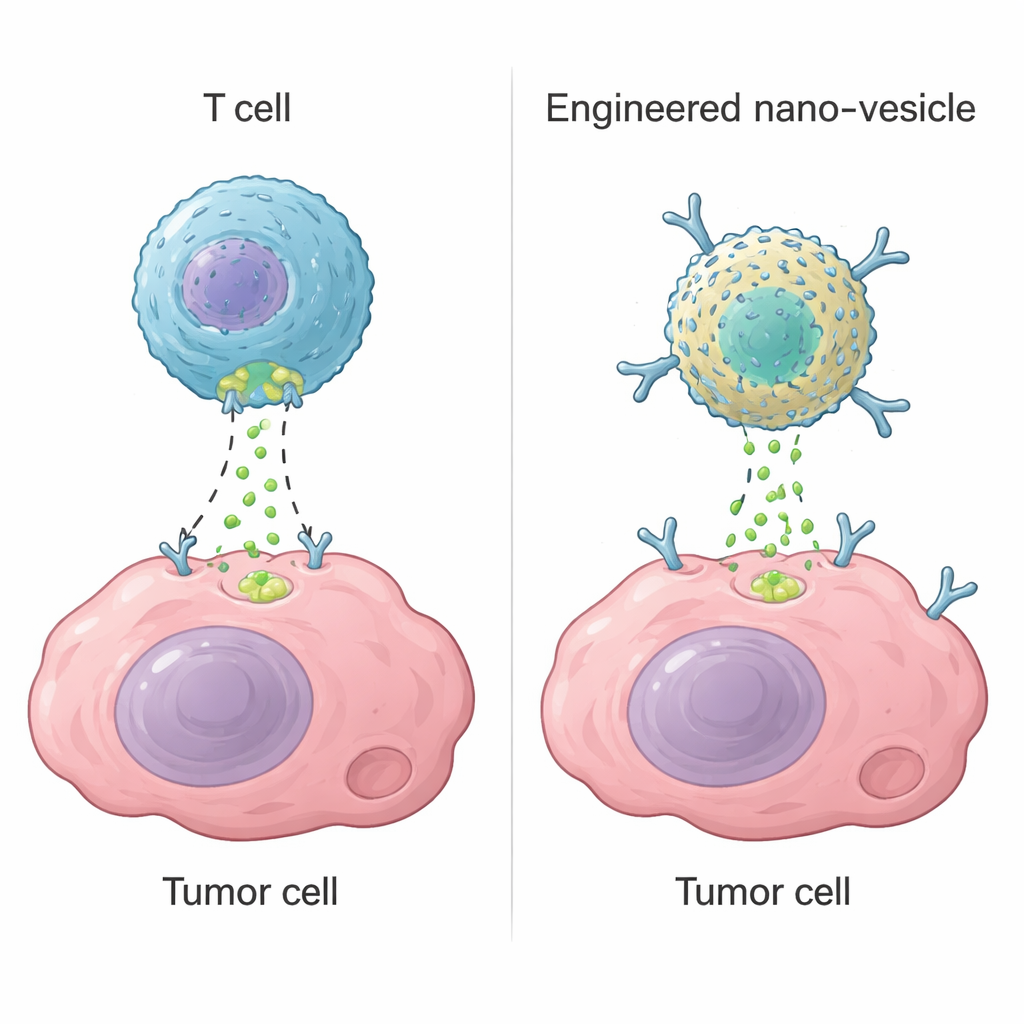
Diseñando una enzima artificial diminuta
El equipo partió de la ferritina, una proteína natural que forma nanocápsulas huecas y es fácil de producir en grandes cantidades. Al unir iones de paladio a la ferritina humana, crearon una «nanozima» con comportamiento semejante a una enzima. Estudios estructurales detallados revelaron que dos átomos de paladio se alojan en un bolsillo específico de la superficie proteica, sostenidos por aminoácidos con azufre y nitrógeno y por moléculas de agua. Este centro metálico binuclear actúa como un sitio de corte artificial que reconoce la misma secuencia corta que utiliza la granzyme B en un blanco crucial conocido como caspasa-3. En pruebas de laboratorio, la nanozima recortó eficientemente la caspasa-3 en la posición correcta, activándola, mientras ignoraba proteínas estrechamente relacionadas. La enzima artificial fue algo menos eficiente que la granzyme B natural pero notablemente más estable frente a un amplio rango de temperaturas y pH.
Contrabandeando la nanozima dentro de las células tumorales
Las enzimas como la granzyme B solo funcionan si alcanzan el interior de las células tumorales. Para ello, los investigadores encapsularon su nanozima de paladio–ferritina dentro de nanovesículas lipídicas, pequeñas burbujas blandas hechas de moléculas similares a grasas. Luego recubrieron estas vesículas con fragmentos de anticuerpos que reconocen HER2, una proteína que a menudo se sobreexpresa en cánceres de mama y de vejiga. Cuando estas vesículas camufladas se encuentran con células ricas en HER2, se unen fuertemente y se fusionan con la membrana celular, permitiendo que la carga de la nanozima se deslice directamente hacia el citoplasma en lugar de quedar atrapada y digerida en los compartimentos de reciclaje celular. La microscopía mostró las vesículas permaneciendo en la superficie celular mientras la nanozima se difundía hacia el interior, preparando el escenario para una autodestrucción controlada desde dentro.
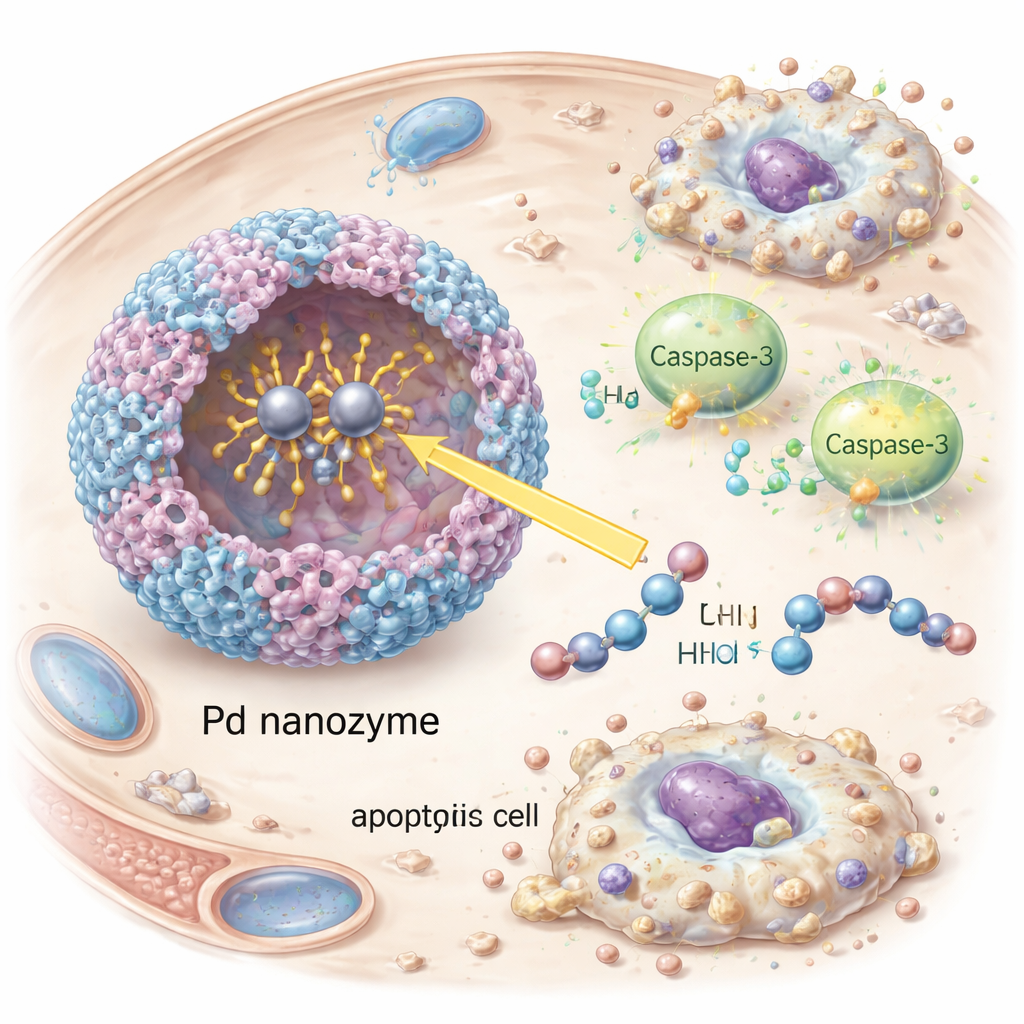
Activar con precisión el suicidio de células cancerosas
Una vez dentro de las células cancerosas, la nanozima activó la caspasa-3, un ejecutor central de la muerte celular programada. Los investigadores observaron la aparición de caspasa-3 activada y de su diana aguas abajo PARP, así como claros signos de apoptosis —células encogidas y fragmentadas— en cultivos de tumores HER2-positivos. Silenciar la caspasa-3 mediante interferencia de ARN redujo drásticamente la muerte celular, lo que confirma que el efecto dependía de esta vía y no de un daño inespecífico. En ratones portadores de tumores HER2-positivos, las vesículas decoradas con anticuerpos circularon más tiempo en la sangre, se acumularon más fuertemente en los tumores y frenaron el crecimiento tumoral de forma más eficaz que las vesículas que carecían del anticuerpo dirigible o de la carga de nanozima. Importantly, los animales tratados no mostraron pérdida de peso evidente, anomalías sanguíneas ni daño tisular en órganos principales, lo que sugiere un perfil de seguridad favorable en estas pruebas preliminares.
Lo que esto podría significar para la atención del cáncer en el futuro
Para no especialistas, el mensaje central es que los investigadores han construido un dispositivo diminuto y no vivo que se comporta como una parte clave de la maquinaria inmune que mata el cáncer. En lugar de editar células T vivas, diseñaron una nanoenzima estable que activa el mismo interruptor de suicidio dentro de las células tumorales y la envolvieron en una carcasa de administración inteligente que se dirige a cánceres específicos. Aunque queda mucho trabajo antes del uso humano, este enfoque ofrece una plataforma flexible: en principio, el recubrimiento de anticuerpos podría intercambiarse para dirigirse a distintos marcadores tumorales, y la enzima artificial podría optimizarse aún más. El estudio demuestra una vía prometedora hacia una inmunoterapia sin células, en la que nanomateriales cuidadosamente diseñados, en lugar de células inmunitarias vivas, se usan para localizar y destruir tumores sólidos.
Cita: Hu, X., Liu, Q., Kang, H. et al. Granzyme B-mimetic nanozyme for nanovesicle targeted anticancer applications. Nat Commun 17, 2031 (2026). https://doi.org/10.1038/s41467-026-68773-x
Palabras clave: nanomedicina contra el cáncer, inmunoterapia, granzyme B, nanozima, tumores HER2-positivos