Clear Sky Science · es
Química bioortogonal activada por especies reactivas de oxígeno en sistemas vivos habilitada por dihidrotetrazinas enmascaradas con boronato
Convertir el estrés celular en un interruptor preciso
Muchas enfermedades, desde el cáncer hasta problemas cardiacos, se caracterizan por células bajo estrés oxidativo que generan niveles elevados de especies reactivas de oxígeno, como el peróxido de hidrógeno. Este estudio muestra cómo los químicos pueden aprovechar ese mismo estrés como un interruptor incorporado para activar terapias potentes solo donde se necesitan. Al diseñar componentes farmacológicos que reaccionan únicamente en estos entornos estresados, los investigadores pretenden eliminar células tumorales o destruir proteínas dañinas mientras preservan los tejidos sanos.
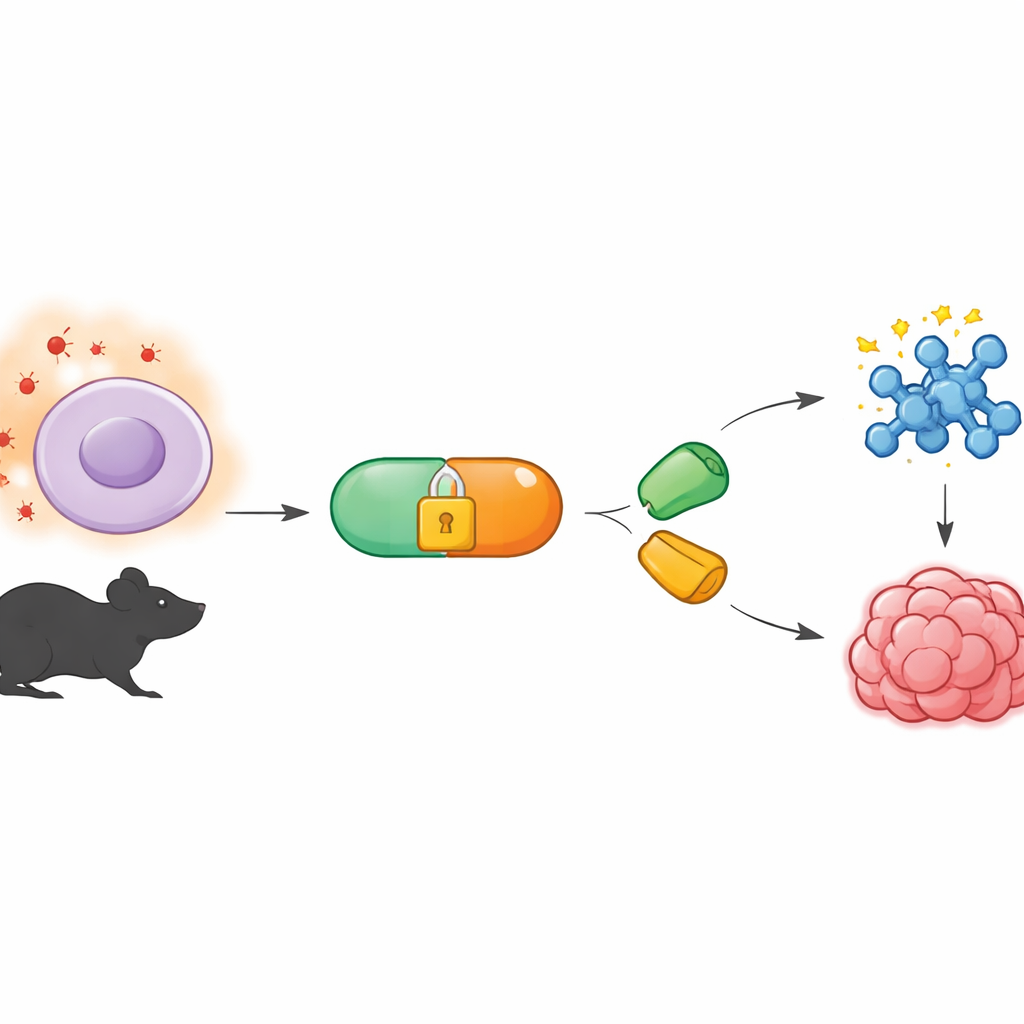
Una herramienta química que actúa en silencio
El trabajo se basa en un campo llamado química bioortogonal, que desarrolla reacciones que pueden realizarse dentro de organismos vivos sin perturbar la biología normal. Una versión popular utiliza pares especiales de moléculas que se ensamblan como piezas de un rompecabezas, incluso en el interior concurrido de una célula. Un socio, llamado tetrazina, reacciona muy rápidamente con una pareja complementaria en forma de “anillo”, conocida como dienófilo. Hasta ahora, muchas de estas reacciones se han controlado mediante luz o añadiendo enzimas. Los autores buscaron, en cambio, un sistema que escuchara las propias señales químicas del cuerpo —específicamente, los niveles inusualmente altos de especies reactivas de oxígeno que se encuentran en tumores y otros tejidos enfermos.
Construyendo un disparador químico sensible a ROS
Para ello, el equipo creó precursores de tetrazina que denominan BTz, que están químicamente “enmascarados” para permanecer inertes en tejidos normales. La máscara está formada por un grupo boronato vinculado a una forma reducida de tetrazina. Cuando el peróxido de hidrógeno escasea, BTz es estable en agua y en cultivo celular durante muchas horas. Pero cuando el peróxido de hidrógeno abunda —a niveles similares a los medidos en tumores— el grupo boronato se oxida y se descompone mediante una secuencia de autodestrucción, revelando la tetrazina activa. En experimentos de tubo de ensayo, aumentar de forma escalonada las concentraciones de peróxido de hidrógeno produjo un incremento correspondiente en la cantidad de tetrazina activa generada, confirmando que la reacción es selectiva y fuertemente dependiente de la dosis.
Usar el estrés celular para destruir una proteína promotora de cáncer
Los investigadores utilizaron primero su interruptor para controlar una estrategia farmacológica moderna llamada degradación dirigida de proteínas. Unieron BTz a talidomida, una molécula pequeña que puede reclutar un complejo enzimático responsable de etiquetar proteínas para su eliminación. En células cancerosas, este conjugado BTz–talidomida permaneció inactivo hasta que los niveles de peróxido de hidrógeno aumentaron, momento en que la máscara se abrió para formar una tetrazina activa. Esta tetrazina luego se enlazó rápidamente con una pareja complementaria unida a un fármaco que se dirige a BRD4, ensamblando un “quimera” mayor que arrastra la proteína relacionada con el cáncer BRD4 hacia la maquinaria de desecho celular. En líneas celulares de cáncer de pulmón y cervical, los niveles de BRD4 cayeron drásticamente solo cuando todas las piezas estaban presentes y había peróxido de hidrógeno disponible; bloquear las especies reactivas de oxígeno impidió la degradación, subrayando que el proceso está realmente activado por el estrés.
Administrar un fármaco tóxico solo donde se necesita
A continuación, el equipo convirtió la misma química en un sistema de liberación preciso para doxorrubicina, una quimioterapia potente pero dañina para el corazón. Vincularon la doxorrubicina a un dienófilo en tensión de modo que quedara bloqueada en una forma de profármaco inactiva. Cuando este profármaco encontró BTz en un entorno rico en peróxido de hidrógeno, la tetrazina recién formada reaccionó con el anillo en un proceso de “clic-para-liberar”, uniendo las piezas y expulsando doxorrubicina libre. En células de cáncer de colon cultivadas en placas, este sistema en dos pasos mató células casi con la misma eficacia que el fármaco libre, pero solo cuando el peróxido de hidrógeno estaba presente; sin él, las células permanecieron en gran medida indemnes. Un profármaco sensible al peróxido de hidrógeno más simple de doxorrubicina fue menos efectivo y menos selectivo en estas pruebas, resaltando la ventaja de separar el sensing y la liberación en dos pasos coordinados.
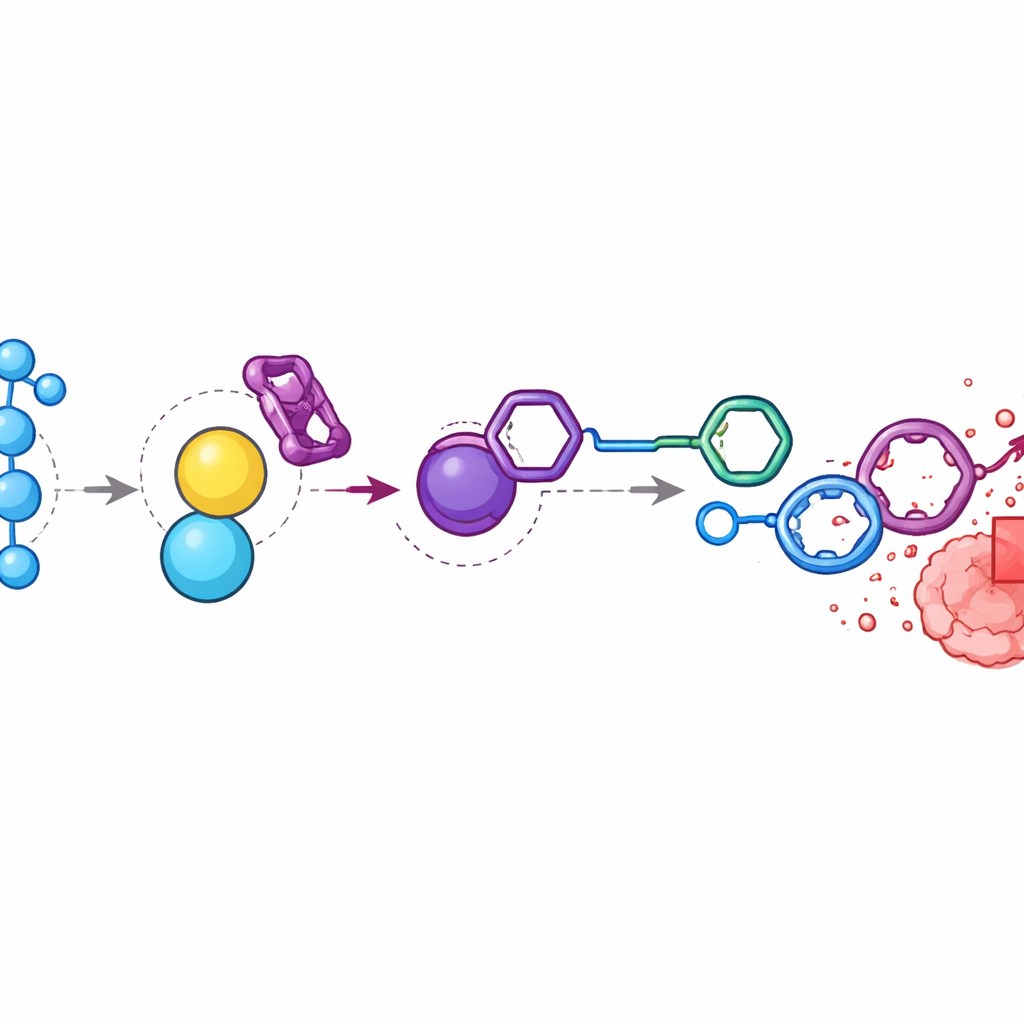
Concentrar la quimioterapia dentro de los tumores
En ratones con tumores de colon, los investigadores hallaron que los niveles de peróxido de hidrógeno en los tumores eran casi nueve veces mayores que en el músculo circundante. Inyectaron el profármaco de doxorrubicina y BTz en una secuencia temporizada para que ambos se acumularan cerca del tumor. El análisis químico mostró que los componentes desaparecían en gran medida del torrente sanguíneo y de los órganos, pero generaban altos niveles de doxorrubicina libre dentro de los tumores. En comparación con animales tratados con doxorrubicina estándar, los tratados con el sistema activado mostraron una reducción tumoral similar o mejor, pero mantuvieron un peso corporal estable y evitaron la toxicidad severa observada con dosis más altas del fármaco. Cuando el equipo interrumpió la señal de peróxido de hidrógeno inyectando catalasa, una enzima que elimina el peróxido de hidrógeno, la liberación del fármaco y la acumulación selectiva en el tumor se redujeron considerablemente, confirmando que el estrés oxidativo en el sitio tumoral es el impulsor clave.
Del señal de estrés a la terapia de precisión
En conjunto, este estudio demuestra una plataforma química versátil que convierte una característica de la enfermedad —el exceso de oxígeno reactivo— en un control preciso para reacciones potentes dentro de sistemas vivos. Al mantener la maneta tetrazina reactiva bloqueada hasta que encuentra peróxido de hidrógeno, el enfoque permite a los investigadores construir terapias complejas dentro del cuerpo solo donde se necesitan, ya sea para desmantelar una proteína promotora de cáncer o para liberar un fármaco tóxico dentro de un tumor. Dado que el estrés oxidativo también interviene en el envejecimiento, la inflamación, la diabetes y los trastornos neurodegenerativos, reacciones sensibles al estrés similares podrían adaptarse en última instancia para muchas condiciones donde la precisión y la seguridad son fundamentales.
Cita: Ming, D., Zhang, J., Mu, B. et al. Reactive oxygen species-activated bioorthogonal chemistry in living systems enabled by boronate-caged dihydrotetrazines. Nat Commun 17, 2568 (2026). https://doi.org/10.1038/s41467-026-68771-z
Palabras clave: química bioortogonal, especies reactivas de oxígeno, unión de tetrazina, liberación dirigida de fármacos, PROTAC