Clear Sky Science · es
Análisis microfluídico electroquímico potenciado por membrana homotípica de vesículas extracelulares para un diagnóstico preciso del cáncer
Convertir la propia armadura del cáncer en una herramienta diagnóstica
Las membranas que rodean las células cancerosas están repletas de distintivas “banderas” moleculares. Este estudio muestra cómo los científicos pueden arrancar esa armadura, extenderla sobre pequeñas placas de oro y usarla para pescar partículas reveladoras en la sangre. El resultado es una prueba sanguínea muy sensible que puede indicar no solo si existe cáncer de mama, sino qué subtipo es—información crucial para elegir el tratamiento adecuado.
Por qué importa el subtipo del cáncer de mama
El cáncer de mama no es una sola enfermedad. Los tumores se agrupan en subtipos como receptores de estrógeno positivos (ER+), HER2-positivos y triple negativo, y cada uno responde de forma distinta a la terapia hormonal, a fármacos dirigidos o a la quimioterapia. Hoy, los médicos suelen determinar el subtipo a partir de una biopsia de tejido tomada directamente del tumor. Ese procedimiento es invasivo, no puede repetirse con frecuencia y puede pasar por alto cambios que ocurren a medida que la enfermedad evoluciona. Una prueba basada en sangre que pueda seguir estas firmas de subtipo a lo largo del tiempo permitiría a los médicos ajustar la terapia antes y con más precisión.
Pequeños mensajeros flotando en la sangre
Las células cancerosas liberan constantemente burbujas a escala nanométrica llamadas vesículas extracelulares (VE) hacia el torrente sanguíneo. Las VE transportan proteínas, lípidos y material genético que se parecen estrechamente a los de sus células parentales, lo que las convierte en candidatas atractivas para “biopsias líquidas”. Pero hay un desafío: las VE de distintos subtipos de cáncer de mama pueden parecer muy similares si solo se analiza una o dos proteínas. Las pruebas existentes o bien apuntan a marcadores compartidos—lo que dificulta distinguir subtipos—o dependen de ensayos genéticos complejos que son lentos y pueden dar resultados engañosos. Los autores se propusieron leer la huella molecular más completa en la superficie de las VE de una manera simple y robusta.
Construyendo una red de pesca biomimética
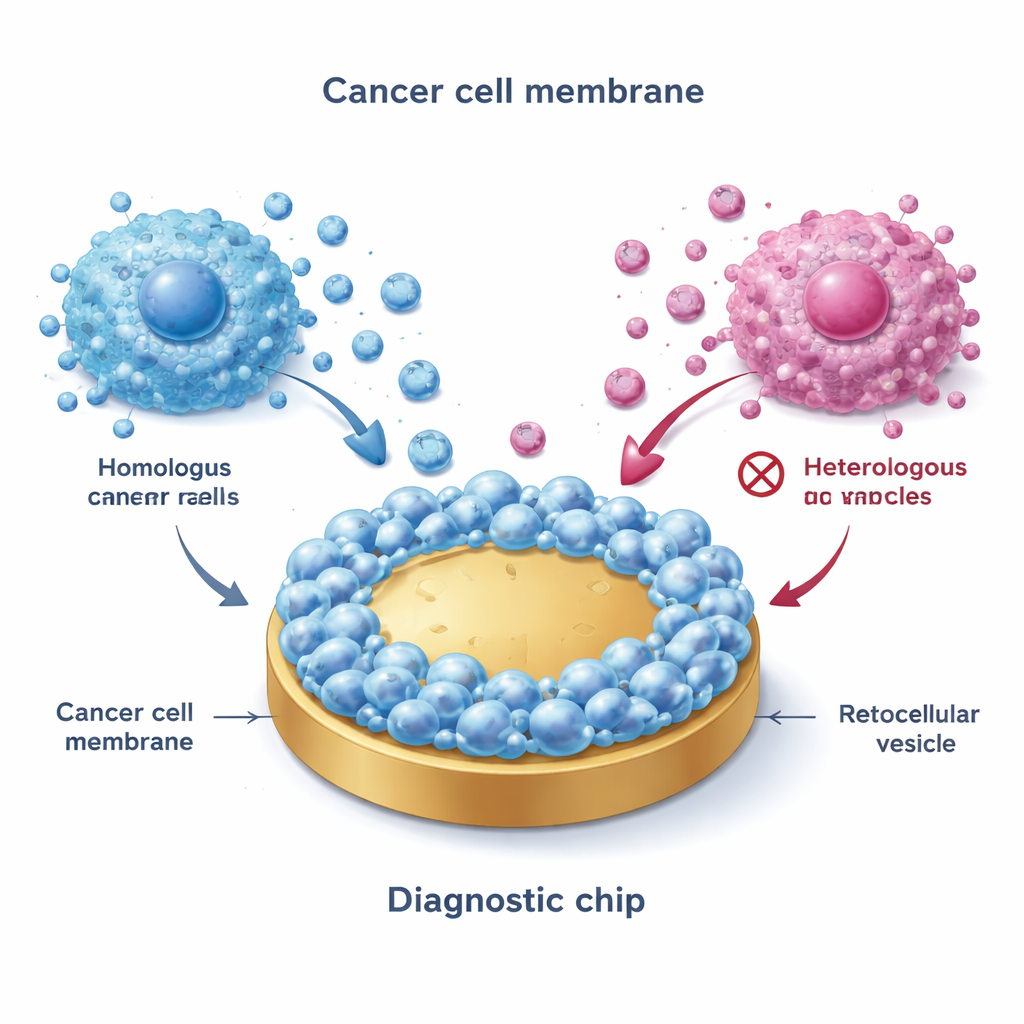
El equipo empezó por obtener membranas de cultivos de células de cáncer de mama que representaban los principales subtipos: ER+ (como MCF-7), HER2-positivo y triple negativo. Mediante un proceso de congelación–descongelación, lisaron las células, aislaron las membranas externas y luego fusionaron esas membranas sobre superficies planas de oro. Esto creó una “interfaz biomimética” que imita de cerca el exterior de las células cancerosas originales. De forma notable, cuando las VE se hacían fluir sobre esas superficies recubiertas, solo se adherían con fuerza las vesículas de subtipos coincidentes o estrechamente relacionados—un fenómeno llamado unión homotípica. Imágenes avanzadas y mediciones eléctricas confirmaron que las superficies recubiertas con membrana eran más rugosas, más hidrofílicas y mucho menos propensas a la unión inespecífica que el oro desnudo, lo que las hace adecuadas para mediciones limpias en fluidos complejos como la sangre.
Convirtiendo la captura de vesículas en una señal eléctrica
Para transformar la unión en una señal medible, los investigadores apuntaron a una proteína abundante llamada CD47 en la superficie de las VE. Unieron anticuerpos contra CD47 a nanopartículas de plata mediante un puente corto de ADN, creando pequeñas etiquetas electroactivas. Después de que la superficie recubierta con membrana capturara sus VE preferidas, estas etiquetas se anclaban a CD47 en las vesículas unidas. Al exponerlas a una solución ácida y medir luego electroquímicamente, la plata produjo una corriente marcada y fácilmente cuantificable. La intensidad de esta señal aumentaba de forma lineal en un amplio rango de concentraciones de VE, hasta apenas unos cientos de vesículas por mililitro—mucho más sensible que métodos comunes como los kits ELISA o el seguimiento por nanopartículas. Cada tipo de membrana cancerosa produjo una señal fuerte solo con sus VE coincidentes, incluso en presencia de vesículas de otros subtipos, plaquetas o células no relacionadas.
Del banco de laboratorio a muestras de sangre de pacientes
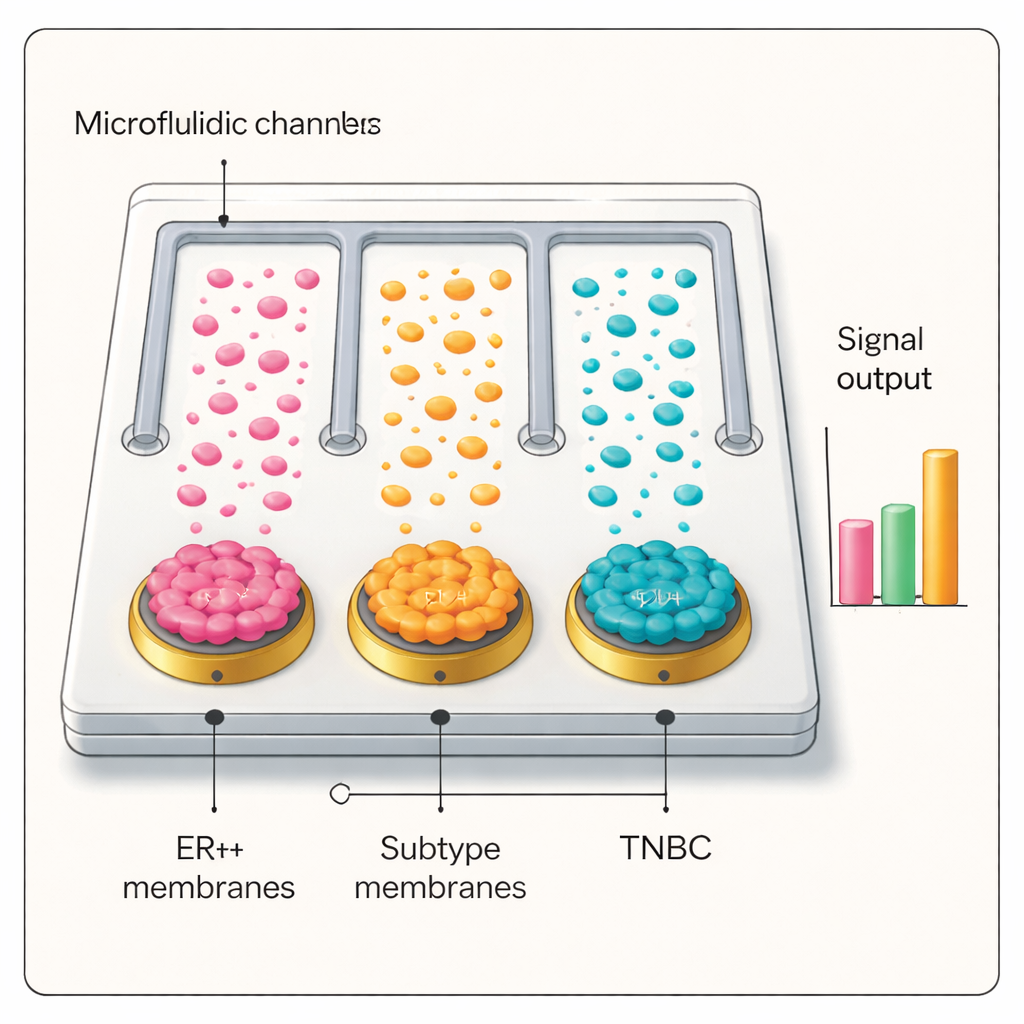
Con esta interfaz selectiva y sensible, el equipo construyó un chip microfluídico con canales paralelos, cada uno recubierto con la membrana de un tipo distinto de célula de cáncer de mama, además de un control sin recubrimiento. Cuando se hizo pasar plasma de pacientes por el chip y se sondó con las etiquetas plata–anticuerpo, solo el canal cuya membrana coincidía con el subtipo tumoral del paciente produjo una señal eléctrica alta. En pruebas cegadas con docenas de personas—incluyendo pacientes con cáncer de mama ER+ y triple negativo, individuos con enfermedad mamaria benigna, pacientes con cáncer de pulmón y voluntarios sanos—la plataforma distinguió con precisión cáncer de no cáncer e identificó correctamente los subtipos de cáncer de mama. El rendimiento diagnóstico igualó o superó a la patología estándar en muchos casos y mostró potencial para estadificar la enfermedad y seguir su progresión.
Qué podría significar esto para el cuidado del cáncer en el futuro
En términos sencillos, los investigadores han convertido la propia cubierta externa del cáncer en un cebo altamente selectivo para las pequeñas partículas que los tumores liberan en la sangre. Al leer la firma eléctrica de qué canal “se ilumina”, los médicos podrían algún día determinar no solo si hay cáncer, sino de qué tipo se trata, usando solo una muestra de sangre. Aunque el sistema aún requiere más refinamiento—como añadir más marcadores y más tipos de membrana, e integrar análisis de datos inteligentes—apunta hacia un futuro en el que pruebas sanguíneas rutinarias y mínimamente invasivas ayuden a guiar tratamientos oncológicos personalizados y a monitorizar cómo cambian los tumores con el tiempo.
Cita: Zou, Z., Jin, X., Yu, X. et al. Homotypic membrane-powered electrochemical microfluidic analysis of extracellular vesicles for precise cancer diagnosis. Nat Commun 17, 1953 (2026). https://doi.org/10.1038/s41467-026-68770-0
Palabras clave: subtipos de cáncer de mama, biopsia líquida, vesículas extracelulares, diagnóstico microfluídico, sensores de membrana celular