Clear Sky Science · es
Ensambles moleculares cíclicos para la imagen y la alteración del Golgi
Convertir el centro de envío celular en un objetivo estratégico
En el interior de cada célula animal se encuentra el aparato de Golgi, una activa estación de clasificación que termina, empaqueta y envía miles de proteínas y lípidos. Muchas células cancerosas dependen en gran medida de este núcleo para modificar señales de crecimiento y secretar factores que remodelan su entorno. Este artículo presenta diminutas moléculas diseñadas que se dirigen al Golgi, lo iluminan para una imagen rápida y, cuando se reconfiguran, pueden bloquear selectivamente sus operaciones para perjudicar a las células cancerosas mientras preservan a ciertas células sanas.
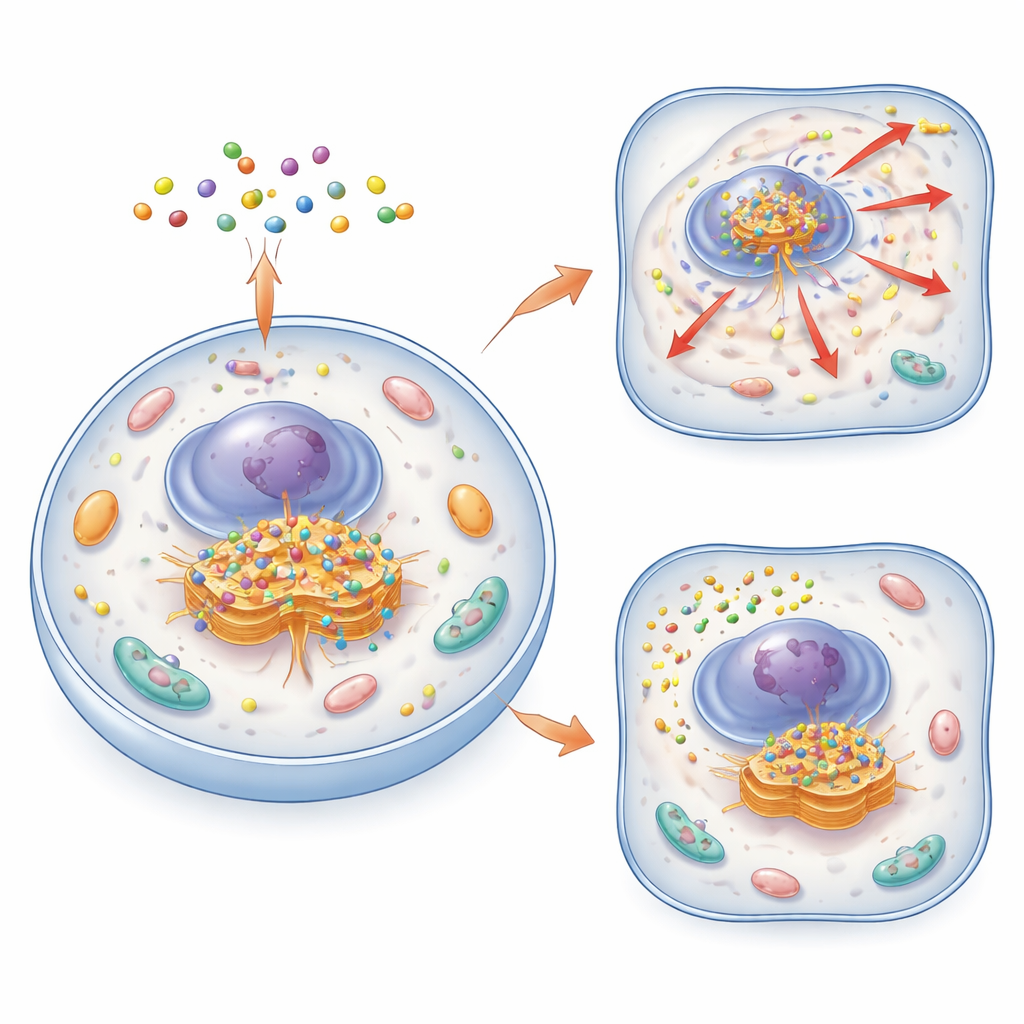
Una nueva manera de localizar y observar el Golgi
Los autores crearon una familia de pequeñas moléculas inteligentes llamadas ensambles moleculares cíclicos, o CyMA. Estas moléculas se construyen a partir de péptidos cortos que pueden tanto atravesar las membranas celulares como agruparse en pequeños cúmulos. En su versión «de imagen» (CyMA‑i), los péptidos llevan un tinte fluorescente que brilla intensamente cuando las moléculas se ensamblan. Una vez dentro de la célula, enzimas cortan una tapa protectora del precursor CyMA, exponiendo un grupo reactivo. Enzimas residentes del Golgi luego añaden una cadena grasa a ese grupo, haciendo que las moléculas sean mucho más adhesivas y propensas a autoensamblarse precisamente en el Golgi. Dado que este proceso es rápido y utiliza la maquinaria celular natural, los investigadores pueden delinear la forma del Golgi en células vivas en cuestión de minutos y con concentraciones de la sonda muy bajas.
Un ciclo fútil que fija moléculas en el Golgi
Los CyMA no son simplemente marcadores; están diseñados para participar en un «ciclo fútil» en el Golgi. Un grupo de enzimas añade cadenas grasas al péptido, mientras otro grupo las elimina. A medida que la célula añade y retira repetidamente estas cadenas, los péptidos modificados siguen ensamblándose y desensamblándose in situ. Este vaivén constante atrapa un núcleo parecido a un sólido de ensambles en las membranas del Golgi, pero mantiene las moléculas individuales en ciclo continuo. La célula debe gastar continuamente sus propios bloques de construcción de ácidos grasos para mantener este bucle, alimentando efectivamente los ensambles y ayudando a su persistencia. Al mismo tiempo, enzimas adicionales pueden cortar lentamente un enlace éster distinto dentro de CyMA, transformándolos en fragmentos más hidrofílicos que se dispersan. Como algunas células sanas, por ejemplo hepatocitos y ciertas células inmunitarias, son ricas en enzimas que rompen ésteres, pueden desmontar CyMA de forma más eficiente y, por tanto, se ven menos afectadas.
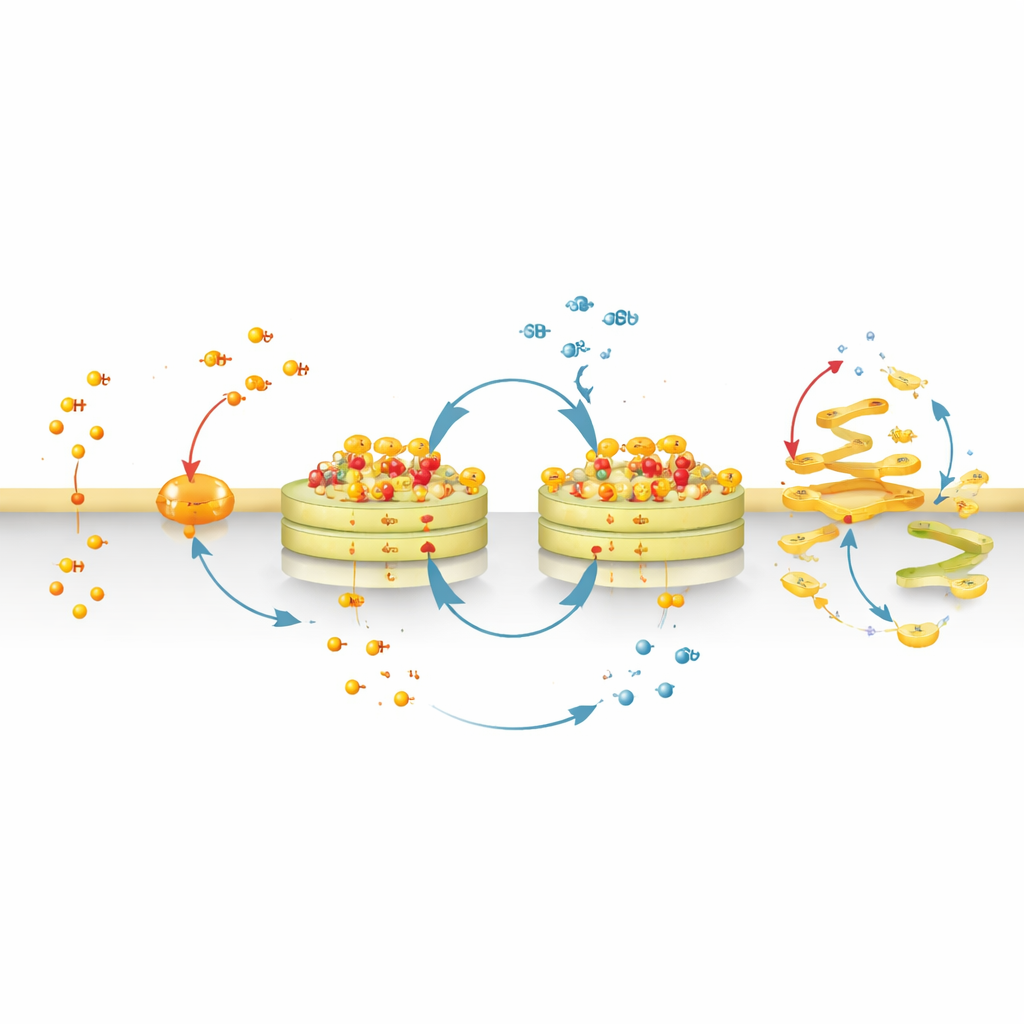
De herramienta de imagen suave a perturbador del Golgi
Cambiando el tinte fluorescente por un grupo químico con mayor afinidad por la membrana, el equipo convirtió CyMA‑i en CyMA‑d, una versión disruptiva que ya no brilla pero que sigue ciclando y ensamblándose en el Golgi. Estos ensambles perturban físicamente la estructura del Golgi y el flujo constante de vesículas hacia y desde él. Proteínas que normalmente viajan del retículo endoplásmico al Golgi y de allí a la superficie celular quedan atrapadas o se desvían. Las rutas entrantes—desde la superficie celular de vuelta al Golgi o desde el Golgi a otros orgánulos—también se bloquean. Como resultado, receptores de superficie clave y moléculas de señalización o no alcanzan sus destinos o se acumulan en lugares equivocados dentro de la célula.
Desorden en las señales celulares y los mensajes secretos
El Golgi es donde muchas proteínas reciben toques finales cruciales, como cadenas de azúcares y colas lipídicas. Los ensambles CyMA‑d reducen la lipidación y glicosilación adecuadas de numerosas proteínas, incluidos impulsores del cáncer bien conocidos como Ras y las principales tirosina‑quinasas receptoras. Estos cambios descarrilan vías promotoras del crecimiento como AKT y mTOR. Al mismo tiempo, la producción secretora de la célula se atenúa: factores importantes como TGF‑β1 y VEGF, que los tumores emplean para suprimir la inmunidad y estimular la angiogénesis, ya no se liberan de manera eficiente. El estrés de esta desorganización provoca redes reticulares endoplásmicas enmarañadas, alteraciones mitocondriales, una autophagia detenida (el sistema de reciclaje celular) y un aumento de proteínas dañadas etiquetadas con ubiquitina, empujando en conjunto a las células cancerosas hacia la muerte.
Presión selectiva sobre los tumores y promesa terapéutica
Puesto que CyMA‑d dependen de un conjunto compartido de enzimas y metabolitos que muchas células cancerosas usan en exceso, pueden matar a una amplia variedad de tipos tumorales, incluidos modelos de cáncer de ovario resistentes a fármacos, a dosis muy bajas. Sin embargo, las células con niveles altos de determinadas esterolas—enzimas esterasas—desmontan CyMA‑d con mayor facilidad y resultan menos dañadas, lo que ofrece una vía de selectividad integrada. En esferoides tumorales tridimensionales, cultivos derivados de pacientes y modelos murinos, CyMA‑d reducen tumores, disminuyen metástasis y reducen el acúmulo de líquido en el abdomen. Al combinarse con terapias de bloqueo inmunitario (checkpoint), mejoran además el control tumoral y la supervivencia. En esencia, este trabajo demuestra que construir materiales dinámicos dentro del Golgi—en lugar de dirigirnos a una única proteína—puede cerrar simultáneamente múltiples procesos críticos para el cáncer.
Qué significa esto para tratamientos futuros
Para un no especialista, la idea clave es que los autores han convertido al Golgi de un observador pasivo en un objetivo terapéutico activo. Reclutando las propias enzimas de la célula para ensamblar y reciclar pequeñas moléculas en este centro, pueden o bien resaltarlo de forma inocua o bien abrumar gradualmente su función. Esta plataforma de doble uso sugiere un nuevo tipo de tratamiento: en vez de diseñar un fármaco para una proteína concreta, podríamos diseñar pequeños precursores que las células transformen en materiales autoorganizados capaces de desbaratar redes completas de comunicación y transporte de las que dependen los cánceres para crecer y diseminarse.
Cita: Tan, W., Zhang, Q., Liu, Z. et al. Cycling molecular assemblies for Golgi imaging and disruption. Nat Commun 17, 2102 (2026). https://doi.org/10.1038/s41467-026-68768-8
Palabras clave: Aparato de Golgi, ensambles moleculares, transporte de proteínas, terapia contra el cáncer, dirigido a orgánulos