Clear Sky Science · es
Un quimera de antígeno en tándem estabilizada que provoca una potente actividad de reducción de la transmisión de la malaria
Por qué importa detener la transmisión por mosquitos
Las vacunas contra la malaria que se usan hoy pueden reducir considerablemente las formas graves de la enfermedad y la mortalidad en niños pequeños, pero dejan una laguna importante: las personas que no se sienten enfermas pueden seguir alojando parásitos que infectan a los mosquitos y mantienen la transmisión. Este estudio presenta un diseño de vacuna de próxima generación pensado no para proteger únicamente a una persona, sino para cortar la cadena de infección entre humanos y mosquitos. Al diseñar con precisión cómo se exhiben las proteínas clave del parásito al sistema inmunitario, los investigadores aspiran a generar anticuerpos que conviertan a los mosquitos en huéspedes pobres para la malaria, ayudando a las comunidades a acercarse al objetivo de eliminación.
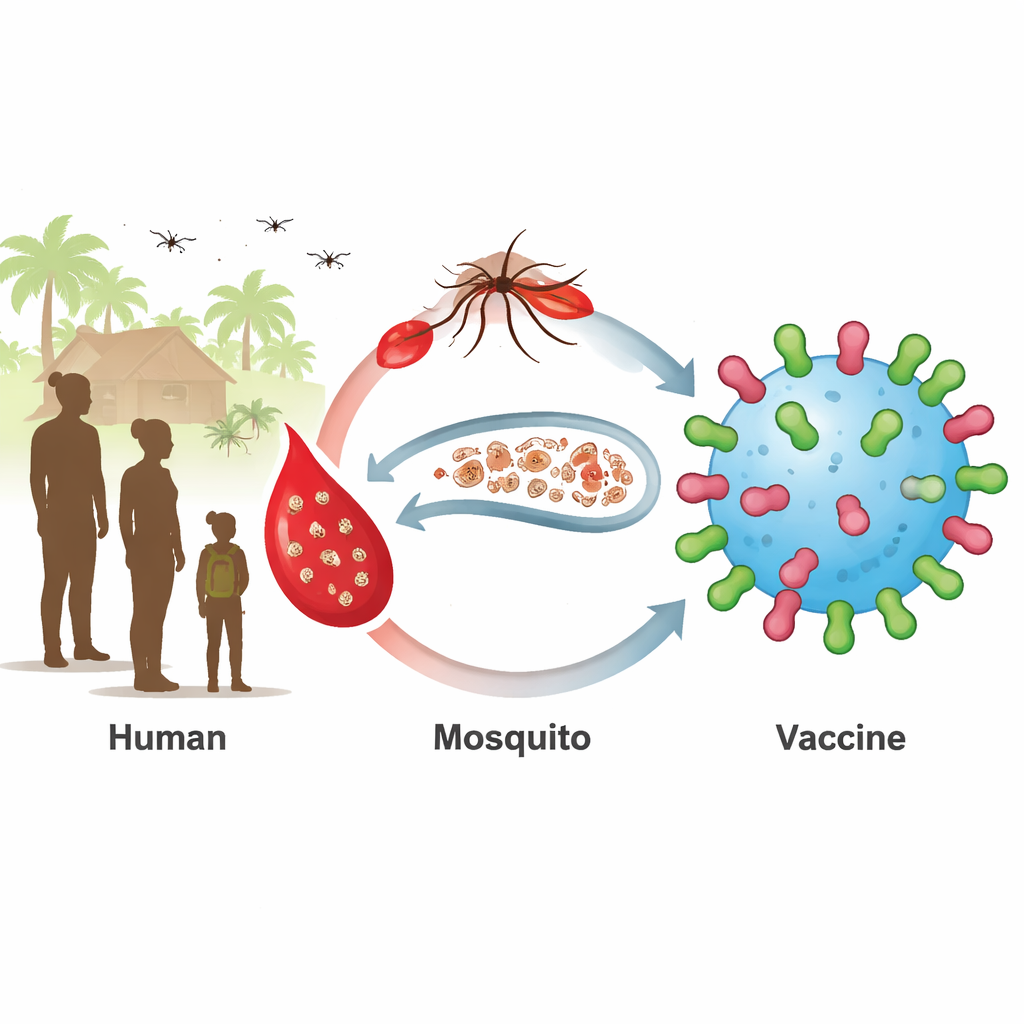
Un reservorio oculto que mantiene viva la malaria
Las vacunas actuales contra la malaria se centran en las primeras fases de la infección en el hígado y la sangre. Funcionan mejor en niños pequeños, pero los niños mayores y los adultos a menudo albergan parásitos en la fase sexual madura, denominados gametocitos, sin presentar síntomas. Cuando los mosquitos pican a estas personas, recogen los parásitos y los diseminan. Dos proteínas de superficie del parásito, conocidas como Pfs230 y Pfs48/45, se encuentran en estas fases sexuales y son dianas atractivas para las llamadas vacunas bloqueadoras de la transmisión. Vacunas contra fragmentos de estas proteínas han entrado en ensayos clínicos, pero han tenido dificultades para inducir respuestas de anticuerpos fuertes y duraderas en todos los receptores.
Construir un señuelo más inteligente para el sistema inmunitario
Para mejorar los diseños previos, los autores adoptaron un enfoque de biología estructural, examinando en detalle atómico cómo se unen los anticuerpos humanos potentes a Pfs230 y Pfs48/45. Identificaron pequeñas regiones, o epítopos, que son especialmente eficaces para bloquear el desarrollo del parásito dentro de los mosquitos. Igual de importante, cartografiaron epítopos “no funcionales” que atraen anticuerpos que se unen pero no impiden la transmisión, desperdiciando en esencia el esfuerzo inmunitario. Usando modelado por ordenador y herramientas de ingeniería de proteínas, fusionaron la región más potente de Pfs230 (su primer dominio) con la región clave de Pfs48/45 (su tercer dominio) en una sola proteína cuidadosamente organizada que denominan quimera de antígeno en tándem estabilizada, o STAC.
Ocultar los blancos inútiles, conservar los útiles
El reto fue presentar estos dos dominios juntos de una forma que imite cómo se disponen en el parásito, al tiempo que se ocultan físicamente las superficies no funcionales que normalmente quedan enterradas en la proteína intacta. El equipo rediseñó de forma iterativa el enlace corto y la interfaz entre los dos dominios, probando cada versión en cuanto a estabilidad, correcto plegamiento y si aún se unía a un panel de anticuerpos bien caracterizados. Software avanzado de diseño sugirió mutaciones que apretaron la interfaz y mejoraron la expresión en células en cultivo. Estudios estructurales mediante cristalografía de rayos X, dispersión de rayos X a bajo ángulo y crio‑microscopía electrónica confirmaron que en la construcción final de STAC, los epítopos deseados se muestran con alta fidelidad, mientras que los sitios conocidos como poco útiles quedan bloqueados estéricamente.
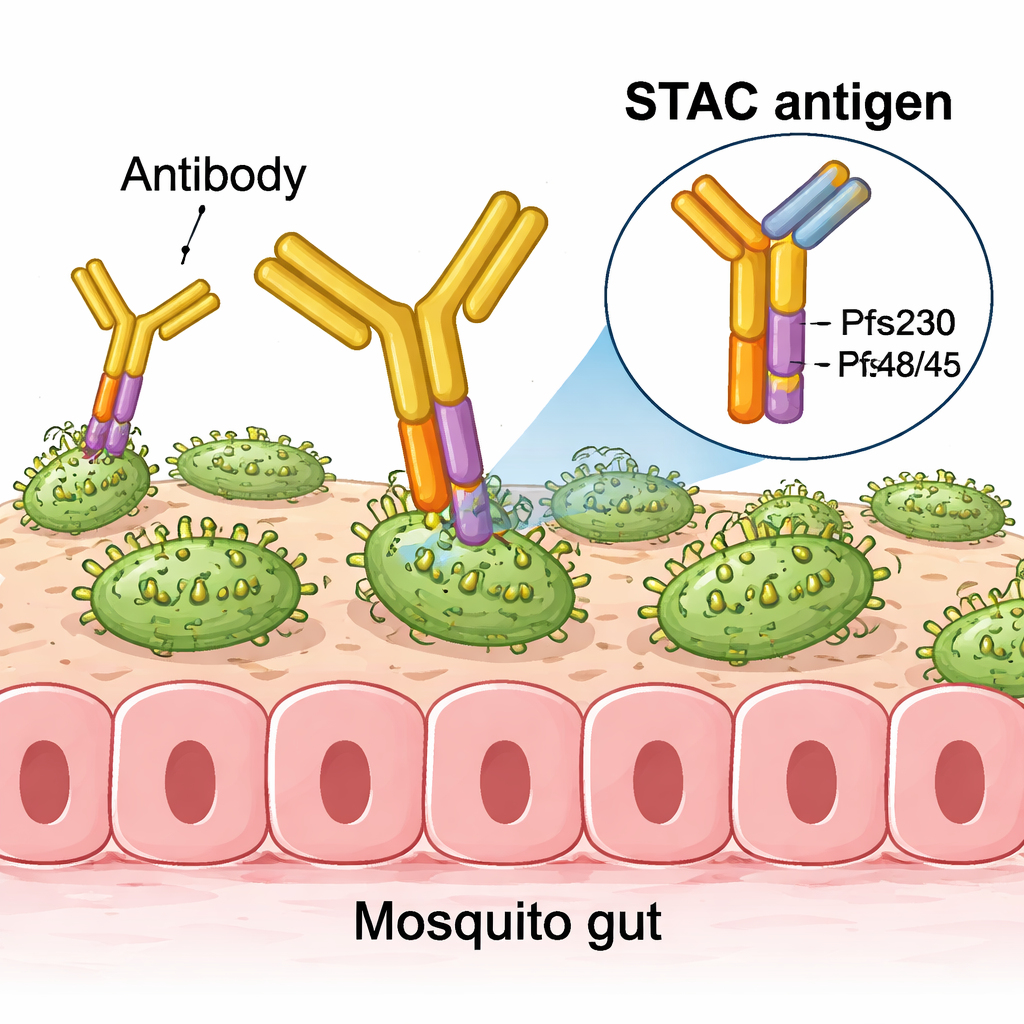
De moléculas únicas a potentes nanopartículas
Las pruebas en ratones mostraron que cuando STAC se fijó a liposomas especializados o a nanopartículas proteicas autoensamblantes, desencadenó respuestas de anticuerpos fuertes capaces de reducir drásticamente el desarrollo del parásito en ensayos estándar de alimentación de mosquitos. A dosis iguales o menores, STAC frecuentemente igualó o superó a las vacunas que usaban fragmentos de Pfs230 y Pfs48/45 por separado, ya fuera administradas solas, mezcladas o presentadas conjuntamente en la misma partícula. En ensayos altamente sensibles que diluyeron sueros de ratón muchas veces, los anticuerpos inducidos por nanopartículas decoradas con STAC mantuvieron mejor la actividad de reducción de la transmisión que los de otras formulaciones, lo que indica respuestas particularmente potentes y focalizadas.
Qué podría significar esto para el control de la malaria
Para quienes no son especialistas, la idea clave es que STAC es un señuelo diseñado a medida que muestra al sistema inmunitario exactamente las partes del parásito de la malaria que más importan para bloquear la propagación, mientras oculta regiones distractoras que no ayudan. En modelos animales, este diseño produce anticuerpos que dificultan que los parásitos completen su ciclo de vida en los mosquitos, incluso cuando los niveles de anticuerpos son relativamente bajos. Si resultados similares se mantienen en humanos, STAC podría convertirse en un socio poderoso de las vacunas contra la malaria existentes: protegiendo a las personas vacunadas frente a la enfermedad y, al mismo tiempo, reduciendo el reservorio infeccioso en la comunidad. Más en general, el trabajo muestra cómo el conocimiento estructural detallado y la ingeniería de proteínas pueden utilizarse para crear vacunas multicomponente que sean potentes, estables y potencialmente más baratas de fabricar.
Cita: Ivanochko, D., Miura, K., Hailemariam, S. et al. A stabilized tandem antigen chimera that elicits potent malaria transmission-reducing activity. Nat Commun 17, 2010 (2026). https://doi.org/10.1038/s41467-026-68761-1
Palabras clave: vacunas contra la malaria, bloqueo de la transmisión, Pfs230, Pfs48/45, inmunógeno nanopartícula