Clear Sky Science · es
Papel esencial del eje NONO-HOXA1-Wnt en la diferenciación de cardiomiocitos
Por qué las diminutas células del corazón nos importan a todos
Cada latido depende de miles de millones de células musculares especializadas que se forman en el útero. Cuando este proceso falla, los bebés pueden nacer con defectos cardíacos graves. Este estudio usa células madre humanas para desvelar un sistema de control crucial —conformado por moléculas llamadas NONO y HOXA1 y una señal bien conocida llamada Wnt— que ayuda a las células tempranas a comprometerse con convertirse en músculo cardíaco sano. Comprender este circuito oculto podría, en el futuro, orientar mejores diagnósticos y tratamientos para la cardiopatía congénita.
De células en blanco a los primeros constructores del corazón
Los investigadores partieron de células iPS humanas —células versátiles que se pueden inducir a casi cualquier tipo celular—. Con una receta estándar, dirigieron estas células hacia cardiomiocitos, las células que laten del corazón. Al eliminar el gen NONO, muchas menos células adoptaron con éxito identidad cardiaca. Marcadores tempranos clave que normalmente aparecen cuando las células abandonan su estado primitivo y se encaminan hacia la línea cardíaca se redujeron drásticamente. El secuenciamiento de ARN a nivel de célula única mostró que muchas células deficientes en NONO se quedaron a mitad de camino, atrapadas en un estado inmaduro tipo mesendodermo en lugar de progresar hacia un músculo cardíaco plenamente desarrollado.
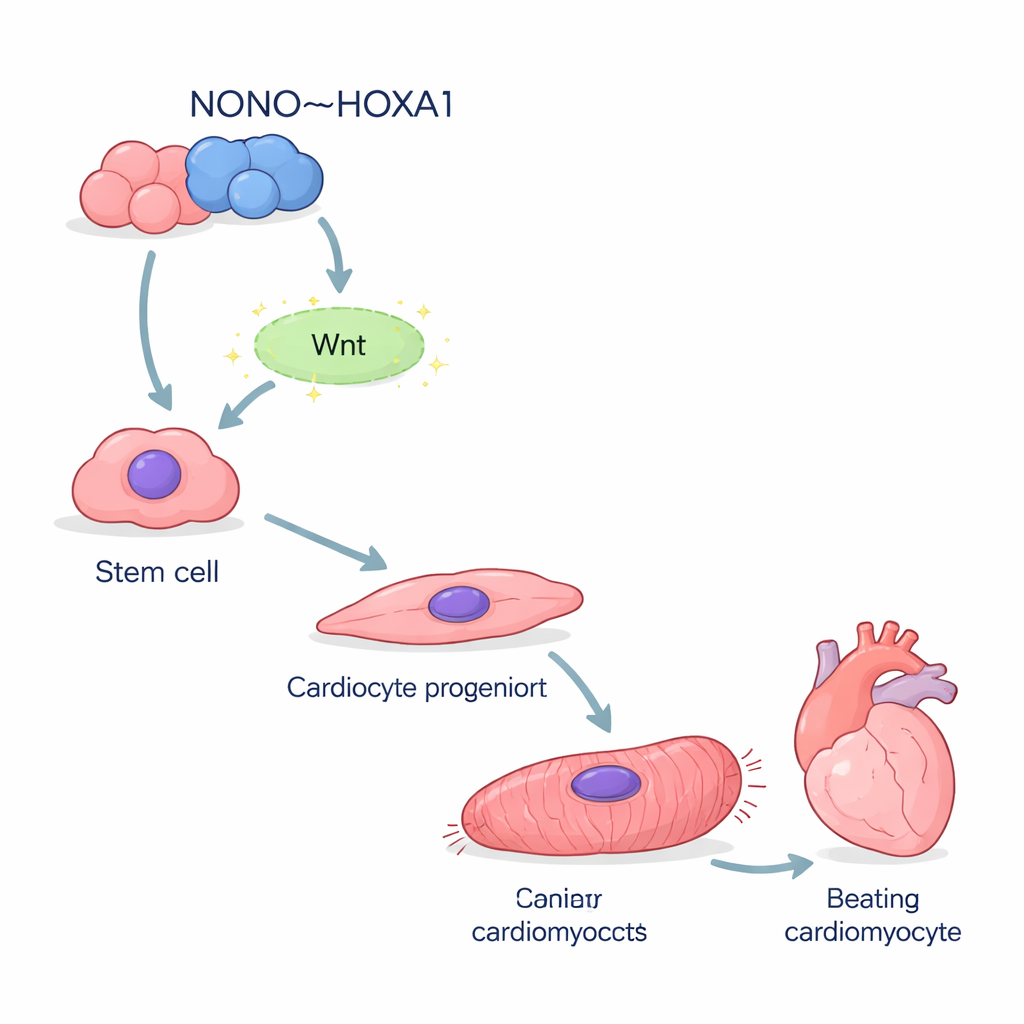
Cuando falta el andamiaje, las células cardíacas fallan
Las pocas células que llegaron a convertirse en cardiomiocitos sin NONO estaban lejos de ser saludables. Expresaban niveles mucho más bajos de proteínas estructurales que forman el sarcómero, la maquinaria microscópica que impulsa la contracción. Al microscopio, la mayoría de las células mutantes mostraban fibras contráctiles fragmentadas y desorganizadas en lugar de las franjas ordenadas vistas en células normales. La microscopía electrónica confirmó que los “peldaños” del disco Z del andamiaje contráctil estaban ausentes o malformados. Funcionalmente, estas células latían más despacio y de forma irregular. Las mediciones de los picos de calcio —los eventos eléctricos que desencadenan cada latido— revelaron formas de onda erráticas con picos retardados y recuperación lenta, reflejando los defectos en la expresión génica de los canales de manejo de calcio.
Rescatando el desarrollo y mostrando la asociación NONO–HOXA1
Para comprobar si estos problemas realmente provenían de la pérdida de NONO, el equipo reintrodujo NONO de forma controlada y regulada por un fármaco durante los dos primeros días de diferenciación. Este pulso breve de NONO restauró en gran medida el aumento de genes cardíacos tempranos, incrementó la proporción de células cardíacas latientes y reconstruyó sarcómeros y discos Z organizados. El perfilado de la expresión génica confirmó que muchos genes de contracción muscular y desarrollo cardíaco volvieron hacia niveles normales. En contraste, versiones mutadas de NONO derivadas de pacientes no rescataron la fenotipo, apoyando la idea de que tales variantes causan enfermedad al interrumpir este programa temprano. Experimentos de interacción proteica revelaron que NONO se une físicamente a un factor de transcripción llamado HOXA1, y que este contacto estabiliza HOXA1 y facilita la formación de dímeros necesarios para unirse al ADN.
Activar la señal Wnt para comprometerse con el destino cardíaco
Mapear dónde se sitúan estas proteínas en el genoma mostró que NONO y HOXA1 ocupan con frecuencia las mismas regiones regulatorias, incluidas las que controlan genes tempranos importantes del corazón y de la vía Wnt. Cuando faltaba NONO, la unión de HOXA1 a muchos de estos sitios se debilitó, especialmente en genes que impulsan el mesodermo precardiaco —el tejido formador del corazón más temprano. La vía downstream Wnt/β-catenina, que normalmente ayuda a lanzar el desarrollo del mesodermo y del corazón, también se vio atenuada: menos β-catenina se acumuló en el núcleo y las pruebas con reporteros sensibles a Wnt disminuyeron. Potenciar las señales Wnt con una dosis mayor de un fármaco activador de Wnt durante los primeros días de diferenciación pudo en parte compensar la ausencia de NONO, restaurando más células cardíacas y aumentando la expresión de genes cardíacos.
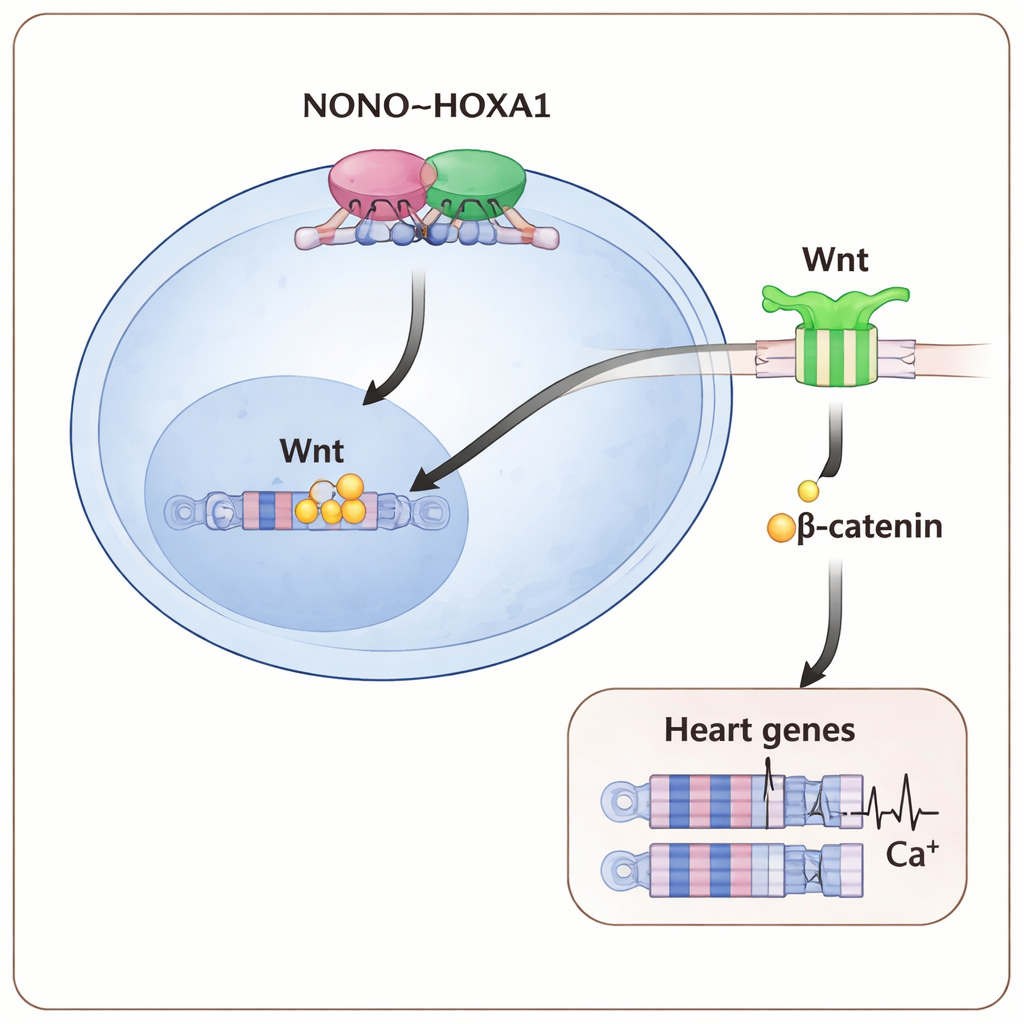
Qué significa esto para comprender los defectos de nacimiento
Para los no especialistas, el mensaje central es que un pequeño equipo molecular —NONO trabajando mano a mano con HOXA1 para ajustar finamente las señales Wnt— actúa como un “controlador de tráfico” temprano que indica a las células jóvenes que se conviertan en músculo cardíaco y las equipa para latir correctamente. Cuando cualquier parte de este eje NONO–HOXA1–Wnt se altera, las células dudan, los genes cardíacos clave permanecen apagados y los cardiomiocitos resultantes son frágiles a nivel estructural y eléctrico. Estos hallazgos aportan una explicación molecular más clara de por qué las mutaciones en NONO se asocian con cardiopatías congénitas, y señalan vías para manipular este circuito en modelos con células madre o, algún día, en terapias destinadas a prevenir o reparar malformaciones cardíacas.
Cita: Feng, Z., Gao, Y., Gao, H. et al. Essential role of NONO-HOXA1-Wnt axis in cardiomyocyte differentiation. Nat Commun 17, 2013 (2026). https://doi.org/10.1038/s41467-026-68760-2
Palabras clave: cardiopatía congénita, diferenciación de cardiomiocitos, señalización Wnt, modelos cardíacos con células madre, regulación génica